
- •Физические основы микроэлектроники
- •Глава 1. Структура и физико-механические свойства твердых тел
- •1.1. Кристаллизация
- •Структура идеальных кристаллов
- •Обозначение узлов, направлений и плоскостей в кристалле.
- •Жидкие кристаллы
- •Молекул в кристаллической (а), жидкокристаллической (нематической) (б) и жидкой (в) фазах
- •И смектической (б) фазах
- •Типы межатомной связи и классификация твердых тел
- •Кристаллов с ковалентной связью: а — элементы группы ivb;
- •Дефекты реальных кристаллов
- •Внедрения (а) и замещения (б)
- •Диффузия в твердых телах
- •Два соседних узла решетки, один из которых занят атомом а, другой вакансией в
- •Распределение примеси в частных случаях диффузионного процесса
- •1. Диффузия из источника с постоянной поверхностной концентрацией.
- •2. Диффузия из тонкого слоя с фиксированным количеством примеси.
- •Температурная зависимость коэффициента диффузии.
- •Поверхностная диффузия.
- •Деформационные свойства кристаллических тел
- •Рекристаллизация
- •Дислокации
- •Перпендикулярной линии дислокации
- •Явления упрочнения
- •Физические свойства пленок и покрытий
- •Адгезия пленок и покрытий
- •Формирование адгезионной связи.
- •1. Пластичные металлы в месте соприкосновения подвергаются сильной пластической деформации (рис. 2.12), при которой полностью сминаются все неровности. Так осуществляется холодная сварка.
- •Тела жидкостью
- •Функции распределения невырожденного и вырожденного газов
- •Ферми — Дирака для вырожденного газа при абсолютном нуле.
- •Влияние температуры на распределение ферми — дирака.
- •Тепловые свойства твердых тел. Понятие о нормальных колебаниях решетки
- •Элементы зонной теории твердых тел зонный характер энергетического спектра кристаллов
- •Образование энергетических зон.
- •Эффективная масса электрона
- •Заполнение зон электронами; деление на проводники, диэлектрики и полупроводники
- •Собственные полупроводники
- •Примесные уровни в полупроводниках
- •Статистика носителей заряда в полупроводниках.
- •Положение уровня ферми и концентрация свободных носителей заряда в собственных и примесных полупроводниках
- •Основные и неосновные носители.
- •Неравновесные носители
- •Электропроводность твердых тел
- •Электропроводность металлов и сплавов
- •Электропроводность металлических сплавов.
- •Эффекты сильного поля
- •Явление сверхпроводимости
- •Температуры
- •Потенциального барьера при эффекте Шоттки
- •Контактная разность потенциалов
- •Электронно-дырочный переход. Методы получения р-п-перехода
Типы межатомной связи и классификация твердых тел
По характеру сил связи твердые кристаллические тела можно разделить на четыре группы:
- ионные кристаллы, в которых основным видом связи является ионная;
- атомные кристаллы, в которых основные связи ковалентные;
- металлические кристаллы с характерной металлической связью;
- молекулярные кристаллы, в которых связь осуществляется в основном силами Ван-дер-Ваальса.
Число К ближайших соседей, окружающих ион (атом) в решетке, называют координационным числом решетки.
Атомные (ковалентные) кристаллы. Для уяснения природы ковалентной связи рассмотрим простейший пример взаимодействия двух атомов водорода (рис. 1.13, а).
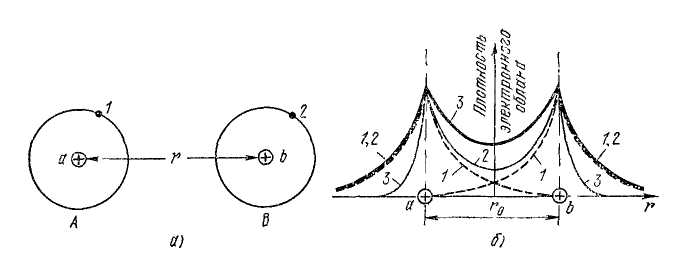
Рис 1 13. К объяснению природы ковалентной связи в молекуле водорода:
а — схематическое изображение атомов водорода А и В; a, b — ядра атомов,
1 — электрон атома А, 2 — электрон атома В,
б — распределение электронной плотности в системе из двух атомов водорода: 1 — распределение электронной плотности в изолированных атомах Н, 2 — электронная плотность, которая получилась бы при простом наложении электронных облаков изолированных атомов, сближенных до расстояния r0, 3 — действительное распределение плотности в молекуле Н2
При r 2 Ǻ наступает перекрытие электронных облаков этих атомов. Электроны в этом состоянии принадлежат одновременно обоим ядрам, обобществлены.
Энергию связи, возникающую в результате по-парного обобществления электронов, называют обменной.
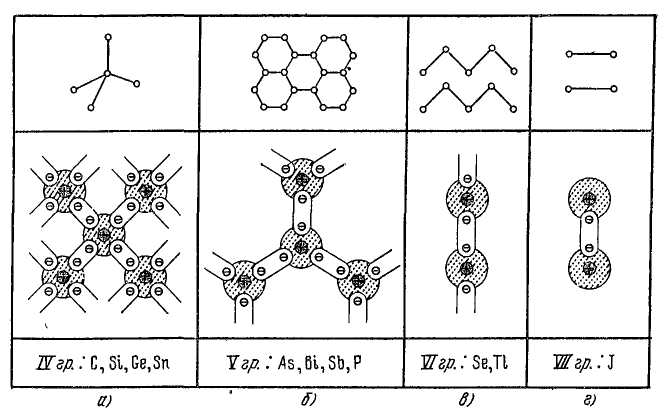
Рис. 1.14. Схематическое изображение структуры
Кристаллов с ковалентной связью: а — элементы группы ivb;
б —элементы группы VB;
Алмаз, кремний, германий являются элементами IV группы. Поэтому они имеют тетраэдрическую решетку, в которой каждый атом окружен четырьмя ближайшими соседями, как показано на рис. 1.14, а.
Ковалентные кристаллы обладают высокой прочностью, твердостью, имеют высокие точки плавления и теплоты сублимации.
Дефекты реальных кристаллов
Примеси. Твердые тела всегда содержат примеси. Процесс растворения состоит в том, что примесные атомы внедряются в промежутки между атомами кристалла (рис. 1.15, а) или замещают часть этих атомов, размещаясь в узлах решетки (рис. 1.15, б). В первом случае твердый раствор называется раствором внедрения, во втором — раствором замещения. Присутствие чужеродных атомов вызывает искажение решетки.
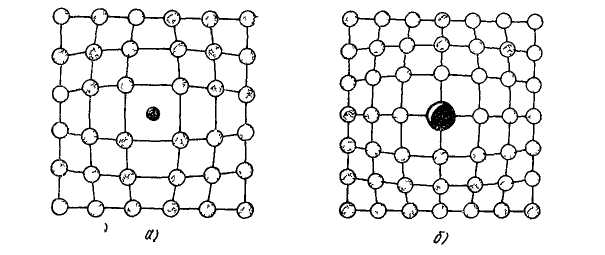
Рис.1.15. Искажение кристаллической решетки в твердых растворах
Внедрения (а) и замещения (б)
Дефекты по Френкелю и по Шоттки. При любой температуре в кристалле атомы, обладающие достаточно высокой энергией, могут удаляться на значительные расстояния от положений равновесия и преодолевать потенциальный барьер (рис. 1.16, а). Процесс сопровождается возникновением вакантного узла и атома в междоузлии. Такого рода дефекты называются дефектами по Френкелю.
При полном испарении атом покидает поверхность кристалла, при частичном испарении он с поверхности переходит в положение над поверхностью (рис. 1.16, б). В поверхностном слое кристалла образуется вакансия. Путем замещения вакансия перемещается внутрь кристалла. Такого рода вакансии называют дефектами по Шоттки.
