- •Кристаллография и минералогия
- •Для студентов высших учебных заведений
- •Предисловие
- •Содержание
- •Введение
- •Основы кристаллографии
- •Глава 1. Аморфные и кристаллические вещества
- •Историческая справка о развитии геолого-минералогических наук. Закон Стенона
- •1.3 Аморфные и кристаллические вещества
- •1.4 Основные свойства кристаллов
- •Глава 2. Зарождение и рост кристаллов
- •2.1 Пути образования кристаллов
- •2.2 Выращивание кристаллов из растворов
- •Факторы, влияющие на облик кристаллов
- •Практическое значение кристаллизации растворов в технологии силикатов
- •2.5 Кристаллизация из расплавов и стекол
- •2.6. Промышленные методы выращивания кристаллов
- •Глава 3. Симметрия кристаллов и их классификация
- •3.1 Элементы симметрии
- •Р исунок 3.1 - Центр симметрии
- •3.2 Взаимодействие между элементами симметрии в кристалле
- •3.3 Классификация кристаллов
- •Глава 4. Простые формы и их комбинации в кристаллах различных сингоний
- •4.1 Распределение простых форм по сингониям и категориям
- •Расшифровка комбинированных форм
- •Глава 5. Установка кристаллов. Определение индексов граней
- •5.1 Понятие о кристаллографических символах
- •Установка кристаллов
- •5.3 Закон Гаюи
- •5.4 Практические рекомендации по определению кристаллографических символов
- •Глава 6. Стереографические проекции кристаллов
- •6.1 Принципы стереографического проектирования
- •6.2 Проектирование элементов симметрии кристаллов
- •Глава 7. Изучение пространственной решетки
- •7.1 Решетки Браве
- •7.2 Определение формульной единицы
- •7.3 Координационные числа и координационные многогранники
- •Глава 8. Плотнейшие упаковки
- •8.1 Понятие о кристаллохимическом радиусе
- •8.2 Виды плотнейших упаковок в структурах
- •8.3 Доля заполненных пустот
- •Глава 9. Типы физико-химических связей в кристаллах
- •9.1 Типы кристаллических структур
- •9.2 Металлический тип связи
- •9.3 Ионная или гетерополярная связь
- •9.4 Ковалентная (гомеополярная) или атомная связь
- •9.6 Водородная связь
- •9.7 Явление поляризации в кристаллических телах
- •Глава 10. Полиморфизм, изоморфизм
- •10.1 Определение полиморфизма, его типы
- •10.2 Примеры полиморфных переходов
- •10.3. Полиморфные превращения в системе SiO2
- •10.4 Понятие об изоморфизме
- •10.5 Виды изоморфизма
- •Глава 11. Главнейшие типы кристаллических структур
- •11.1 Способы моделирования кристаллов. Метод координационных полиэдров
- •11.2 Понятие о структурном типе
- •11.3 Примеры основных структурных типов
- •Тема 12. Кремнекислородные структуры
- •12.1 Особенности строения силикатов
- •12.2 Состав силикатов в виде структурных формул
- •12.3 Классификация силикатов по типу кремнекислородных группировок (радикалов, мотивов)
- •12.4 Особенности структур кварца, тридимита, кристобалита
- •Глава 13. Дефекты кристаллической решетки
- •13.1 Классификация дефектов кристаллической решетки
- •13.2 Нульмерные (точечные) дефекты
- •13.3 Линейные дефекты
- •13.4 Свойства дислокации
- •13.5 Влияние дислокации на скорость роста кристаллов
- •Минералогия
- •Глава 14. Минералогия. Свойства минералов
- •14.1 Наука «минералогия» и объекты ее исследования. Написание формул минералов
- •14.2 Морфология минералов
- •14.3 Явление двойникования и эпитаксии в реальных кристаллах
- •14.4 Физико-химические свойства минералов
- •Тема 15. Геологические процессы образования минералов
- •15.1. Классификация минералов и горных пород по генезису
- •15.2.Эндогенные процессы образования минералов и пород
- •15.3 Экзогенные процессы минералообразования
- •15.4 Метаморфические процессы минералообразования
- •Глава 16. Классификация минералов. Особенности различных классов минералов
- •16.1 Классификация минералов по с.Д. Четверикову
- •16.2 Класс самородных элементов
- •16.3 Сульфиды. Сульфаты
- •16.4 Галоидные соединения. Бораты. Фосфаты
- •16.5 Карбонаты. Нитраты
- •16.6 Оксиды и гидроксиды
- •Глава 17. Силикаты
- •Основные сведения о силикатах
- •17.2 Островные силикаты
- •17.3 Цепочечные и ленточные силикаты
- •17.4 Слоистые силикаты
- •17.5 Каркасные силикаты
- •Литература
9.6 Водородная связь
В образовании участвует атом водорода одной молекулы или ёе радикала (ОН или NН, как правило) и атомы N, O, F, Cl, S соседних молекул. Т.е. связь образуется между положительно поляризованным атомом водорода и отрицательно поляризованными атомами с большой электроотрицательностью (N, O, F, Cl, S).
Например, при образовании молекулы воды между атомами водорода и кислорода образуется полярная ковалентная связь. Электронное облако сильно смещено к атому кислорода, который характеризуется высокой электроотрицательностью. В результате атом О приобретает отрицательный заряд, а атом Н – положительный заряд. Между +Н одной молекулы и – О другой молекулы возникает электростатическое притяжение. Таким образом, это разновидность ван-де-ваальсовской молекулярной связи, но более прочная.
Примеры: сезонный минерал лед, минералы пакетного строения – каолинит Al2O3 2SiO2 2H2O.
И ван-дер-ваальсовская и водородная связь обусловлены явления поляризации молекул.
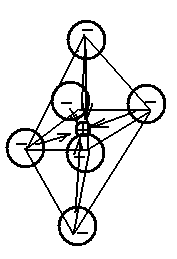
9.7 Явление поляризации в кристаллических телах
Считать ионы несжимаемыми шарами можно только в глубоком приближении. В электрическом поле решетки электронные оболочки ионов деформируются и они поляризуются.
|
Рисунок 9.1 – Явление поляризации |
Поляризуемость аниона тем сильнее, чем больше его радиус.
Поляризующее действие катиона тем интенсивнее, чем меньше его радиус и больше его заряд.
AgFAgCl AgBrAgJ (поляризуемость анионов увеличивается)
Поляризация может привести к уменьшению расстояния между частицами, поскольку сферы ионов как бы взаимно проникают друг в друга, как бы сплющиваются.
В связи с этим, поляризация может вызвать изменение координационного числа и типа структуры.
Пример – изменение типа структуры в ряду галоидных соединений серебра. Ион Ag+, имеющий 18 электронов во внешней оболочке, оказывает сильное поляризующее действие, а ионы галогенов поляризуются тем легче, чем больше их радиус, т.е. в ряду F Cl Br J. Ввиду сильной поляризации йода, координационное число 6, характерное для AgF, AgCl, AgBr (структурный тип NaCl), для AgJ заменяется координационным числом 4 (структурный тип сфалерита ZnS).
Кроме того, явление поляризации оказывает значительное влияние на формирование структурных мотивов. Например, в кристаллах типа CdCl2, CdJ2, MoS2 в результате поляризации происходит параллельная ориентировка групп атомов, вследствие чего образуются слоистые структуры. Состоят из пакетов, каждый из которых представляет собой слой катионов кадмия или молибдена между двумя слоями сильно поляризованных анионов (SCd2+S). Внутри пакетов связь имеет электростатический характер между положительно и отрицательно заряженными ионами, а между пакетами, обращенными друг к другу одинаково заряженными анионами, силы связи имеют характер остаточный, поляризационный.
Глава 10. Полиморфизм, изоморфизм
10.1 Определение полиморфизма, его типы
Полиморфизм – свойство веществ давать в различных термодинамических условиях две или несколько модификаций с одинаковым химическим составом, но с различной кристаллической структурой и соответственно с различными физико-химическими свойствами. Полиморфизм простых элементов принято называть аллотропией. Для различных полиморфных модификаций одного и того же вещества приняты буквенные обозначения , , и т.д.
Типы полиморфизма:
1. Превращения в первой координационной сфере - изменяется координационное число. Приводит к нарушению в расположении ближних соседей и созданию нового типа решетки.
Пример: модификация кварца SiO2, где к.ч. Si/О=4, имеет плотность d =2,3-2,65 г/см3, тогда как для стишовита, где к.ч. Si/О=6, характерна плотность d=4,35г/см3.
2. Превращения во второй координационной сфере – изменяется пространственное расположение координационных многогранников (полиэдров). Меняется дальний порядок связей, а ближний порядок сохраняется, то есть координационное число не меняется.
Пример: переход -кварца в -кварц, сфалерит-вюртцит.
3. Превращения с изменением типа связи.
Пример: серое олово () имеет ковалентный тип связи белое олово () -металлический тип связи; графит (ковалентный тип в слоях и Ван-дер-ваальсовский между слоями) алмаз (ковалентный).
Кроме того, различают полиморфизм:
а
 )
энантиотропный (обратимый) обозначается
;
)
энантиотропный (обратимый) обозначается
;
б ) монотропный (необратимый ) обозначается .
Те или иные полиморфные модификации данного вещества устойчивы при определенных физико-химических условиях, в определенных интервалах температур и давлений. Изменение этих условий может привести к полиморфному превращению. Во многих случаях, однако, скорость превращения настолько мала, что неустойчивая при данных условиях модификация тем не менее существует в этих условиях. В этой связи полиморфные модификации могут быть стабильными или метастабильными. И поэтому, в обычных условиях возможно существование обеих модификаций одного и того же вещества (алмаз – графит).
Можно и искусственно вызвать торможение превращений неустойчивых модификаций в устойчивые. Например, переохлаждением расплава, введением примесей и т.д.