
ДЕСТРУКЦИЯ ПОЛИМЕРОВ (от лат. destructio- разрушение), общее назв. процессов, протекающих с разрывом хим. связей в макромолекулах и приводящих к уменьшению степени полимеризации или мол. массы полимера.
В зависимости от места разрыва хим. связей различают деструкцию (Д.) в основной и боковых цепях полимера. Д. в основной цепи может протекать по закону случая (равновероятный разрыв хим. связи в любом месте микромолекулы) и как деполимеризация (отщепление мономерных звеньев с концов полимерной цепи). Часто причиной Д. п. является одновременное действие неск. факторов, напр., тепло и О2 приводят к термоокислит. Д. Нередко всю сумму превращений, происходящих в полимере под действием внеш. факторов, наз. Д. Д. - одна из причин старения полимеров . Как правило, она является цепным процессом и включает след. осн. стадии:
1) инициирование (образование активных центров Д.);
2) продолжение, или развитие, цепи (совокупность р-ций с участием активных центров, приводящих к изменению хим. структуры и физ. св-в полимера);
3) обрыв кинетич. цепи (процессы дезактивации активных центров).
Термическая Д. (под действием высоких т-р в отсутствие О2 и др. факторов) в зависимости от типа полимера происходит с заметной скоростью выше 230-430 °С. Процесс в большинстве случаев протекает по радикально-цепному механизму. Осн. стадии его можно рассмотреть на примере полиэтилена. Инициирование (самая медленная стадия) осуществляется в результате термич. распада макромолекулы с образованием макрорадикалов:
Развитие цепи включает изомеризацию радикалов , отщепление молекул мономера (2) или высших олефинов (3), передачу цепи на соседние макромолекулы (р-ция + RH : RH + ) и разрыв макромолекулы (4):
Обрыв цепи происходит при взаимод. двух радикалов.
В зависимости от соотношения скоростей отдельных стадий при термич. Д. образуются разл. кол-ва мономера и продуктов с меньшей мол. массой, чем у исходного полимера, а при глубокой Д. - нередко кокс. Пример сложного процесса, включающего радикальные, ионные и молекулярные р-ции - термодеструкция ПВХ. Фотохимическая Д. (фотолиз) вызывается светом, поглощаемым хромофорными группами полимера, продуктами термич. или термоокислит. его превращения и (или) примесями. При фотолизе, помимо разрыва хим. связей, происходят сшивание, образование двойных связей и своб. радикалов. Процесс характеризуют квантовым выходом разрывов цепи (числом разрывов на поглощенный квант света), к-рый для разных полимеров лежит в пределах 10-4-10-1. Радиационная Д. вызывается жесткой ионизирующей радиацией (a-, b- и g-излучением), ускоренными электронами и ионами. Осн. процесс - отщепление водорода и небольших боковых групп, напр. СН3, С2Н5. Из-за высокой концентрации своб. радикалов в относительно небольших участках в-ва эта Д. сопровождается сшиванием макромолекул, в большинстве случаев преобладающим над самой Д. Механическая Д. (механохим.) протекает при действии на твердые полимеры постоянных (статич.) и переменных мех. нагрузок или при перемешивании расплавов и р-ров полимеров. Первая стадия этой Д. - разрыв полимерной цепи под действием напряжений:
Далее в полимере могут протекать те же процессы, что и при термич. Д. Действие на полимеры хим. в-в приводит к окислительной (О2) или химической (О3, вода, к-ты, щелочи, Сl2 и т. п.) Д. Последнюю подразделяют на озонную, гидролитич. и др. Окислительная (или термоокислительная) Д. -многостадийная цепная р-ция. Осн. стадии:
Инициирование (зарождение цепи): (где RH - мономерное звено полимера, напр. ~ СН2—СН2 ~).
Развитие цепи
Разветвление цепи протекает в результате распада гидропероксидных групп
Обрыв цепи происходит в результате рекомбинации и диспропорционирования радикалов, гл. обр. пероксильных ( : ROOR + О2).
При распаде пероксидов ROOR часть радикалов регенерируется. Большую роль в обрыве цепи играют низкомол. радикалы (НО*2, и др.). Скорость термоокислит. Д., как правило, значительно выше, чем термической. При одновременном действии света и О2 происходит фотоокислительная Д., при к-рой зарождение и разветвление цепи являются фотохим. процессами Разветвление цепи может протекать вследствие фотолиза гидро-пероксидов и образования новых хромофорных групп (напр., кетонных, кетоимидных). Озонная Д. сопровождается окислит. процессами. Вследствие высокой реакц. способности О3 протекает в поверхностных слоях полимера, в к-рых происходят глубокие превращения, приводящие к растрескиванию.. Гидролитическая Д. (одновременное действие воды и к-т или щелочей) в обычных условиях также протекает в поверхностных слоях и ограничивается диффузией воды, к-т или щелочей. Биологическая Д. вызывается ферментами, выделяемыми микроорганизмами, организмами высших растений и животных. Особое значение имеет Д. в тканях человека. В большинстве практически важных случаев Д. - вредный процесс, приводящий к изменению св-в полимеров и даже к разрушению изделий из них. Для борьбы с Д. разработаны разнообразные методы стабилизации полимеров . В ряде случаев стойкость к Д. - осн. фактор, определяющий возможность использования полимера в конкретных условиях эксплуатации; это ставит задачу прогнозирования стабильности полимеров или материалов на его основе. Однако в нек-рых случаях Д. может иметь положит. значение. Так, контролируемой Д. получают нек-рые полимеры, напр., поливиниловый спирт - щелочным гидролизом поливинилацетата. Для регулирования технол. св-в каучуки подвергают пластикации (многократной деформации на вальцах в присут. воздуха), в процессе к-рой происходит механоокислит. Д. Поверхностный гидролиз используют для придания шероховатости изделиям из полиэфиров и эфиров целлюлозы и снижения их электризуемости. Гидролитич. Д. целлюлозы и крахмала получают сахара. Для повышения адгезии изделий из полиолефинов к клеям и металлам проводят поверхностное окисление их с помощью сильных окислителей или электрич. разряда. Д. применяют также для установления хим. строения полимеров.
Стабилизация полимеров
Антиоксиданты (термостабилизаторы)
Полимеры подвержены окислению. Это приводит к изменению вязкости, цвета, охрупчиванию изделий и ухудшению физико-механических характеристик. Окисление происходит на каждой стадии существования полимерного материала – при его производстве и хранении, при переработке в изделия и последующем использовании. Окисление также называют деструкцией или старением. Обычно разделяют термомеханическую (в процессе переработки) и термоокислительную (эксплуатация изделия) деструкцию полимерного материала. Различные полимерные материалы обладают различной стойкостью к старению – например, полипропилен сильно подвержен деструкции даже при комнатной температуре, а полистирол и полиметилметакрилат (оргстекло) стабильны даже при температурах переработки.
Изделия из чистого полимера используются чрезвычайно редко, а композиции содержат различные функциональные добавки, а также наполнители, пигменты и т.д., которые могут влиять на окислительные процессы в полимерной матрице.
Механизм окисления полимеров
Процесс взаимодействия полимеров (и других органических соединений) с кислородом называется автоокислением, и представляет собой свободнорадикальную цепную реакцию. Как и все свободнорадикальные реакции, процесс автоокисления необратим, и состоит из трёх стадий: инициирование, рост и разветвление, передача и обрыв цепи. В большинстве случаев процесс окисления полимеров характеризуется наличием индукционного периода, в течение которого не происходит видимых изменений.
Механизм возникновения первичных свободных радикалов, инициирующих реакцию, ещё окончательно не выяснен. Прямая реакция углеводородов с молекулярным кислородом кинетически и термодинамически не выгодна. Образование радикалов можно объяснить взаимодействием переходных металлов или пероксидов (катализаторов), примесей в мономере со следами кислорода во время полимеризации, приводящих к образованию активных пероксидных радикалов, которые отщепляют водород от цепи полимера, и образуют алкил радикалы. Энергия активации реакции алкил радикалов с кислородом очень низка, поэтому реакция идёт очень быстро при любой температуре с образованием пероксидных радикалов. Реакция отрыва водорода пероксидным радикалом от полимерной цепи обладает довольно высокой энергией активации, и является лимитирующей стадией в процессе автоокисления.
В полукристаллических полимерах, к которым относятся полиолефины, термоокислительная деструкция представляет собой гетерогенный процесс. Морфология полимера в значительной степени влияет на процесс диффузии и растворения кислорода, который в полиолефинах происходит преимущественно в аморфных областях. Механические свойства полиолефинов в значительной степени определяются зацеплениями проходных молекул, поэтому окисление в этих областях быстро приводит к снижению прочностных характеристик.
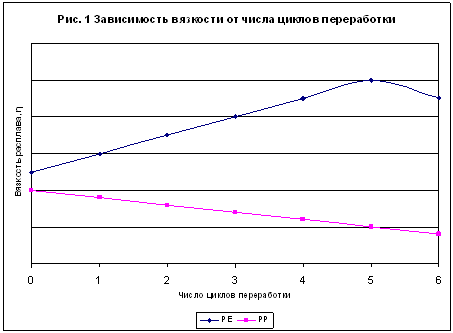
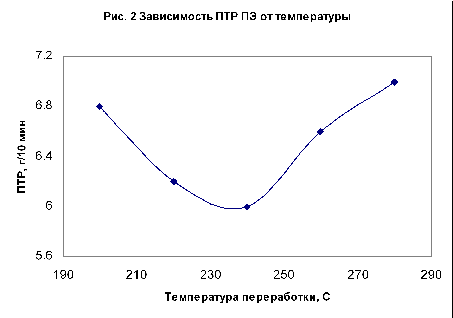
Основное влияние на свойства оказывают реакции, приводящие к изменению молекулярной массы и молекулярно-массового распределения полимеров – реакции обрыва цепи и сшивания (образование гель-фракции). Эти изменения приводят к снижению физико-механических свойств и усложняют переработку полимерных материалов. Рис. 1, 2
Типы антиоксидантов
Термоокислительная деструкция полимеров может быть замедленна путём введения соответствующих стабилизаторов, называемых антиоксидантами. Антиоксиданты подразделяются на 2 большие группы – первичные (защищающие готовые изделия в течение всего срока службы) и вторичные (защищают полимер в процессе переработки в изделия).
Кроме этих двух основных типов существуют так называемые дезактиваторы металлов. Хорошо известно, что ионы переходных металлов (например, меди) ускоряют реакции разложения полимеров. Дезактиваторы образуют стабильные комплексы с металлом и снижают скорость реакции.
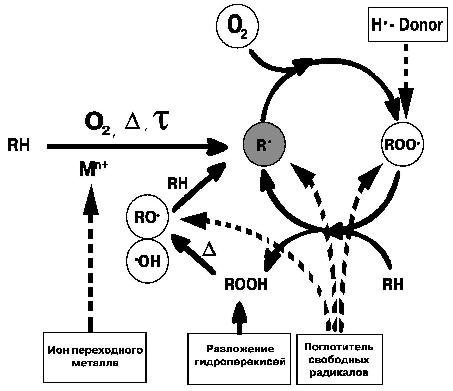
Рисунок 3. Механизм ингибирования реакции автоокисления антиоксидантами разных типов.
· Первичные антиоксиданты. Также называются донорами протона и поглотителями свободных радикалов. К этому классу относятся замещённые фенолы, вторичные ароматические амины и производные бензофурана. В качестве поглотителей свободных радикалов обычно используются HAS (подробнее о HALS см. Полимерные Материалы № 43)
Соединения этого типа представляют собой массивную, малоподвижную молекулу с подвижным, легко отщепляющимся атомом водорода, который реагирует со свободным радикалом. Активность образующегося после отщепления водорода радикала существенно ниже активности алкил радикала полимера.
Фенольные антиоксиданты обладают рядом неоспоримых преимуществ – высокоэффективны, не летучи, разрешены к применению в прямом контакте с пищевыми и косметическими продуктами. Кроме того, в соответствии с европейским и американским законодательством разрешено использовать природный антиоксидант витамин Е (a-d токоферол).
Применение вторичных и ароматических аминов в пищевой упаковке ограниченно, кроме того, они могут вызвать изменение цвета изделия, поэтому применяются в основном в окрашенных в тёмные цвета изделиях. Фенольные антиоксиданты также способны в соответствующих условиях образовывать окрашенные производные бензохинона, поэтому в процессе переработки может потребоваться не только защита полимера, но и защита первичного антиоксиданта.
Антиоксиданты данного типа особенно эффективны при стабилизации полиэтилена низкой и высокой плотности (0,01-0,1 %масс.), особенно в кабельной и трубной изоляции, полипропилена (в трубах горячего водоснабжения); полистирола и его сополимеров (УПС, АБС). Также может использоваться для стабилизации ПВХ (растворим в пластификаторе), чтобы предотвратить охрупчивание кабельной изоляции. Возможно также использование в полиамидах и полиуретанах.
Эффективность первичных антиоксидантов значительно повышается в присутствии фосфитов и тиоэфиров (вторичные антиоксиданты), с которыми они образуют синергические смеси. При использовании синергических смесей в таких полимерах как полиэтилен и полипропилен эффективность стабилизирующей системы возрастает в 2-3 раза по сравнению с отдельными компонентами.
· Вторичные антиоксиданты. Взаимодействуют с гидроперероксидами и разрушают их без образования активных радикалов. Образующиеся продукты должны обладать очень низкой реакционной способностью и высокой термической стабильностью. Скорость взаимодействия вторичных антиоксидантов с гидроперекисями должна быть выше скорости термолиза пероксидов. В этом случае стадия роста и разветвления цепи в цикле автоокисления подавляется. Гидропероксиды восстанавливаются до спиртов, а антиоксидант окисляется. К этому классу относятся органические соединения трехвалентного фосфора (фосфиты и фосфониты), металлические соли дитиокарбаматов и дитиосульфатов и тиоэфиры.
Фосфиты и фосфониты считаются наиболее эффективными в группе вторичных антиоксидантов. Они прекрасно подходят для защиты полимеров и первичных антиоксидантов в процессе переработки в изделия. Единственным недостатком таких соединений является чувствительность к гидролитической деструкции, приводящей к образованию кислых соединений, вызывающих коррозию перерабатывающего оборудования. В таких случаях предпочтительнее использовать ароматические фосфиты, которые обладают большей термостабильностью, например тринонилфенил фосфит (TNPP).
Среди сульфосодержащих антиоксидантов наиболее важную роль играют тиоэфиры (эфиры 3,3 тиодипропионовой кислоты). При термическом разложении тиоэфиров выделяются серосодержащие продукты, разлагающие гидроперекиси. Тем не мене, соединения этого типа не обеспечивают стабильности расплава в процессе переработки. Их основное применение – длительная термостабилизация полимеров работающих при высоких (100-1500С) температурах. В основном используются в смесях с фенольными антиоксидантами.
