- •2.1.Углеводороды.
- •2.1.1.Алканы.
- •2.1.2.Циклоалканы.
- •Номенклатура
- •2.1.3.Алкены
- •2.1.4.Алкины
- •2.1.5.Алкадиены
- •2.1.6.Арены
- •2.2.Гидроксисоединения.
- •2.2.1.Одноатомные спирты.
- •2.2.2.Фенолы.
- •2.2.3.Простые эфиры.
- •Приведенное выше расщепление диметилового эфира представляет собой sn2 реакцию. Однако другие простые эфиры могут расщепляться и по механизму sn1. I
- •2.2.6.Двухатомные фенолы.
- •2.3.Оксосоединения.
- •Номенклатура карбонильных соединений.
- •2.4.Карбоновые кислоты
- •2.4.1.Особенности дикарбоновых кислот.
- •2.5.Функциональные производные карбоновых кислот.
- •2.6.Амины.
2.2.2.Фенолы.
Спирты, в которых гидроксильная группа непосредственно связана с атомом углерода ароматического ядра, называются фенолами.

Фенол о-метилфенол, о-крезол
Фенол является сильным дезинфицирующим средством. Под названием “карболовая кислота” его используют в медицинских учреждениях. Дезинфицирующая жидкость “лизол” содержит 2-фенилфенол и 2-бензил-4-хлорфенол, которые обладают бактерицидным действием. Студенты, изучающие микробиологию, знают, что антимикробную активность соединений сравнивают с активностью фенола при помощи так называемого “фенольного коэффициента”.
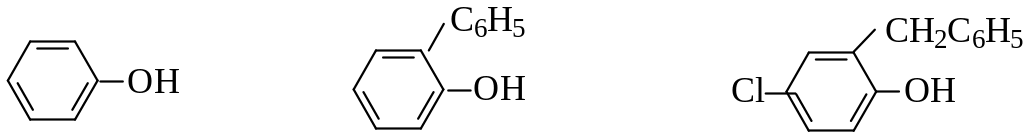
Фенол 2-фенилфенол 2-бензил-4-хлорфенол
Как показывает само название «карболовая кислота», фенолы характеризуются кислотными свойствами. Фенолы гораздо более сильные кислоты, чем спирты, хотя много слабее карбоновых и минеральных кислот и, как кислота, фенол на 9 порядков сильнее обычных алифатических спиртов. (рКа фенола 9.7).Следовательно, кислотные свойства у фенолов ярко выражены. В отличие от алифатических спиртов фенол реагирует с водными растворами щелочей, образуя феноксиды:
C 6H5-OH + NaOH C6H5ONa +H2O,
в то же время в реакцию со слабыми основаниями не вступают:
C 6H5OH + NaHCO3 /
Повышенные кислотные свойства фенолов объясняются тем, что свободная электронная пара кислорода в феноле оттянута к ядру (+ М эффект гидроксильной группы):
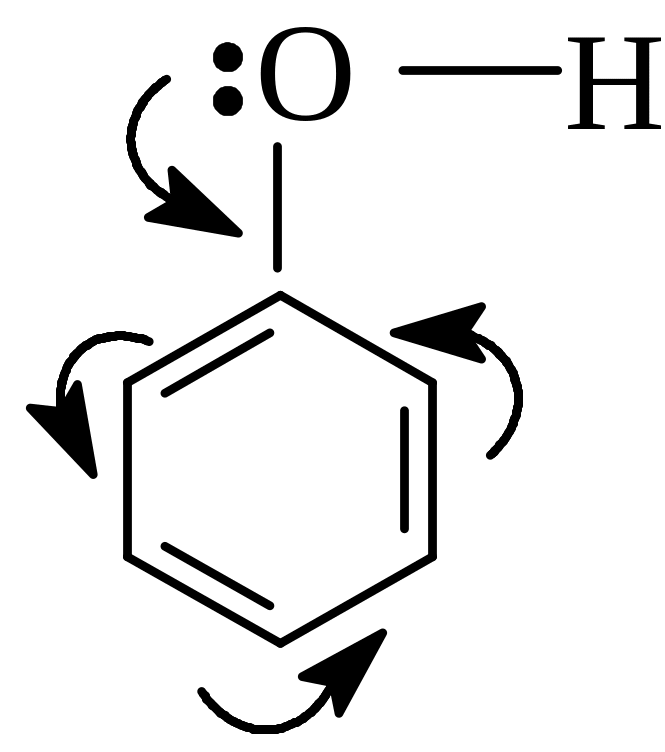
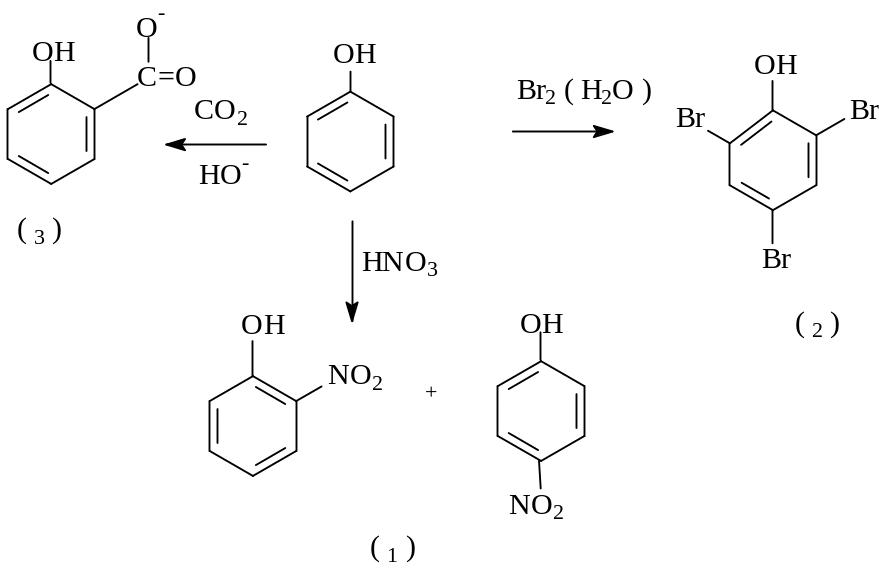
Повышение кислотных свойств фенолов имеет своим следствием понижение основных свойств. В отличие от алифатических спиртов фенолы практически не вступают в реакции нуклеофильного замещения. Наличие в феноле ароматического ядра позволяет получать различные производные фенолов реакциями электрофильного замещения ( SE).Электронодонорная ОН - группа фенолов активирует бензольное кольцо к атаке электрофилами и, в общем, реакции фенолов протекают в значительно более мягких условиях, чем соответствующие реакции бензола. Hапример:
(3) Салициловая кислота (2) 2,4,6-трибромфенол
 ( 1 )
2-нитрофенол 4-нитрофенол
( 1 )
2-нитрофенол 4-нитрофенол
Активность фенолов в реакциях электрофильного замещения настолько велика, что даже альдегиды в присутствии кислоты реагируют с фенолом. На этой реакции основано получение фенолформальдегидных (бакелитовых) смол - дешевых и широко применяемых полимеров.
Ф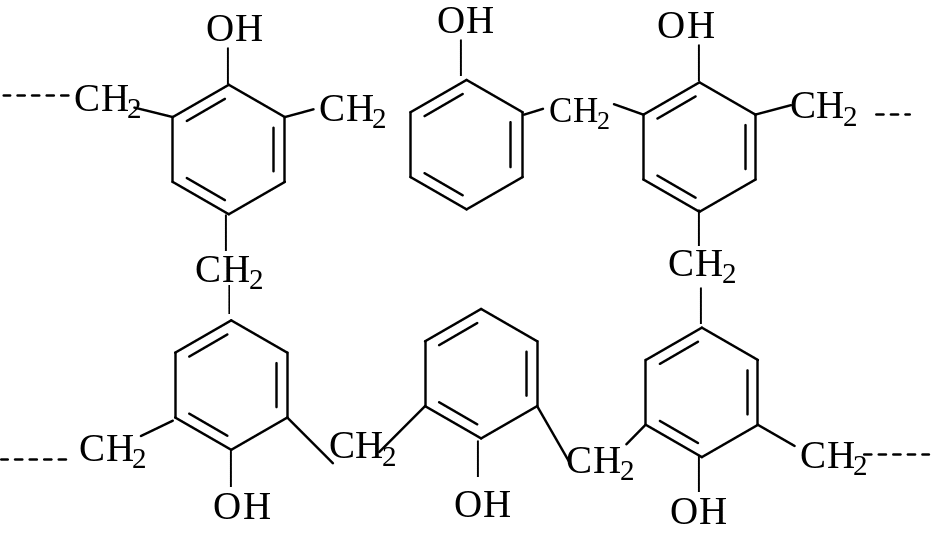 енол
широко используется для получения
лекарственных препаратов на основе
салициловой кислоты.
енол
широко используется для получения
лекарственных препаратов на основе
салициловой кислоты.
Реакция получения салициловой кислоты является еще одним примером активации бензольного ядра под действием гидроксильной группы в щелочных условиях.
Окисление. Фенолы очень легко окисляются самыми разнообразными реагентами, включая атмосферный кислород.
В ряде случаев процесс окисления фенолов оказывается весьма сложным, протекающим с образованием радикалов. Последние являются достаточно устойчивыми вследствие сопряжения с бензольным ядром. На этом основано применение фенолов как ингибиторов в свободно-радикальных реакциях.
Синтез спиртов и фенолов.
Спирты могут быть получены:
1. гидролизом моногалогенпроизводных. Это один из общих способов получения спиртов. Реакция гидролиза идет по механизму SN1 и SN2, в зависимости от строения галогенпроизводного. Например:
2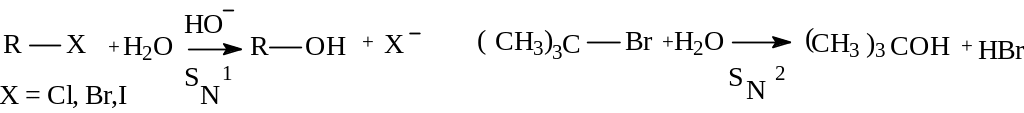 .Гидратация
алкенов. Реакция протекает при нагревании
алкенов с водой в присутствии
катализаторов:серной кислоты, хлорида
цинка и др.
.Гидратация
алкенов. Реакция протекает при нагревании
алкенов с водой в присутствии
катализаторов:серной кислоты, хлорида
цинка и др.
И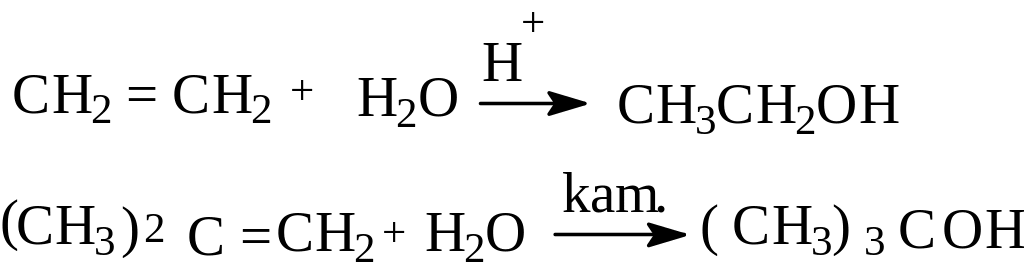 з
этилена получают первичный спирт;
гомологи этилена образуют вторичные и
третичные спирты. Присоединение воды
идет по правилу Марковникова: атом
водорода присоединяется к наиболее
гидрогенизированному атому углерода:
з
этилена получают первичный спирт;
гомологи этилена образуют вторичные и
третичные спирты. Присоединение воды
идет по правилу Марковникова: атом
водорода присоединяется к наиболее
гидрогенизированному атому углерода:
3.Восстановление карбонильных соединений. Альдегиды восстанавливаются до первичных спиртов, кетоны- до вторичных:
4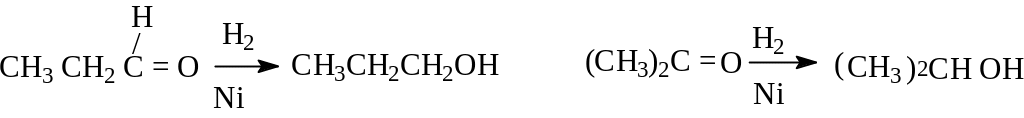 .
Этанол получают ферментацией сахара,
получаемого из природного сырья.
Разработаны способы получения спирта
и из непищевого сырья. Так, например,
этиловый спирт получают при ферментации
углеводов, образующихся при гидролизе
древесины. Это так называемый гидролизный
спирт, применяемый в синтезе каучука.
.
Этанол получают ферментацией сахара,
получаемого из природного сырья.
Разработаны способы получения спирта
и из непищевого сырья. Так, например,
этиловый спирт получают при ферментации
углеводов, образующихся при гидролизе
древесины. Это так называемый гидролизный
спирт, применяемый в синтезе каучука.
Получение фенолов.
1.Гидролиз хлорбензола. Реакция осуществляется в промышленных масштабах при очень жестких условиях (высокая температура и давление)
NaOH
C 6H5Cl C6H5-OH
t , p
2.Сплавление натриевой соли бензолсульфокислоты с едким натром( реакция нуклеофильного замещения) :
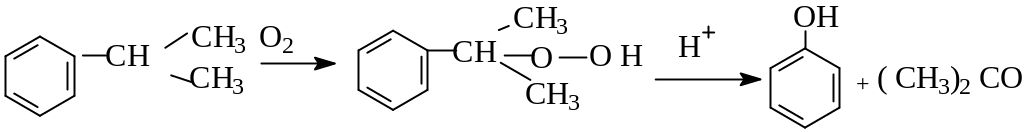
3 .Окисление
кумола:
.Окисление
кумола: