
- •Глава 4. Количественный химический анализ Титриметрический анализ
- •4.1. Общие представления и понятия титриметрического анализа. Способы фиксации точки эквивалентности
- •4.2. Кривая титрования. Подбор индикаторов
- •4.2.1. Кривая титрования и ее области
- •4.2.2 Индикаторы и их подбор
- •4.2.3. Теории, объясняющие изменение окраски индикаторов.
- •4.2.4 Определение интервала перехода для отдельных групп
- •4.2.5 Индикаторные ошибки в кислотно-основном методе титрования.
- •4.3. Методы и способы титрования. Титр, титр по определяемому веществу
- •4.3.1 Способы титрования.
- •4.3.2 Титр раствора и титр по определяемому веществу.
- •4.4. Классификация растворов, применяемых для титрования и способы их приготовления.
- •4.5. Кислотно-основное титрование (протолитометрия). Особенности кривой титрования
- •4.6. Факторы, влияющие на ход кривой титрования, величину скачка и положение точки эквивалентности в протолитометрии
- •4.7. Буферные растворы, классификация буферов и их применение в анализе
- •4.7.1 Классификация буферных систем.
- •4.7.2 Роль буферных растворов в аналитике
- •4.8. Расчет кислотно-основных (протолитических)
- •4.8.1. Растворы гидролизующихся солей.
- •4.8.2. Растворы сильных кислот и оснований.
- •4.8.3. Растворы слабых кислот и оснований.
- •4.8.4 Расчет концентрации протонов в кислотных и основных буферах
- •4.8.5 Определение кислотности среды при смешении растворов.
- •4.8.5.1 Смешение растворов, компоненты в которых не взаимодействуют
- •4.8.5.2 Смешение растворов, компоненты которых взаимодействуют
- •4.8.6 Многоосновные кислоты и многокислотные основания.
- •4.9. Особенности хода кривых титрования различных систем. Условия титрования многокомпонентных систем, многоосновных кислот и их солей
- •4.9.1 Кривая титрования системы сильное – сильное
- •4.9.2 Кривые титрования системы слабое – сильное
- •А) Кривая титрования слабой одноосновной кислоты сильным основанием
- •3. Область скачка, содержащая т.Э.
- •4.9.3 Титрование многоосновных (полипротонных) кислот и оснований
- •4.9.3 Кривые титрования смеси 2-х веществ
- •4.10. Окислительно-восстановительное титрование (редоксиметрия), Кривая титрования и ее особенности.
- •4.11. Расчет кривой титрования с учетом и без учета кислотности
- •4.11.1 Расчет молярной массы эквивалента в редоксиметрии.
- •4.12. Расчет потенциала в точке эквивалентности и значения константы равновесия
- •4.13. Основные виды редоксиметрии и их применение
- •4.13.1. Перманганатометрия
- •4.13.2. Иодометрия
- •4.14. Комплексометрический анализ
- •4.15. Виды комплексов. Понятие дентатности и координационного числа
- •4.16. Комплексоны, используемые для титрования. Применение комплексонометрии
- •4.17. Метод седиментации (осадительное титрование). Кривая титрования, особенности определения точки эквивалентности. Методы Фольгарда и Мора
- •4.17.2 Безиндикаторные способы определения точки эквивалентности.
- •4.17.3. Меркурометрия
4.9.2 Кривые титрования системы слабое – сильное
Система слабое – сильное представляет собой кривые титрования слабого электролита (кислоты или основания) сильным электролитом, взятым в качестве титранта. Особенностью этих кривых является несимметричность относительно линий эквивалентности и нейтральности, так как до точки эквивалентности в таких растворах образуются сопряженные системы: слабый электролит и его соль, которые обладают выраженным буферным действием, замедляющим изменение рН среды. Точка эквивалентности смещена и не совпадает с линией нейтральности в следствии гидролиза продуктов реакции, но она по-прежнему находится в середине скачка. Величина скачка значительно меньше, чем в системе сильное – сильное, поэтому подбор индикатора должен осуществляться с учетом этих особенностей. Существует два вида кривых титрования (КТ) системы слабое – сильное: а) слабой кислоты сильным основанием (титрант); б) слабого основания сильной кислотой (титрант).
А) Кривая титрования слабой одноосновной кислоты сильным основанием
Пусть титруют слабую кислоту сильным основанием, например 0,1 н. раствор CH3COOH – титруемое вещество (X), а 0,1 н. раствор NaOH – титрант (Т). Пример К.Т. такой системы представлен на рисунке 4.16.
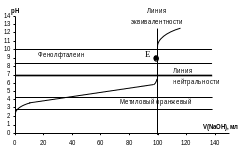
Рисунок 4.16 – Кривая титрования слабой кислоты (0,1н. CH3COOH)
сильным основанием (0,1н.NaOH)
1.
![]() – начальная
точка титрования.
– начальная
точка титрования.
pH раствора определяется концентрацией слабой кислоты Са и значением ее константы диссоциации Kд (раздел 4.8). Обычно величина рН составляет порядка 2 – 4 (выше, чем у сильной кислоты).
2. – область до начала скачка.
Раствор недотитрован. В результате реакции с титрантом образуется соль слабой кислоты и сильного основания, которая вместе с остатком неоттитрованной кислотой образует сопряженную систему – кислотный буфер: CH3COOHост – CH3COONa, поэтому pH меняется очень медленно и кривая идет почти горизонтально. Вблизи скачка, как и в начале КТ, буферное действие ослабевает и кислотность раствора начинает изменяться несколько быстрее. Для построения этой части КТ используют формулу кислотного буфера (таблица 4.4).
3. область скачка, содержащего Т.Э.
В растворе только продукт реакции – соль, гидролизующаяся по аниону. Для данной системы уравнением, описывающим Т.Э., будет:
CH3COOH + NaOH = CH3COONa + H2O.
Запишем уравнение гидролиза соли CH3COONa:
CH3COO + HOH CH3COOH + OH
т.к. в избытке ионы OH, то Т.Э. в этой системе смещена в щелочную среду и рассчитывается по формулам гидролизующихся солей (таблица 4.4).
Для фиксации Т.Э. применяют индикаторы, срабатывающие при pH > 7, например фенолфталеин. Интервал работы индикатора метилового оранжевого (рис. 4.16) находится вне области скачка и титровать с ним нельзя.
4. раствор перетитрован .
Титруемый раствор содержит избыток титранта NaOH, концентрация которого и определяет свойства системы, поэтому значения pH будут меняться достаточно быстро. Влиянием образовавшейся соли на ход КТ можно пренебречь, т.к. ее гидролиз подавляется избытком щелочи.
б) Кривая титрования слабого основания сильной кислотой
Пусть титруют слабое основание сильной кислотой, например 0,1 н. раствор NH4OH – титруемое вещество (X), а 0,1 н. раствор HCl – титрант (Т). Пример КТ такой системы представлен на рисунке 4.17. Вычисление значений рН также выполняют по формулам, приведенным в разделе 4.8, таблица 4.4.
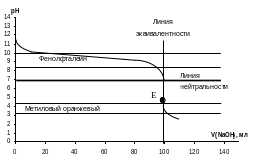
Рисунок 4.17 – Кривая титрования слабого основания (0,1н. NH4OH)
сильной кислотой (0,1н. HCl)
1. – начальная точка титрования.
Исходный раствор слабого основания имеет щелочную реакцию и для слабого электролита обычно составляет порядка pH = 10 – 12. Значение pH определяется начальной концентрацией раствора С(NH4OH) и константой диссоциации слабого основания Kд
2. – область до скачка.
После начала прибавления титранта – сильной кислоты, в титруемом растворе образуется соль NH4Cl, содержащая катион слабого основания и анион сильной кислоты, которая с остатком неоттитрованного слабого основания образует буферную систему NH4OH NH4Cl (основный буфер), что и определяет общее слабое изменение рН в ходе титрования (рис. 4.17).
В начале титрования, когда количество образовавшейся соли невелико, раствор обладает недостаточно эффективными буферными свойствами, как и вблизи Т.Э., когда в растворе остается незначительное количество слабого основания. В этих областях изменение рН происходит несколько быстрее.
