
- •1. Будова нуклеїнових кислот. Пуринові і пиримідинові азотисті основи, нуклеотиди, мононуклеотиди.
- •2. Окислювальне перетворення глюкозо-6-фосфата (пентозофосфатний шунт), його значення.
- •3. Основні шляхи перетворення амінокислот в організмі: трансамінування, дезамінування, декарбоксилювання.
- •4. Метаболізм нейтральних ліпідів. Біосинтез триацилгліцеролів в печінці та кишечнику.
- •5. Заг. Уява про процес аеробного окислення – дихання. Етл мітохондрій тварин, його зв’язок з процесами субстратного ф-ня.
- •6. Рівняння Міхаеліса-Ментен. Константа Міхаеліса та макс. Швидкість ферм. Реакції. Конкурентне та неконкурентне інгібування.
- •7. Структура та властивості ферментів. Ізоферменти. Механізм дії ферментів.
- •8. Дихальний шлях. Енергетика переносу електронів. Спряженість окисного фосфорилювання з процесом перенесення електронів.
- •9. Мембранозв'язані етл. С-ми синтезу стероїдів в мх. Мікросомальні етл. Дихальна с-ма мітохондрій.
- •10. Простагландини, тромбоксани і лейкотрієни. Характеристика. Біологічна роль. Молек. Механізм дії.
- •11. Характеристика гістонових та негістонових білків. Ковалентні модифікації. Біохімічні механізми конденсації та деконденсації хроматину.
- •12. Ліпіди. Властивості, розповсюдження, класифікація, значення.
- •13. Коферменти, класифікація і роль, зв'язок з вітамінами.
- •14. Перетворення білків у кишково-шлунковому тракті. Протеолітичні ферменти та їх специфічність.
- •15. Процесінг первинних транскриптів. Механізми сплайсингу рнк. Особливості процесінгу тРнк, мРнк, рРнк у про- та еукаріотів. Регуляція експресії генів шляхом альтернативного сплайсингу.
- •16. Енергетика ферментативних процесів. Енергія активації. Рівняння Арреніуса та Вант-Гоффа; Лейдлера-Скетчарда та Бренстеда-б'єрума.
- •17. Біохімічні основи регуляції клітинного циклу. Роль білка mpf, білків сімейства циклінів, ростових факторів та циклін-залежних кіназ.
- •18. Регуляція метаболізму ліпідів, жирова тканина і печінка в регуляції метаболізму ліпідів, регуляція обміну холестеролу.
- •19. Катаболізм вуглеводів, шляхи розпаду вуглеводів у тканинах, анаеробне перетворення вуглеводів.
- •20. Шляхи регуляції вуглеводного обміну, роль адреналіну та інсуліну.
- •21. Характеристика складних ліпідів, фізіологічне значення.
- •23. Молекулярні механізми проведення регуляторних сигналів. Система вторинних посередників.
- •24. Регуляція вуглеводного обміну. Роль гормонів у вуглеводному обміні. Порушення. Цукровий діабет.
- •25. Перекисне окиснення ліпідів. Регуляція пол. Біологічна активність продуктів пол
- •26. Роль білків в процесі реплікації. Поcтреплікативні модифікації днк. Роль рестриктаз у збереженні „чистоти” ген. Інформації.
- •27. Вітамін в12 – кобаломін. Будова вітаміну. Особливості всмоктування вітаміну в тонкому кишечнику. Транскобаломіни. Біологічна роль, будова в12-коферментів.
- •28. Рівні структурної організації хроматину. Хромосома, теломера та теломеразна активність.
- •29. Загальні шляхи обміну амінокислот: трансамінування, процеси дезамінування та декарбоксилювання.
- •30. Молек механізми проведення і підсилення рецепторного сигналу. Основні теорії рецепції. Вторинні месенджери. Механізми проведення та підсилення рецепторного сигналу.
- •31. Кальмодулін – регуляторний тригерний білок, його участь у роботі месенджерних каскадів.
- •32. Катаболізм триацилгліцеролів та фосфоліпідів
- •33. Класифікація кофакторів та їх характеристика.
- •34. Шляхи катаболізму пуринових та піримідинових основ, кінцеві продукти.
- •35. Кінетика та енергетика мембранного транспорту
- •36. Структура та властивості рнк-полімерази.
- •37. Пасивний та активний транспорт через мембрану.
- •38. Кінетика ферментативного каталізу. Швидкість ферментативних реакцій. Енергія активації.
- •39. Система циклічних нуклеотидів:структура, утворення, роль.
- •40. Гормони підшлункової залози, структура, механізм дії.
- •41. Біологічні мембрани та їх функції. Сучасне уявлення про структуру та функції мітохондрій.
- •42. Утворення моносахаридів. Біосинтез оліго- та полісахаридів.
- •43. Гормони щитовидної залози: структура, біологічна роль.
- •44. Характеристика вітамінів а, е, к. Структура, біологічна роль.
- •45. Транспортна рнк, особливості будови, роль в біосинтезі білка.
- •46. Трансамінування амінокислот, його механізм.
- •47. Транскрипція, ферменти транскрипції і її регуляція. Реорганізація хроматину при транскрипції.
- •48. Рівні організації днк, реплікація днк.
- •50. Роль металів у каталітичній активності ферментів.
- •51. Перетворення енергії в живих системах. Шляхи синтезу атф у клітині.
- •52. Молекулярні механізми проведення регуляторних сигналів
- •53. Гормони. Хімічна будова, фізіологічна роль найважливіших гормонів.Молекулярний механізм дії.
- •54. Цикл ди та трикарбонових кислот (цикл Кребса)
- •55. (№7) Ферменти. Структура ферментів, ізоферменти, механізми дії ферментів.
- •56. Структура та роль нуклеотидтрифосфатів.
- •57. Структура і біологічна роль днк.
- •58. Принцип класифікації і номенклатура ферментів.
- •59. Глюконеогенез - синтез глюкози
- •60. Структура, властивості та класифікації амінокислот.
- •61. Мембрани й міжклітинні взаємодії
- •62. Гідроліз білків в шкт. Внутрішньоклітинне перетворення білків.
- •63. Кінетика гальмування (інгібування) ферментативних реакцій
- •64. Шляхи перетворення ліпідів у клітині
- •65. Вуглеводи, будова, властивості, класифікація і роль у живій природі.
- •66. Основні етапи біосинтезу білка на рибосомах
- •67. Анаеробне перетворення вуглеводів. Спиртове бродіння.
- •68. Характеристика хромопротеїдів. Представники. Гемоглобін і транспорт кисню.
- •69. Білки, структура і біологічна функція. Рівні організації білкових структур.
- •70. Шляхи біосинтезу пуринових та піримідинових основ.
- •71. Характеристика активних центрів ферментів.
- •72. Чоловічі статеві гормони.
- •73. Поняття про кінетику ферментативного каталізу.
- •74. Регуляція біосинтезу білка в клітинах.
- •75. Метаболічний розпад пуринів та піримідинів.
- •76. Метаболізм простагландинів.
- •77. Вітаміни а та d: структуру, значення.
- •78. Структура і біологічна роль рнк. Види рнк.
- •79. Порушення обміну вуглеводів. Цукровий діабет.
- •80. Біосинтез сечовини.
- •81. Регуляція метаболізму ліпідів
- •82. Біосинтез фосфоліпідів.
- •83. Регуляція ферментного апарату клітин.
- •84. Розпад та біосинтез полісахаридів.
- •85. Біосинтез жирних кислот (жк)
- •86. Декарбоксилювання амінокислот, роль амінів
- •87. Біогенні аміни та їх значення.
- •88. Дихальний ланцюг (ланцюг переносу електронів).
- •89. Анаеробне перетворення вуглеводів, глікогеноліз.
- •90. Ейкозаноїди - похідні арахідонової кислоти, класифікація, значення.
1. Будова нуклеїнових кислот. Пуринові і пиримідинові азотисті основи, нуклеотиди, мононуклеотиди.
Нуклеїнові кислоти (від лат. пикіеиз - ядро) - це особливий клас ви-сокомолекулярних сполук, які виконують функції збереження й передачі генетичної інформації, визначають вид, форму і склад живої клітини та її функції.
Нуклеїнові кислоти — складні високомолекулярні біополімери, що складаються з ланцюжків нуклеотидів. Природні нуклеїнові кислоти — ДНК і РНК — виконують у всіх живих організмах роль передачі і експресії генетичної інформації.
Основна маса ДНК у клітині локалізована в ядрі - 97-99 %, а 1-3 % припадає на позаядерну ДНК. На відміну від ДНК РНК розподілена у клітині більш рівномірно.
Хімічний склад нуклеїнових кислот
М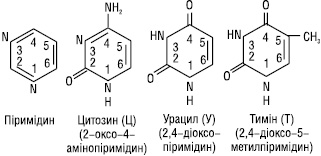 олекули
нуклеїнових кислот (ДНК і РНК) складаються
з великої кількості мономерів-мононуклеотидів,
тобто є полімерами нуклеотидів
(полінуклеотиди).
Нуклеотиди утворені трьома компонентами:
азотвмісною циклічною сполукою -пуриновою
чи
піримідиновою
основою
(основами їх називають тому, що вони
здатні приєднувати Н+),
вуглеводами (пентозами) та фосфорною
кислотою.
олекули
нуклеїнових кислот (ДНК і РНК) складаються
з великої кількості мономерів-мононуклеотидів,
тобто є полімерами нуклеотидів
(полінуклеотиди).
Нуклеотиди утворені трьома компонентами:
азотвмісною циклічною сполукою -пуриновою
чи
піримідиновою
основою
(основами їх називають тому, що вони
здатні приєднувати Н+),
вуглеводами (пентозами) та фосфорною
кислотою.
Піримідинові основи. Ці речовини є похідними шестичленної гетероциклічної сполуки - піримідину. Обидві нуклеїнові кислоти містять одну й ту саму піримідинову основу - цитозин (2-окси-4-амінопіримідин)-Ц. Тимін (5-ме-тил-2,4-діоксипіримідин)-Т переважно входить до складу ДНК, а урацил (2,4-діо-ксипіримідин)-У - РНК. У структурі урацилу та тиміну атом вуглецю в положенні 4 окиснений, а в цитозині - амінований:
Пуринові основи. Пурин є похідним піримідину, гетероциклічна мо-пекула якого складається з піримідинового та імідазольного кілець, що сполучені зв'язками 4-5. З пуринових похідних до складу нуклеїнових кислот обох типів входять переважно дві основи - 6-амінопурин (аденін, А) та 2-амі-но-6-оксипурин (гуанін, Г):
У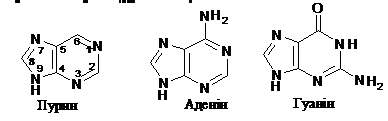 структурі аденіну атом вуглецю в
положенні 6 амінований, а гуаніну
-окиснений.
структурі аденіну атом вуглецю в
положенні 6 амінований, а гуаніну
-окиснений.
Іншими важливими природними похідними пурину є гіпоксантин, ксантин і сечова кислота:
(6-Оксипурин) (2,6-Діоксипурин) (2,6,8-Тріоксипурин)
Вуглеводи (пентози). Вуглеводний компонент нуклеїнових кислот представлений альдопентозами. Вони є О-ізомерами і знаходяться в Р-фуранозній формі:
У нуклеїнових кислотах п'ятичленне фуранозне кільце ніколи не буває плоским. Воно набуває або конформації конверта, або твіст-конформації (напівкрісло). До складу РНК входить р-О-рибоза, а ДНК - р-О-2-дезоксирибоза, в якій ОН-група в положенні 2 атома вуглецю замінена атомом водню. Відсутність у положенні 2 гідроксильної групи в дезоксирибозі надає ДНК більшої стійкості до лужної деградації. Пуринові та піримідинові основи, що містять рибозу або дезоксирибозу, називаються відповідно рибонуклеозидами чи 2'-дезоксири-(юнуклеозидами.
Н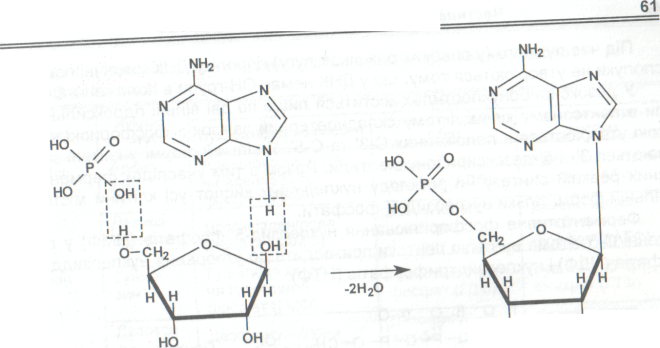 уклеотиди
- це фосфорнокислі етери нуклеозидів,
в яких фосфорна кислота з'єднана
складноетерним зв'язком з однією з
вільних гідроксильних груп пентози.
Назви нуклеотидів походять відназви
основ - аденілова, гуанілова, тиміди-нова,
цитидилова та уридилова кислоти.
Нуклеотиди є сильними кислотами, тому
що залишок фосфорної кислоти легко
дисоціює. Утворення нуклеотидів із
складових призводить до вивільнення
двох молекул води:
уклеотиди
- це фосфорнокислі етери нуклеозидів,
в яких фосфорна кислота з'єднана
складноетерним зв'язком з однією з
вільних гідроксильних груп пентози.
Назви нуклеотидів походять відназви
основ - аденілова, гуанілова, тиміди-нова,
цитидилова та уридилова кислоти.
Нуклеотиди є сильними кислотами, тому
що залишок фосфорної кислоти легко
дисоціює. Утворення нуклеотидів із
складових призводить до вивільнення
двох молекул води:
У клітині вільні нуклеотиди утворюються при синтезі або в результаті часткового гідролізу нуклеїнових кислот ферментами.
Нуклеотиди, що містять О-рибозу, називаються рибонуклеотидами, 2-дез-окси-О-рибозу - дезоксирибонуклеотидами.
Ферментативне фосфорилювання нуклеозид-5'-фосфатів (НМФ) у положенні С-5' атома вуглецю пентози призводить до утворення нуклеозиддифо-сфатів (НДФ) і нуклеозидтрифосфатів (НТФ):
У дезоксирибонуклеотидах дНМФ, дНДФ і дНТФ замість рибози міститься дезоксирибоза. Вільні нуклеотиди мають надзвичайно важливе значення, вони беруть участь у всіх метаболічних процесах. У першу чергу НТФ та дНТФ є активованими попередниками під час синтезу РНК та ДНК та їх кодованими елементами. Система АТФ-АДФ-АМФ бере участь у біоенергетичних процесах.
Нуклеотиди можуть бути алостеричними модуляторами певних регуляторних ферментів - під час біосинтезу пуринових нуклеотидів, гліколізу тощо. Різні похідні нуклеотидів виконують функції коферментів - НАД, НАДФ, ФАД, ФМН, КоА та ін. Окрему групу складають циклічні нуклеотиди (цАМФ, цГМФ, цЦМФ тощо), в яких фосфатний залишок утворює складноетерні зв'язки з 3'- та 5'-ОН-групами рибози. Вони відіграють в організмі роль вторинних посередників при передачі сигналів гормонів.
