
Рішення
Розглянемо приклад рішення для реакції Fe3O4 + CO = 3FeO + CO2 .
Методику наближеного розрахунку вже розглянуто в завданні 3.
Термодинамічні властивості речовин, що беруть участь у реакції, наведено в таблиці 1.
Таблиця 1 – Термодинамічні властивості речовин
-
Вещество
Фаза
FeO
тв.
266,7
54,0
CO2
газ
393,78
213,78
CO
газ
110,60
198,04
Fe3O4
тв
1122,0
146,6
Розрахуємо
 :
:

Розрахуємо :

Отримані
дані
підставимо
в рівняння,
що наведено нижче та обчислимо величини
 і
і
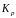 для
заданих температур:
для
заданих температур:

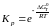
Результати розрахунків:
1)
Т
= 298 К:


2)
Т
= 600 К:
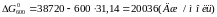

3)
Т
= 1000 К:


4)
Т
= 1500 К:


За результатами розрахунку константи рівноваги побудуємо графік залежності lgКР=f(T).
Як показують розрахунки, з підвищенням температури значення константи рівноваги теж збільшується. Це свідчить про те, що рівновага ендотермічної реакції відновлення гематиту з підвищенням температури зміщується праворуч, в сторону продуктів реакції. Таким чином, вплив температури на рівновагу реакції відновлення позитивний – з підвищенням температури відновлення полегшується. Але, як показує значення , відновлення гематиту газовою сумішшю Н2 – Н2О стає можливим тільки за температур вищих за 1000 К.
