

Гіпоксантин
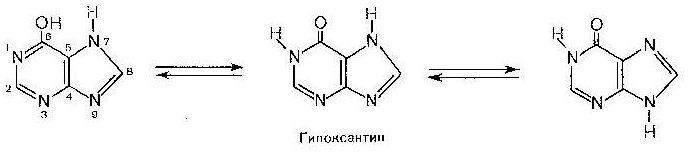
Похідні піридину-коферменти
НАД і НАДН (бере участь в ОВР)
і НАДН (бере участь в ОВР)
R
= РО3Н2
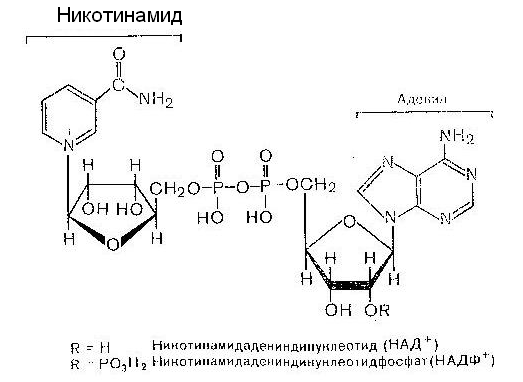
Нікотинамідаденіндинуклеотидфосат
(НАДФ+)
R
= Н
Нікотинамідаденіндинуклеотид (НАД+)
Аденін
форма



Нікотинамід
R
= Н
Нікотинамідаденіндинуклеотид (НАД ·
Н
)

Вітаміни групи В: піридоксальфосфат - бере участь у реакції переамінування
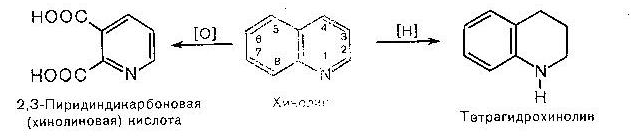
Хінолін
Тетрагідрохінолін
2,3-Піридиндикарбонова
(хінолінова)
кислота

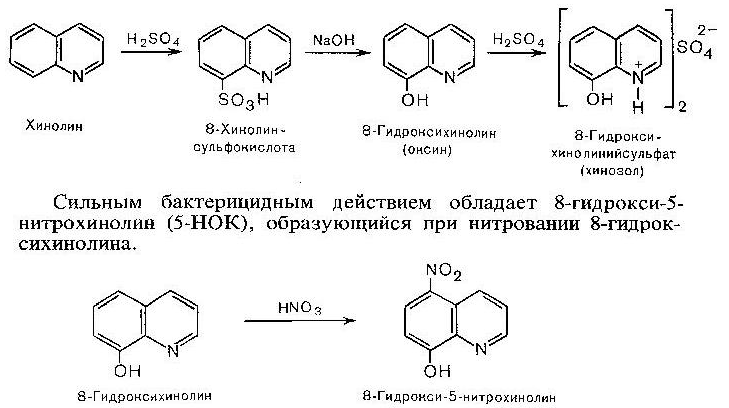
Хінолін і лікарські препарати на його основі:
Сильну
бактерицидну дію має 8-гідрокси-5-
нітрохінолін (5-НОК), що утворюється при
нітруванні 8-гідроксихіноліна.
8-Гідроксихінолін
8-Гідрокси
-5-нітрохінолін
8-Гідрокси
–
хінолінийсульфат
(хінозол)
8-Гідроксихінолін
(оксин)
8-Хінолін
–
сульфокислота
Хінолін





Біологічна дія препаратів гідрокси-хінолінового ряду заснована на їхній здатності до утворення хелатних комплексів з іонами деяких металів і «зв'язуванні» мікроелементів, необхідних для життєдіяльності кишкових бактерій:
8-Гідрокси
-7-йод-5-хлор-
Хінолін
(ентеросептол)
Приклад
утворення хелата
8-Гідроксихіноліна
з іоном
двовалентного
металу (ентеросептол)


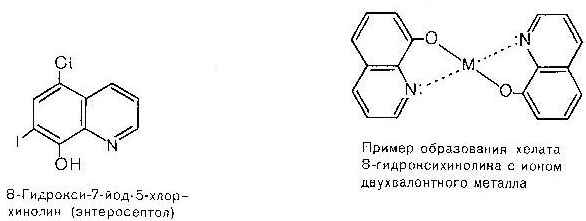
Група піримідину:
1,4-Діазин,
Піразин
1,3-Діазин,
піримидин
1,2-Діазин,
Піридазін

Амінопохідні піримидину
Цитозин
(4-аміно-2-гідроксипіримідин)
Тимін
(2,4-дигідроксм-5-метилпіримідин,
3-метілурацил)
Урацил
(2,4-дигідроксипіримідин)



Сечова кислота - кінцевий продукт метаболізму нуклеїнових основ в організмі
Динатрієва
сіль
сечової
кислоти
Мононатрієва
сіль
сечової
кислоти
Сечова
кислота

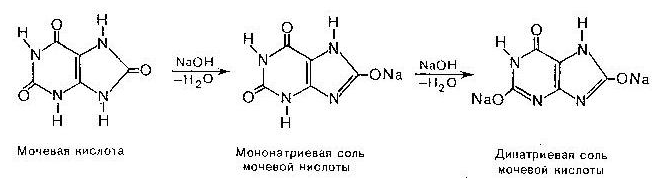
Солі сечової кислоти - урати (при порушенні обміну речовин можуть накопичуватися в суглобах при подагрі, а також у вигляді каменів в нирках.
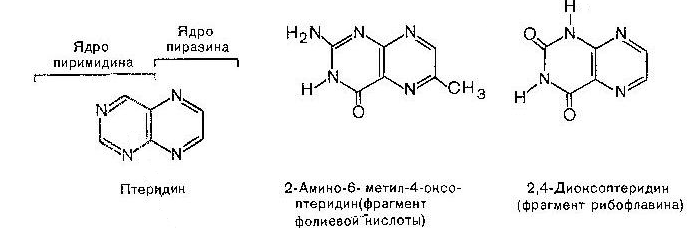
Група птеридина
2,4-Диоксоптеридин
(фрагмент
рібофлавіна)
2-аміно-6-метил-4-оксо-
птеридин
( фрагмент
фолієвої
кислоти)
Ядро
пиразину
Ядро
піримідину



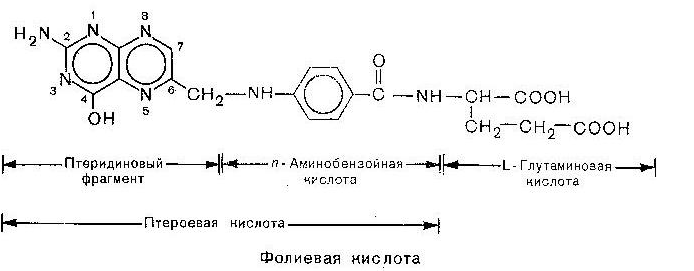
Фолієва кислота (від лат. folium-лист)
Відіграє важливу роль у метаболізмі нуклеїнових кислот і білків:
Птероєва
кислота
Фолієва
кислота
L-Глутамінова
кислота
n-Амінобензойна
кислота
Птеридиновий
фрагмент




Контрольні питання й вправи:
1. Напишіть структурні формули наступних сполук: 1) 1, 2-диазин;
2) 2,4, 6-тригідроксипіримідин; 3) N-Оксид піразина; 4) піперазин; 5) урацил; 6) тимін; 7) цитозин; 8) дибензо[b,е]-4Н-1, 4-тіазин; 9) метиленовий синій.
2. Назвіть наведені сполуки:
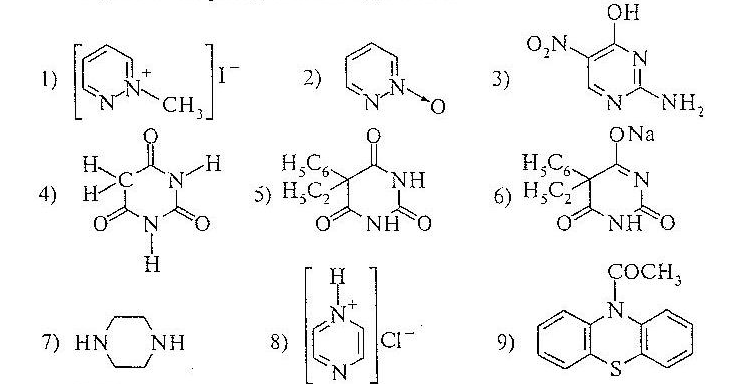
3. Напишіть схеми послідовних хімічних перетворень, що дозволяють одержати: 1) 3, 6-диметилпірідазин з гексан-диона-2,5 і гідразину;
2) піримідин - з малонового ефіру й сечовини; 3) пиразин з этилендиаміну й гліоксаля. Назвіть проміжні продукти.
4. Охарактеризуйте електронну будову диазинів. Поясните, чому диазини, незважаючи на наявність двох основних центрів, утворять солі тільки з одним еквівалентом кислоти. Напишіть відповідне рівняння реакції.
5. Розташуйте в ряд згідно
зниженню основності 1, 2-, 1.3- і 1, 4-диазини,
якщо рКвн-
у воді (20 С) становить: піридазина — 2,33; піримідина
— 1,3; піразина — 0,6. Відповідь пояснить.
С) становить: піридазина — 2,33; піримідина
— 1,3; піразина — 0,6. Відповідь пояснить.
6. Порівняй реакційну здатність піримідину й піридину в реакціях электрофільного й нуклеофільного заміщення (SЕ, SN)- Пояснить розходження, що мають місце. Напишіть відповідні рівняння реакцій.
7. Наявність яких электронодонорних
заступників у молекулі піримідина
сприяє протіканню реакцій S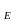 ? Напишіть схеми нітрування
4-гидроксипиримидина й бромування
2-аминопіримідина. Назвіть продукти.
? Напишіть схеми нітрування
4-гидроксипиримидина й бромування
2-аминопіримідина. Назвіть продукти.
8. Приведіть схему одержання барбітурової кислоти з малонового ефіру й сечовини. Напишіть можливі таутомерні перетворення барбітурової кислоти. У структурі найбільш стійкої таутомерної форми барбітурової кислоти вкажіть групи, що обумовлюють кето-єнольну й лактам-лактимну таутомерію.
9. Напишіть схеми й назвіть продукти реакцій барбітурової й 5, 5-диетлбарбітурової кислоти з натрію гідроксидом. Назвіть продукти.
10. Напишіть схеми таутомерних перетворень нуклеїнових основ піримідинового ряду (урацил, тимін, цитозин). Укажіть, яка з таутомерних форм переважає в рівновазі. Назвіть вид таутомерії.
11. Напишіть структурні формули наступних сполук:
1) імідазо[4, 5-d]піримідин; 2) гіпоксантин; 3) ксантин; 4) сечова кислота; 5) аденін; 6) гуанін; 7) теофілин; 8) теобромін; 9) кофеїн; 10) аллоксазин;
11) мурексид; 12) птеридин.
12. Назвіть наступні сполуки:
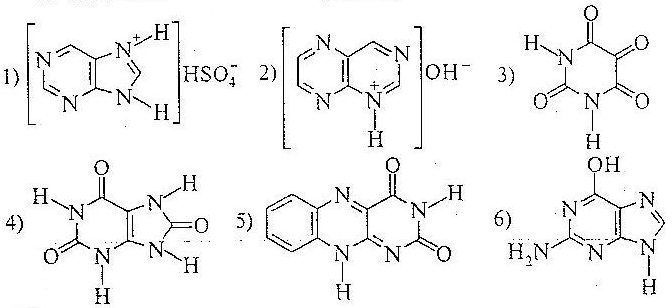
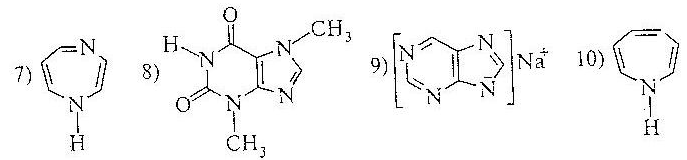
13. Напишіть схему одержання 8-метилпурина з 4 диаміно-піримідина (за методом Траубе).
14. Охарактеризуйте електронну будову пурину. Напишіть
таутомерні форми пурину.
15. Напишіть схеми реакцій, що підтверджують амфотерний характер пурину. Назвіть продукти.
16. Зобразіть структурні формули природних сполук,
до складу яких входить пурин.
17. Приведіть схеми таутомерних перетворень оксопуринів.
Назвіть таутомерні форми.
18. За допомогою яких реакцій можна довести амфотерний характер гіпоксантину й ксантину? Напишіть відповідні рівняння реакцій.
19. Поясніть, чому сечова кислота - двухосновна, а не трьохосновна. Напишіть схеми одержання кислих і середніх солей
сечової кислоти.
20. На прикладі сечової кислоти приведіть схему мурексидної реакції. Назвіть проміжні продукти. Яке значення має дана реакція у фармації?
21. Напишіть схеми реакцій, що доводять наявність у молекулі сечової кислоти піримідинового й імідазольного циклів.
Назвіть продукти.
22. Приведіть рівняння послідовних реакцій, що дозволяють із 2,6, 8-трихлорпурина одержати: 1) аденін; 2) гуанін; 3) гіпоксантин; 4) ксантин. Назвіть проміжні продукти.
23. Напишіть схеми хімічних перетворень, що дозволяють перетворити:
1) сечову кислоту в пурин; 2) аденін у гіпоксантин;
3) 4, 5-диамінопіримідин у птеридин. Назвіть проміжні продукти.
24. Приведіть схеми реакцій, що підтверджують амфотерний характер
N-Метильних похідних ксантину (теофіліну, теоброміну). Чому кофеїн проявляє тільки слабкі основні властивості?
25. Напишіть рівняння реакцій, що дозволяють ідентифікувати
N-Метильні похідні ксантину.
26. Охарактеризуйте будову й хімічні властивості птеридину.
