
- •Галогенопроизводные углеводородов
- •Номенклатура, изомерия
- •Механизм sn1
- •Подвижность галогенов
- •Галогениды аллильного и винильного типа
- •Химические свойства арилгалогенидов
- •Препаративные методы получения спиртов
- •Физические свойства спиртов
- •Химические свойства спиртов
- •Кислотные свойства
- •Основные свойства
- •Реакции замещения он - группы спиртов
- •Способы получения фенолов
- •Химические свойства фенолов
- •Задача 5
- •Решение задачи 5
- •Тема «Спирты, фенолы» Задача 6
- •Решение задачи 6
- •Задача 7
- •Задача 8
- •Решение задачи 8
- •Задача 9
- •Задача 10
- •Вопросы к коллоквиуму №2 «галогенопроизводные, спирты, фенолы»
Галогенопроизводные, спирты, фенолы

Методическое пособие
для подготовки к коллоквиуму 2
Кемерово 2009
Оглавление
Галогенопроизводные углеводородов 3
Номенклатура, изомерия 3
Способы получения галогенопроизводных 4
Замещение атомов водорода в алканах на галоген 4
Замещение атомов водорода в бензоле 4
Получение галогенопроизводных из спиртов 4
Физические свойства 5
Химические свойства 5
Механизм SN2 5
Механизм SN1 6
Подвижность галогенов 7
Галогениды аллильного и винильного типа 7
Химические свойства арилгалогенидов 7
Спирты, фенолы 8
Классификация 8
Номенклатура спиртов 8
Способы получения спиртов 9
Промышленные способы получения 9
Препаративные методы получения спиртов 10
Физические свойства спиртов 11
Химические свойства спиртов 12
Кислотные свойства 12
Основные свойства 12
Реакции замещения ОН - группы спиртов 13
Этанол 14
Многоатомные спирты 15
Способы получения многоатомных спиртов 15
Химические свойства многоатомных спиртов 16
Фенолы 17
Способы получения фенолов 17
Химические свойства фенолов 19
Примеры решения задач 22
Тема «Галогенопроизводные» 22
Тема «Спирты, фенолы» 25
ВОПРОСЫ К КОЛЛОКВИУМУ №2 29
Галогенопроизводные углеводородов
Производные углеводородов, содержащие вместо одного или нескольких атомов водорода галогены называются галогенопроизводными. В зависимости от характера углеводорода, в молекулу которого введен галоген, их делят на галогеналкилы жирного ряда и ароматические галогенопроизводные (галогенарены).
Таблица1
Типы галогеноуглеводородов
Тип галогенуглеводорода |
Формула |
Название |
Алкилгалогениды |
|
Хлорэтан, этилхлорид |
Алкенилгалогениды |
|
Хлорэтен, винилхлорид |
Аллилгалогениды |
|
3 - хлорпропен, аллилхлорид |
Арилгалогениды |
|
Хлорбензол |
Бензилгалогениды |
|
Бензилхлорид |
Номенклатура, изомерия
По рациональной номенклатуре название галогенопроизводных образуют из названия углеводородного радикала и галогена, в необходимых случаях указывают положение последнего.

По систематической номенклатуре положение атома галогена указывают цифрой, которая вместе с его названием располагается перед названием радикала. Нумерацию атомов углерода начинают с того конца молекулы, к которому ближе расположен атом галогена.

Способы получения галогенопроизводных
Замещение атомов водорода в алканах на галоген

Реакции протекают только при повышенных температурах или облучении УФ-светом по гомолитическому (радикальному) механизму. Замещение происходит у третичного атома углерода.
Замещение атомов водорода в бензоле
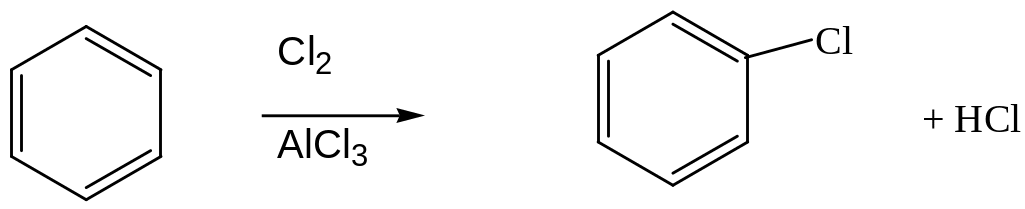
Бензол и его гомологи хлорируются легче, чем алканы, механизм реакции – электрофильное замещение.
Получение галогенопроизводных из спиртов
При взаимодействии спиртов с галогеноводородами применяют водоотнимающие средства (хлорид кальция).
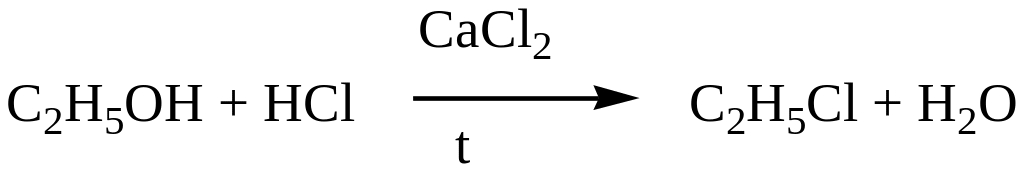
При действии на спирты галогенидов фосфора или серы происходит реакция замещения гидроксильной группы на галоген.
![]()
![]()
Физические свойства
Галогенуглеводороды имеют в своей структуре полярные ковалентные связи, поэтому обладают заметным дипольным моментом. Для этих соединений характерно слабое межмолекулярное взаимодействие, характерны низкие температуры кипения и плавления. Галогенуглеводороды практически нерастворимы в воде, но растворимы в органических растворителях, они растворяют жиры и масла.
Химические свойства
Химические свойства алкилгалогенидов обусловлены разрывом связей С - Галоген.
Наиболее легко реакции замещения протекают для иодпроизводных. Механизм процесса - нуклеофильное замещение (SN).
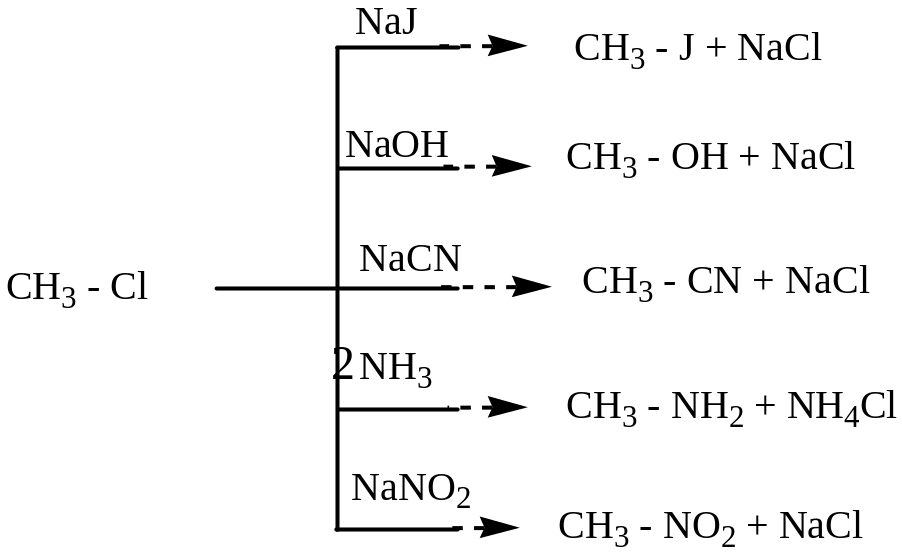
По современным представлениям реакции нуклеофильного замещения могут протекать по двум механизмам: мономолекулярному SN1 и бимолекулярному SN2.
Механизм SN2
Этот механизм характерен для первичных алкилгалогенидов.
![]()
Реакция замещения происходит в результате постепенного вытеснения старой группы новой группой. Образование новой и разрыв старой связи происходит одновременно.

В переходном состоянии центральный атом гибридизован, как в алкенах, все его связи находятся в одной плоскости, а входящая и уходящая группы находятся за и перед плоскостью молекулы. Нуклеофильная атака осуществляется с тыла.
![]()
