
- •Химическая технология неорганических веществ. Основные производства
- •Химическая технология неорганических веществ. Основные производства
- •Предисловие
- •Лекции №1-2 получение синтетического аммиака
- •1. Общие сведения.
- •1.1.Свойства аммиака.
- •1.2. Значение и применение аммиака.
- •2.Физико-химические основы синтеза аммиака.
- •3. Технологическая схема синтеза аммиака при среднем давлении.
- •4. Основные направления развития производства аммиака.
- •Лекции №3-4 химия и технология азотной кислоты.
- •1.Общие сведения.
- •1.1.Физические свойства Диаграммы состояния.
- •1.2. Химические свойства.
- •1.4. Применение азотной кислоты.
- •1.5. Способы получения азотной кислоты.
- •2. Получение неконцентрированной азотной кислоты из аммиака (химические уравнения и стадии).
- •3. Физико-химические основы процесса окисления аммиака.
- •3.1. Химические уравнения процесса окисления аммиака и их анализ.
- •3.2. Выбор оптимальных условий процесса окисления аммиака.
- •3.2.1. Катализаторы процесса окисления аммиака.
- •3.2.2. Скорость окисления аммиака.
- •3.2.3. Определение оптимальной температуры.
- •3.2.4. Определение оптимального давления процесса.
- •3.2.5. Состав газовой смеси.
- •4. Физико-химические основы процесса окисления нитрозных газов (no в no2).
- •5. Физико-химические основы процесса поглощения оксидов азота водой.
- •6. Очистка отходящих газов.
- •Лекция № 5 Получение неконцентрированной азотной кислоты в промышленности.
- •1. Основные операции и принципиальная схема.
- •2. Технологические схемы производства неконцентрированной азотной кислоты.
- •3. Принципиальная технологическая схема получения неконцентрированной азотной кислоты под повышенным давлением
- •Лекция № 6 Получение концентрированной азотной кислоты.
- •1. Общая характеристика методов получения концентрированной азотной кислоты.
- •2. Получение концентрированной азотной кислоты из разбавленных растворов.
- •3. Прямой синтез концентрированной азотной кислоты.
- •3.2. Основные стадии.
- •3.3. Технологическая схема производства концентрированной азотной кислоты прямым синтезом.
- •Лекция № 7 Химическая технология серной кислоты
- •1. Общие сведения.
- •1.1 Значение и применение серной кислоты.
- •1.2 Свойства серной кислоты.
- •1.3 Сырьевые источники.
- •1.4. Промышленные сорта серной кислоты.
- •1.5. Способы получения серной кислоты.
- •2. Производство серной кислоты.
- •2.1. Основные стадии производства серной кислоты.
- •2.2. Получение диоксида серы so2.
- •3. Получение so2 из флотационного колчедана.
- •3.1. Основные стадии получения диоксида серы.
- •3.2. Физико-химические основы процесса обжига флотационного колчедана.
- •3.3. Очистка обжигового газа от пыли.
- •3.4. Специальная тонкая очистка печного газа
- •3.5. Осушка обжигового газа.
- •3.6. Принципиальная схема производства.
- •Лекция №8 Получение диоксида серы из серы.
- •Технологические свойства серы.
- •2. Теоретические основы горения серы.
- •3. Схема установки для сжигания серы в распылённом состоянии.
- •3.6. Схема производства серной кислоты из серы.
- •Лекция № 9 физико-химические основы Контактного окисления диоксида серы
- •Анализ химического уравнения.
- •Выражение для константы равновесия.
- •Кинетическое уравнение.
- •4. Выбор оптимальных условий ведения процесса.
- •4.1. Влияние состава исходной газовой смеси.
- •4.2. Влияние температуры.
- •4.3. Влияние давления.
- •4.4. Катализаторы
- •Лекция №10 абсорбция. Очистка отходящих газов. Производство серной кислоты из сероводорода
- •1. Абсорбция триоксида серы.
- •2. Очистка отходящих газов.
- •3. Производство серной кислоты из сероводорода.
- •4. Основные направления совершенствования сернокислотного производства.
- •Лекция № 11 Электрохимические производства.
- •1. Общие сведения.
- •2. Теоретические основы электролиза.
- •3. Электролиз воды.
- •Лекция №12 Электролиз водного раствора хлорида натрия
- •Общие сведения.
- •2. Электрохимические процессы, протекающие при электролизе водного раствора хлорида натрия.
- •3. Промышленные электрохимические методы получения хлора.
- •4. Электролиз водных растворов хлоридов с применением стального катода.
- •4.1. Приготовление и очистка рассола.
- •4.2. Побочные процессы электролиза.
- •4.4. Технологическая схема производства водорода, хлора и щелочи.
- •4.5. Выпаривание электролитического щёлока.
- •5. Электролиз водного раствора хлорида натрия с ртутным катодом.
- •5.1. Физико-химические основы процесса.
- •5.2. Принципиальная схема электролиза с ртутным катодом.
- •Лекция №13 Производство хлористого водорода и соляной кислоты.
- •1. Свойства и применение хлористого водорода.
- •2. Способы производства хлористого водорода.
- •3. Теоретические основы синтеза хлористого водорода.
- •4. Абсорбция хлороводорода или получение соляной кислоты.
- •5. Схема получения хлороводорода и соляной кислоты.
- •6. Получение жидкого хлороводорода.
- •Лекция № 14 Химическая технология Получения нитрата аммония или аммиачной селитры
- •1. Общие сведения.
- •Физические свойства нитрата аммония.
- •1.2. Химические свойства нитрата аммония.
- •1.3. Технологические свойства.
- •1.4. Применение нитрата аммония.
- •1.5. Характеристика готового продукта.
- •2. Технология производства нитрата аммония.
- •2.1. Физико-химические основы процесса синтеза нитрата аммония.
- •2.2. Технологические схемы производства.
- •3. Техника безопасности в производстве аммиачной селитры.
- •Лекция № 15 Производство карбамида.
- •1. Общие вопросы.
- •1.1. Свойства карбамида.
- •1.2. Применение карбамида.
- •1.3. Сырьё.
- •2. Физико-химические основы процесса синтеза карбамида.
- •2.1. Химические уравнения и их анализ.
- •2.2. Оптимальный технологический режим процесса синтеза карбамида.
- •3. Промышленные схемы производства карбамида.
- •4. Технологическая схема производства карбамида с полным жидкостным рециклом и двухступенчатой дистилляцией плава.
- •5.Стриппинг-процесс.
- •Лекция №16 Производство кальцинированной соды или карбоната натрия.
- •Общие сведения.
- •2. Свойства и нахождение в природе карбоната натрия.
- •3. Получение кальцинированной соды по способу Леблана.
- •4.1. Химические реакции их анализ.
- •4.2. Основные операции (или стадии) производства кальцинированной соды.
- •4.3 Теоретические основы производства кальцинированной соды аммиачным способом.
- •4.4. Принципиальная технологическая схема производства кальцинированной соды по аммиачному способу
- •5. Получение гидрокарбоната натрия
- •Лекция № 17 производство гидроксида натрия или каустической соды химическим способом
- •1. Общие сведения.
- •2. Известковый способ производства гидроксида натрия
- •Химические реакции
- •Физико-химические основы процесса каустификации
- •Основные операции технологического процесса.
- •3.Ферритный способ производства гидроксида натрия.
- •3.1. Сырьё.
- •3.2. Химические реакции.
- •3.3. Основные стадии.
- •3.4. Расходные коэффициенты.
- •3.5. Совершенствование метода.
- •Элементы технологического расчёта реактора.
- •Список рекомендуемой литературы
- •Оглавление
- •650000, Кемерово, ул, Весенняя, 28.
- •650000, Кемерово, ул. Д.Бедного, 4а.
2. Очистка отходящих газов.
После абсорбции газ содержит некоторое количество SO2 (0,23% об.). Так как ПДК выбросов в атмосферу по SO2 составляет 0,05% (об.) и объёмы отходящих газов большие, то необходимо предусмотреть утилизацию отходов.
Методы очистки, как указывалось в первой части курса, зависят от свойств улавливаемого компонента и матрицы.
Вспомним, что диоксид серы растворяется в воде с образованием сернистой кислоты, НО растворяется в воде плохо.
Как кислотный оксид диоксид серы взаимодействует со щелочами и растворами аммиака с образованием соответствующих солей. На этих свойствах может быть основано улавливание диоксида серы из отходящих газов.
В производственной практике широко использовался сульфит-бисульфитный метод, суть которого заключается в следующем.
Диоксид серы поглощается раствором сульфит-бисульфита аммония, которые образуются при пропускании газа, содержащего SO2, через водный раствор аммиака:
SO2 + 2NH3 + H2O = (NH4)2SO3 (cульфит)
(NH4)2SO3 + SO2 + H2O = 2NH4HSO3 (бисульфит).
Из бисульфита (гидросульфита) получают сульфит
2NH4HSO3 + NH3 + H2O = (NH4)2SO3,
который вновь поглощает SO2.
Полученный сульфит-бисульфитный раствор можно утилизировать следующим образом:
cжигать
(NH4)2SO3→2NH3 + SO2 + H2O;
отгружать потребителю;
получать SO2 при взаимодействии с серной кислотой
(NH4)2SO3 + H2SO4 → (NH4)2SO4 + H2O +SO2.
Двойное контактирование (ДК-ДА).
Снизить выбросы диоксида серы более чем в 50 раз позволяет система ДК-ДА. Суть этого приема заключается в том, что после абсорбции газ возвращается на повторное контактирование. Степень окисления SO2 в SO3 на таких установках достигает 99,995%.
3. Производство серной кислоты из сероводорода.
Сущность и особенности метода. Авторы этого метода И.А Ададуров и Д. Гернст, 1931г. Способ состоит в том, что смесь SO2 и H2O в соотношении 1:1, полученная сжиганием сероводорода в токе воздуха, поступает на контактирование без разделения, где SO2 окисляется на твёрдом катализаторе до SO3. затем газовая смесь охлаждается в конденсаторе, где пары образующейся серной кислоты превращаются в жидкость. Этот метод ещё называют «методом мокрого катализа».
Отличие от метода производства серной кислоты из колчедана или из серы заключается в том, что здесь отсутствует специальная стадия абсорбции SO2.
Весь процесс получения серной кислоты включает только три следующие последовательные стадии:
– сжигание сероводорода с образованием смеси SO2 и паров воды эквимолекулярного состава (1:1)
H2S + 1,5O2 = SO2 + H2O ∆H<0
– охлаждение печного газа в котлах-утилизаторах;
– окисление SO2 до SO3 на ванадиевом катализаторе с сохранением эквимолекулярного состава SO3 и Н2О (1:1)
SO2+ 0,5O2 = SO3 ∆H<0
– конденсация паров с образованием серной кислоты
SO3 + H2O = H2SO4 ∆H<0
Таким образом, процесс мокрого катализа описывается суммарным уравнением
H2S + 2O2 = H2SO4 ∆H<0
В качестве сырья используется высококонцентрированный сероводородный газ, содержащий до 90% H2S. Обычно это отходы некоторых производств. Так как при выделении сероводорода из отходов производств газ подвергается промывке, то он уже не нуждается в особой очистке, а продукты его сжигания не содержат вредных для катализатора примесей и также не требуют очистки.
Таким образом, отсутствие стадии абсорбции и стадии очистки существенно упрощают технологическую схему.
На рисунке (Рис.25) представлена схема производства серной кислоты из сероводорода.
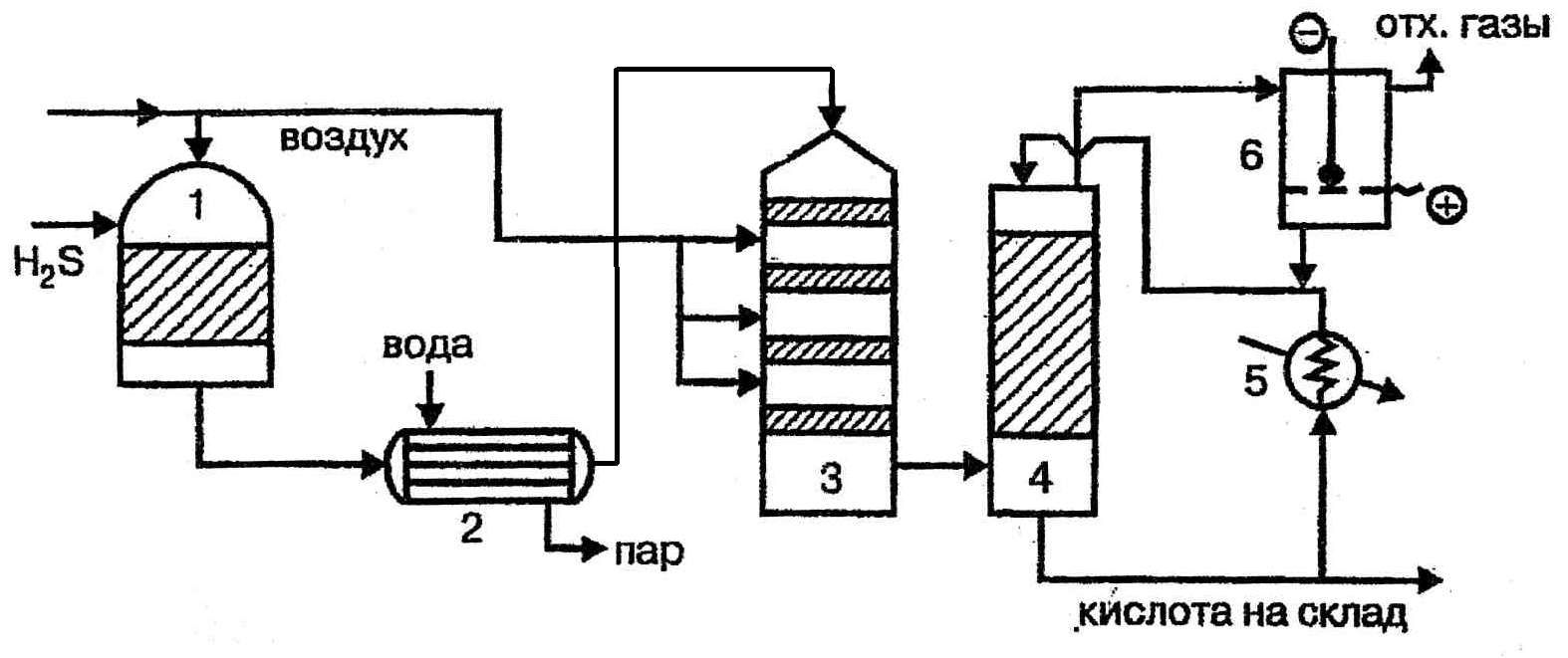
Рис. 25. Технологическая схема производства серной кислоты из сероводорода
1 – печь с огнеупорной насадкой, 2 – котел-утилизатор, 3 – контактный аппарат, 4 – башня-конденсатор, 5 – холодильник, 6 – электрофильтр.
Схема включает следующие операции:
– сжигание сероводородного газа при большом избытке воздуха для исключения перегрева вследствие выделения большого количества тепла
– охлаждение газо-паровой смеси от 1000ºС до 400ºС в котле-утилизаторе
– разбавление газовой смеси воздухом до оптимального состава для контактиравания
– контактирование в контактных аппаратах, термостатируемых введением воздуха между слоями катализатора
– охлаждение конвертированного газа в башнях, орошаемых серной кислотой, с образованием продукционной серной кислоты и сернокислотного тумана, который улавливается в электрофильтрах.
Описание схемы.
Сероводород поступает в печь 1, где смешивается с воздухом. В процессе реакции температура повышается до 1000ºС, поэтому сразу после печи, полученные SO2 и H2O направляются в котёл-утилизатор 2, где температура смеси снижается до 400ºС. Охлаждённая смесь поступает в контактный аппарат 3, где происходит окисление оксида серы(IV) в оксид серы(VI). Полученный конвертированный газ охлаждается в конденсаторе 4 путём орошения охлаждённой в холодильнике 5 серной кислотой. В процессе образуется продукционная кислота и сернокислотный туман, который улавливается на электрофильтре 6.
Теоретически, при абсолютно сухих сероводородном газе и воздухе должна получаться 100%-я серная кислота. На практике, концентрация серной кислоты не превышает 96%, так как присутствует в воздухе влага.
Одновременно побочно получается водяной пар высоких параметров (температура и давление).
Производительность существующих установок, работающих по методу мокрого катализа, достигает 300 т/сут. По моногидрату.
