
- •Министерство образования российской федерации
- •Череповецкий государственный университет
- •Инженерно -технический институт
- •Кафедра химии
- •Лабораторный практикум
- •По дисциплине
- •Часть 2
- •Титриметрический (объёмный) анализ
- •Определение массовой доли h2so4 в технической серной кислоте
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм выполняемой работы
- •Классификация титриметрических методов
- •5. Обработка результатов
- •Массовая доля серной кислоты, %:
- •Экспериментальные и расчетные данные
- •Плотность водных растворов серной кислоты h2so4
- •6. Контрольные вопросы и задания
- •Окисляемость воды
- •Определение окисляемости воды перманганатометрическим методом
- •2. Сущность метода
- •Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Установка титра раствора kMnO4
- •4.2. Анализ природной воды
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •6. Контрольные вопросы и задания
- •Йодометрия
- •Определение содержания аскорбиновой кислоты в фруктовых соках
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •6. Контрольные вопросы
- •Дихроматометрия
- •Определение массовой доли органического углерода в жидких комплексных удобрениях
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Установка титра соли Мора
- •Установка титра
- •4.2. Определение углерода органического
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •5. Контрольные вопросы и задания
- •Определение хлоридов в водопроводной воде
- •Сущность метода
- •Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Установка титра азотнокислой ртути (II)
- •Установка титра
- •4.2. Определение хлоридов
- •5. Обработка экспериментальных данных Содержание хлоридов в исследуемой воде вычисляют по формуле, мг/дм3:
- •6. Контрольные вопросы и задания
- •Определение кальция и магния в водной вытяжке из почвы
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Определение суммарного содержания ионов кальция и магния
- •Экспериментальные и расчетные данные
- •Определение содержания кальция
- •2. Сущность метода
- •Приборы и реактивы
- •4. Алгоритм определения
- •5. Обработка результатов
- •6. Контрольные вопросы
- •Литература
- •Содержание Ведение 3
- •162600, Г. Череповец, Советский пр. 8.
Министерство образования российской федерации
Череповецкий государственный университет
Инженерно -технический институт
Кафедра химии
Лабораторный практикум
По дисциплине
«Т Е Х Н И Ч Е С К И Й А Н А Л И З»
Часть 2
Учебно-методическое пособие
Череповец
2001
Лабораторный практикум по дисциплине «Технический анализ». Ч.2: Учеб.-метод. пособие. Череповец: ЧГУ, 2000. 26 с.
Учебно - методическое пособие содержит 7 лабораторных работ. Каждая работа содержит теоретические сведения, описание экспериментальных установок, порядок выполнения работы, алгоритмы обработки экспериментальных данных, контрольные вопросы.
Рассмотрено на заседании кафедры химии 05.02.2001 г, протокол № 5.
Одобрено редакционно-издательской комиссией Инженерно-технического института ЧГУ 05.02.2001 г., протокол № 5.
Рецензенты: И.В. Повышева – канд хим. наук (ЧГУ);
О.А. Калько – канд техн. наук, доцент (ЧГУ);
Составители: Н.В. Кунина; Ю.С. Кузнецова
Научный редактор: Л.В. Вострикова – доцент (ЧГУ)
© Череповецкий государственный
университет, 2001


Титриметрический (объёмный) анализ
Краткие теоретические сведения
По типу используемых химических реакций методы объемного анализа делят на четыре большие группы (табл. 5). Каждая из этих групп включает несколько различных методов.
Р а б о т а 6
Определение массовой доли h2so4 в технической серной кислоте
1. Цель работы: получить общие сведения о кислотно-основном методе анализа; определить содержание H2SO4 в технической серной кислоте.
2. Сущность метода
 Определение
H2SO4
основано на титровании её растворов
стандартным раствором щелочи (КОН или
NaOH).
В качестве индикатора применяют метиловый
красный.
Определение
H2SO4
основано на титровании её растворов
стандартным раствором щелочи (КОН или
NaOH).
В качестве индикатора применяют метиловый
красный.
Уравнение реакции этого метода:
H2SO4 + 2NaOH 2H2O + Na2SO4
2H+ + 2OH- 2H2O.
3. Приборы и реактивы
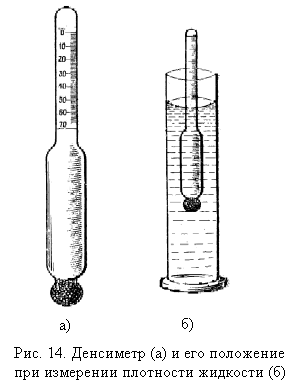
Весы аналитические, набор ареометров;
посуда стеклянная: бюретка
вместимостью 25 см3, пипетка Мора
вместимостью 20 см3, мерная колба
вместимостью 200 см3, мерный цилиндр
вместимостью 200-250 см3, мензурка
вместимостью 50 см3, конические колбы
вместимостью 100 см3, бюксы, воронки
стеклянные; растворы: технической H2SO4,
индикатор-метиловый красный,
стандартный раствор щелочи NaOH.
4. Алгоритм выполняемой работы
1) Определение плотности анализируемой кислоты
Для определения плотности техническую серную кислоту наливают в сухой стеклянный цилиндр объёмом 200-250 см3 (эту операцию проводят в вытяжном шкафу), погружают в него денсиметр (ареометр).
Таблица 5
