
Химия Нефти и Газа. Методичка по органической химии
.pdf
vk.com/club152685050 | vk.com/id446425943
ВВЕДЕНИЕ
Органическая химия изучает соединения, основу которых составляют атомы углерода, связанные между собой и многими элементами периодической системы простыми и кратными связями, способные образовывать линейные и разветвленные цепи, циклы, полициклы и др. В настоящее время известно более 20 миллионов органических соединений, полученных главным образом искусственно, и в живых организмах не встречающихся.
К органическим соединениям относятся химические вещества, содержащие в своем составе углерод, например
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
C |
C |
C |
C |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
за исключением простейших (оксидов углерода, угольной кислоты и ее солей, карбидов).
Разобьем историю развития органической химии на
этапы.
Эмпирический этап.
В 17-18 вв. было получено большое количество органических соединений в индивидуальном виде, таких например, как щавелевая, лимонная, яблочная, муравьиная кислоты, мочевина и т.д.
Аналитический этап - это18 век – середина 19 века. Этот этап ознаменован исследованиями по
установлению состава веществ, в результате которых стало очевидно, что все органические соединения содержат углерод. В этот период были сделаны попытки теоретического осмысления
3
vk.com/club152685050 | vk.com/id446425943
накопленного материала: были созданы две теории – теория радикалов и теория типов. Термин органическая химия впервые введен шведским химиком Й.Я. Берцелиусом в 1808 году, когда еще не были сформулированы названия других разделов химии. Считается, что первый органический синтез провел немецкий химик Ф. Вёллер в 1828 году нагреванием неорганического соединения – изоцианата аммония, при этом образовывалась мочевина:
(NH4)CNO = CO(NH2)2
В дальнейшем были синтезированы и другие органические соединения: жиры, этанол, муравьиная кислота, сахаристые вещества. Появилось целое направление – органический синтез, который стал фундаментом многих отраслей химической промышленности. Многих вершин органический синтез достиг в 20 веке, когда были синтезированы многие сложные органические вещества, такие как витамины, гормоны, хлорофилл, алкалоиды, пептиды, белки и нуклеиновые кислоты.
Структурный этап. 19 век – начало 20 века.
Немецкие химики А. Кекуле и Г. Кольбе установили четырехвалентность углерода и высказали мысль о способности атомов углерода соединяться в длинные цепочки. Русский химик А.М, Бутлеров ввел термин “структура” для обозначения последовательности связей между атомами и сделал вывод о том, что структура определяет химические и физические свойства веществ. Опираясь на свою структурную теорию, Бутлеров дал объяснение явлению изомерии и предсказал существование некоторых из изомеров. Так, опираясь на структурную теорию, он предсказал существование нескольких изомеров бутилового спирта.
4
vk.com/club152685050 | vk.com/id446425943
Здесь же следует упомянуть основателя стереохимии голландского химика Я.Х. Вант-Гоффа, выдвинувшего теорию о пространственном трехмерном строении органических молекул
(1874 г.).
Современный период. Ознаменован развитием синтетической органической химии, внедрением квантовомеханических представлений и физических методов исследования веществ, таких как инфракрасная, электронная, флуоресцентная спектроскопия, спектроскопия ЯМР, рентгеноструктурный анализ. Современная органическая химия тесно связана с другими дисциплинами – с физической, неорганической и координационной химией.
ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕОРИИ ХИМИЧЕСКОГО СТРОЕНИЯ А.М. БУТЛЕРОВА
1.Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения).
2.Химическое строение можно устанавливать химическими методами. (В настоящее время используются также современные физические методы).
3.Свойства веществ зависят от их химического строения.
4.По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства.
5.Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга.
5
vk.com/club152685050 | vk.com/id446425943
Формулы строения
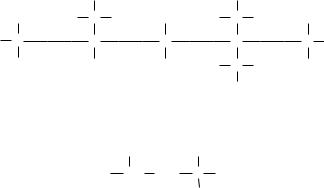
Формула строения (структурная формула) описывает порядок соединения атомов в молекуле, т.е. ее химическое строение. Химические связи в структурной формуле изображают черточками. Связь между водородом и другими атомами обычно не указывается (такие формулы называются сокращенными структурными формулами).
Они показывают не только какие атомы и в каком количестве входят в молекулу данного соединения, но и отражают порядок и характер связей между ними. Различают полную, или развёрнутую, структурную формулу:
|
|
|
H |
|
|
|
H |
|
|
|
|
H |
H |
C |
H |
H |
H |
C |
H |
H |
|
H |
C |
|
C |
|
C |
|
C |
|
C |
H |
|
H |
|
H |
|
H |
H |
C |
H |
H |
|
|
|
|
|
|
|
|
H |
|
|
|
изооктан
и краткую, или звеньевую:
|
CH |
CH |
3 |
|
3 |
|
|
CH |
CH CH |
C |
CH |
3 |
2 |
|
3 |
|
|
CH |
3 |
|
|
|
изооктан
Часто используется еще более краткая запись формулы, когда не изображают не только связи с атомом водорода, но и символы атомов углерода и водорода. Например, строение бензола C6H6.
Структурные формулы отличаются от молекулярных (брутто) формул, которые показывают только, какие элементы и
6
vk.com/club152685050 | vk.com/id446425943
в каком соотношении входят в состав вещества (т.е. качественный и количественный элементный состав), но не отражают порядка связывания атомов. Например, н-бутан и изобутан имеют одну молекулярную формулу C4H10, но разную последовательность связей.
Таким образом, различие веществ обусловлено не только разным качественным и количественным элементным составом, но и разным химическим строением, которое можно отразить лишь структурными формулами.
КЛАССИФИАЦИЯ ОРГАНИЧЕСИХ СОЕДИНЕНИЙ, РЕАГЕНТОВ И ТИПЫ РЕАКЦИЙ.
КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ПО УГЛЕРОДНОМУ СКЕЛЕТУ
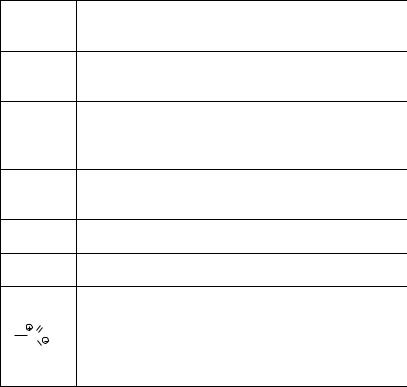
Углеводородами называются органические соединения из углерода и водорода. Их состав выражается общей формулой СхHу. Углеводороды отличаются как углеродным скелетом (циклические, ациклические, гетероциклические), так и характером углерод -углеродных связей (насыщенные, ненасыщенные). Все углеводороды можно классифицировать:
7
vk.com/club152685050 | vk.com/id446425943
|
|
|
|
Углеводороды |
|
|
||
|
|
|
|
ациклические |
|
|
циклические |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(алифатические) |
|
|
|
|
|
|
|
|
непредельные |
|
|
алициклические |
ароматические |
|
|
|
|
|
|
|
|
|
|
|
|
|
(ненасыщенные) |
|
|
|
|
|
алканы |
|
циклоалканы |
циклоалкены |
небензоидные |
|||
|
С H |
|
C H |
|
циклоалкины |
|||
|
|
n |
2n |
|
|
|||
|
n |
2n+2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
арены |
|
|
|
|
|
|
|
|
(бензоидные) |
|
алкены |
|
алкины |
алкадиены |
|
полиненасыщенные |
|
||
C H |
|
С H |
C H |
|
углеводороды |
|
||
|
n 2n-2 |
|
|
|||||
n |
2n |
|
n 2n-2 |
|
|
|
|
|
Схема 1. Классификация углеводородов
КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ПО ФУНКЦИОНАЛЬНЫМ ГРУППАМ
Функциональная группа – это атом, или группа атомов, определяющих характерные свойства определенного класса соединений. Рассмотрим некоторые основные классы органических соединений и функциональные группы, характерные для этих классов. В состав молекул органических соединений могут входить две или более одинаковых или различных функциональных групп.
Например: HO-CH2-CH2-OH (этиленгликоль);
NH2-CH2-COOH (аминокислота глицин).
Все классы органических соединений взаимосвязаны. Переход от одних классов соединений к другим осуществляется
8
vk.com/club152685050 | vk.com/id446425943
в основном за счет превращения функциональных групп без изменения углеродного скелета. Соединения каждого класса составляют гомологический ряд.
Гомологический ряд - ряд родственных органических соединений с однотипной структурой, каждый последующий член которого отличается от предыдущего на постоянную группу атомов (гомологическую разность).
Таблица 1. Наиболее распространённые функциональные группы и классы
органических соединений
Группа
–F, –Cl, – Br, –I
–ОН
–SH
–OR
–N=O
O
N
O
Название |
|
Отдельные |
|
группы |
Название класса |
|
|
представители |
|
||
(в префиксе) |
|
|
|
|
|
|
|
|
|
CH3Cl – хлорметан |
|
Галоген- |
Галогенпроизводные |
С6H5Br |
– |
|
|
бромбензол |
|
|
|
СН3ОН – метанол |
|
Гидрокси- |
Спирты |
С6Н5СН2ОН |
– |
|
бензиловый спирт |
|
|
|
|
|
|
|
|
|
|
|
Фенолы |
С6Н5ОН – фенол |
|
|
|
C2H5SH |
– |
Меркапто- |
Меркаптаны |
этилмеркаптан, |
|
|
|
этантиол |
|
Алкокси- |
Простые эфиры |
(С2Н5)2O |
– |
диэтиловый эфир |
|
||
|
|
|
|
Нитрозо- |
Нитрозосоеди-нения |
C6H5N=O |
– |
нитрозобензол |
|
||
|
|
|
|
|
|
CH3NO2 |
– |
|
|
нитрометан |
|
Нитро- |
Нитро-соединения |
(СH3)2CHNO2 – 2- |
|
нитропропан |
|
||
|
|
|
|
|
|
С6H5NO2 |
– |
|
|
нитробензол |
|
|
|
|
|
9
vk.com/club152685050 | vk.com/id446425943
|
|
Название |
|
Отдельные |
|
|
Группа |
группы |
Название класса |
|
|||
представители |
|
|||||
|
|
(в префиксе) |
|
|
||
|
|
|
|
|
||
|
|
|
|
|
||
H |
|
|
C6H5NH2 – анилин |
|
||
N |
|
Амино- |
Амины |
C4H9NH2 |
– |
|
H |
|
|
бутиламин |
|
||
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
СН3СНО |
– |
|
O |
|
|
ацетальдегид |
|
||
|
|
СН2=СН-СНО |
– |
|||
C |
|
Формил- |
Альдегиды |
|||
|
акролеин |
|
||||
H |
|
|
|
|||
|
|
С6Н5СНО |
– |
|||
|
|
|
|
|||
|
|
|
|
бензальдегид |
|
|
|
|
|
|
|
|
|
C |
O |
Оксо- (кето-) |
Кетоны |
СН3С(О)СН3 |
- |
|
ацетон |
|
|||||
|
|
|
|
|
||
|
|
|
|
|
|
|
O |
|
|
Карбоновые |
НСООН |
– |
|
C |
|
Карбокси- |
муравьиная кислота |
|||
|
кислоты |
|||||
OH |
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|
|
|
|
O |
|
|
СН3СООСН3 |
– |
|
|
Алкокси- |
|
метилацетат |
|
||
C |
|
Сложные эфиры |
|
|||
|
Карбонил- |
С6Н5СООС2Н5 |
- |
|||
|
OR |
|
||||
|
|
|
этилбензоат |
|
||
|
|
|
|
|
||
|
|
|
|
|
|
|
O |
|
|
НС(O)NH2 |
– |
||
|
|
формамид |
|
|||
C |
|
Карбомоил |
Амиды |
|
||
|
CH3C(O)NH2 |
- |
||||
|
|
|||||
NH |
|
|
||||
|
|
|
|
|||
|
2 |
|
|
ацетамид |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
CH3-C≡N |
– |
|
C |
N |
Циано- |
Нитрилы |
ацетонитрил |
|
|
CH2=CH-C≡N |
- |
|||||
|
|
|
|
|||
|
|
|
|
акрилонитрил |
|
|
|
|
|
|
|
||
|
|
|
|
СН2=СН2 – этилен, |
||
–СH=CH2 |
Винил- |
Алкены |
этен |
|
||
Этенил- |
СН3–СН=СН2 |
– |
||||
|
|
|
||||
|
|
|
|
пропилен, пропен |
|
|
|
|
|
|
|
||
–С≡СН |
|
Этинил- |
Алкины |
НС≡СН – ацетилен, |
||
|
этин |
|
||||
|
|
|
|
|
||
|
|
|
|
|
|
|
10
vk.com/club152685050 | vk.com/id446425943
|
Название |
|
Отдельные |
|
Группа |
группы |
Название класса |
||
представители |
||||
|
(в префиксе) |
|
||
|
|
|
||
|
|
|
|
|
|
Фенил- |
Ароматические |
С6Н6 – бензол |
|
|
углеводороды |
С6Н5СН3 - толуол |
||
|
|
|||
|
|
|
|
Примечание: Функциональные группы почти во всех случаях рассматриваются связанными с атомом углерода или водорода.
КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ. ТИПЫ РАЗРЫВА КОВАЛЕНТНОЙ СВЯЗИ
Химические реакции — это процессы, сопровождающиеся изменением распределения электронов внешних оболочек атомов реагирующих веществ. В результате реакции в реагирующих молекулах веществ разрываются одни химические связи и образуются другие. Реакция идет в сторону образования стабильных частиц, т. е. обладающих меньшей внутренней энергией.
Всовременной органической химии реакции классифицируют по их механизмам. Механизм реакции раскрывает последовательность элементарных актов разрыва и образования химических связей, ведущих к превращению исходного вещества в конечный продукт.
Изучить механизм реакции – это значит раскрыть ряд последовательных промежуточных стадий, приводящих к продукту реакции. Знание механизма реакции позволяет ею управлять для получения целевого нужного продукта. В основу классификации реакций по механизмам положен тип разрыва ковалентной связи.
Взависимости от способа разрыва ковалентной связи в реагирующей молекуле (субстрат и реагент). Субстрат — это реагирующее вещество, реагент — действующее вещество.
11

vk.com/club152685050 | vk.com/id446425943
Данное разделение условное. Органические реакции подразделяются на радикальные и ионные реакции. Разрыв ковалентной связи может происходить двумя способами.
Разрыв связи, при котором каждый атом получает по одному электрону из общей пары, называется гомолитическим:
A |
|
A |
|
|
В результате гомолитического разрыва образуются сходные по электронному строению частицы, каждая из которых имеет неспаренный электрон. Такие частицы называются свободными радикалами.
Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется
гетеролитическим:
A |
|
|
|
|
|
A |
|
В результате образуются разноименно заряженные ионы - катион и анион. Если заряд иона сосредоточен на атоме углерода, то катион называют карбкатионом, а анион -
карбанионом.
Различают три типа реагентов:
1) радикалы (R) — это нейтральные атомы или частицы с неспаренным электроном (Н–, С1–.–ОН, —СН3 и др.);
2) нуклеофилы (Nu — «любящие ядра») — это частицы, имеющие электронную пару на внешнем электронном уровне атома (F-, Cl-, Br-, I-, OH-, CH3O-, H2O, спирты, NH3, амины);
3) электрофилы (Е — «любящие электроны») — это частицы, имеющие недостаток электронов — незаполненный валентный электронный уровень (Н+, Br+, NO2+).
12
