- •Биологически активные альдегиды, кетоны и карбоновые кислоты
- •Электронное строение оксогруппы.
- •Химические свойства.
- •Реакции окисления.
- •Реакции полимеризации и конденсации.
- •Карбоновые кислоты
- •Мочевина
- •Лабораторная работа «Свойства альдегидов и кетонов»
- •Тесты для самостоятельной работы студентов Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Литература
Реакции окисления.
Альдегиды легко окисляются в соответствующие карбоновые кислоты. Для их окисления можно использовать сильные окислители, такие как KMnO4, и слабые, такие как аммиачный раствор Ag2O (проба Толленса) и раствор Cu(OH)2 (проба Троммера).
Проба Толленса (реакция серебряного зеркала):

В результате реакции на стенках пробирки образуется серебро в мелкодисперсном состоянии, образуя зеркало, поэтому эта реакция используется как качественная реакция на альдегидную группу.
Проба Троммера (реакция медного зеркала):

В результате реакции, при нагревании образуется оранжевый налет на стенках пробирки оксида меди (I), поэтому эта реакция используется как качественная реакция на альдегидную группу.
Кроме этого качественной реакцией на альдегиды является реакция с фуксинсернистой к-той:
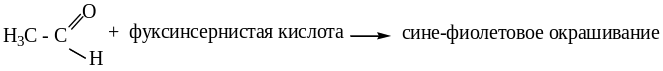
Кетоны окисляются с трудом, только сильными окислителями. При этом образуется смесь карбоновых кислот.

В окислительно – восстановительных реакциях альдегид занимает промежуточное положение, то есть он может восстанавливаться до спирта или окисляться до карбоновой кислоты, следовательно альдегиды обладают окислительно – восстановительной двойственностью и способны вступать в реакции диспропорционирования (реакция Канницарро-Тищенко). Эта реакция характерна для альдегидов, не содержащих атомов водорода в α-положении:
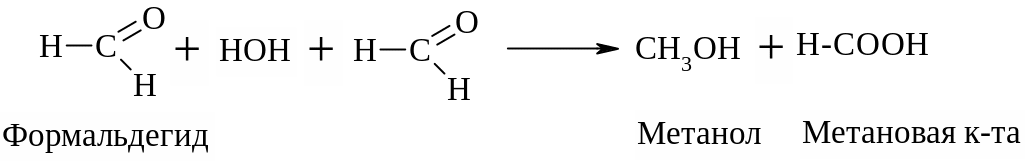
2
Реакции полимеризации и конденсации.
Реакция альдольной конденсации. Благодаря высокой подвижности атомов Н в -положении альдегиды способны вступать в реакцию альдольной конденсации:

 Альдоль
Альдоль
Впервые наблюдали эту реакцию А. Бородин (композитор, врач по образованию, 1872) и Ш. Вюрц.
Механизм реакции:


Часто альдольная конденсация сопровождается отщеплением воды с образованием непредельного альдегида. В этом случае реакция называется кротоновой конденсацией:
 бутен-2-аль
бутен-2-аль
В связи с увеличением подвижности атомов Н в -положении по отношению к карбонильной группе для кетонов характерно также явление кето-енольной таутомерии. Таутомерия – это вид изомерии, происходящей путем перемещения атома Н в молекуле. Образующиеся изомеры находятся в динамическом равновесии и переходят друг в друга за счет внутримолекулярного перемещения атома Н. Этот вид изомерии наз-ся также прототропной:

Обычно процент енольной формы невелик и соответсвует 10-5 – 10-6%. Увеличение цепи сопряжения, введение ЭА заместителей способствует увеличению содержания енольной формы. Так, в ацетилацетоне енольной формы больше, чем в самом ацетоне:

Сопряжения нет! Сопряжение есть!
Замещение Н в енольном гидроксиле на алкилрадикал или ацил- – исключает превращение енола в кето-форму, т.к. не остается подвижного атома водорода. На содержание енола оказывает влияние также температура, природа растворителя и др. факторы.
Реакции с участием углеводородного радикала.
Наличие
в молекуле альдегидов ЭА группы
![]() приводит к повышению реакционной
способности атомов Н в -положении
по отношению к группе
.
Они довольно легко замещаются при
действии некоторых реагентов.
приводит к повышению реакционной
способности атомов Н в -положении
по отношению к группе
.
Они довольно легко замещаются при
действии некоторых реагентов.
Замещение на галоген в алифатических альдегидах:
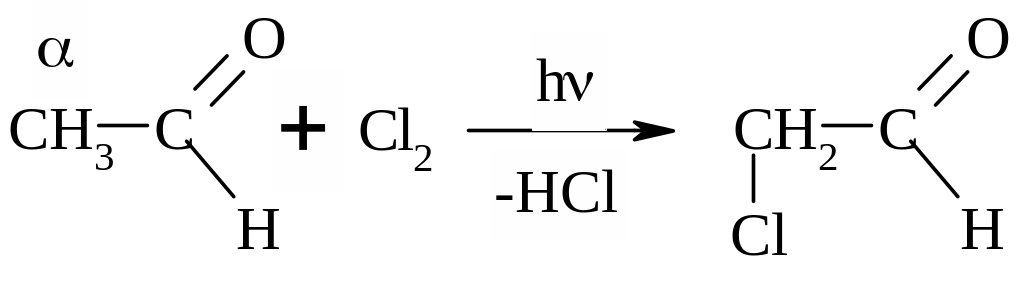
Реакции, характерные для для ароматических радикалов – SЕ.

Реакции, характерные для непредельных альдегидов:

Присоединение НВr происходит против правила Марковникова.
Механизм:
-
1) образование -комплекса

2) образование -комплекса

3) присоединение Вr

(Для увеличения + заряда р-ции часто проводят в слабокислой среде).
Смещение -электронной плотности в группе вызывает, в свою очередь, смещение электронной плотности у соседних С – С связей, что увеличивает подвижность и реакционную способность атомов Н в -положении атома С.
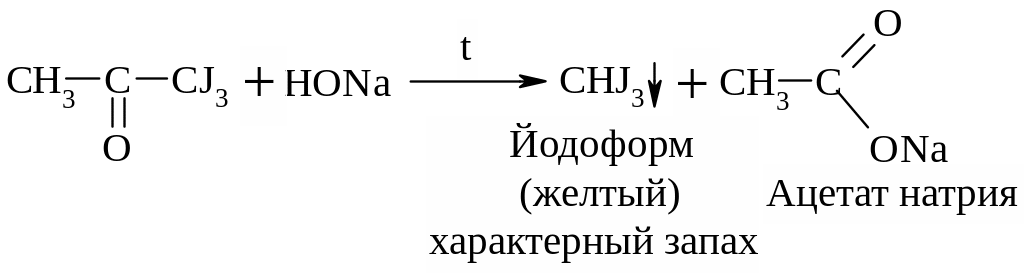
В щелочной среде при действии галогенов (I2, Cl2) альдегиды и кетоны, содержащие R = СН3, образуют йодоформ или хлороформ. Р-ция образования йодоформа используется в клинике для обнаружения ацетона в моче:

Ацетон Трийодацетон