
- •Механическое движение. Относительность движения. Равномерное и равноускоренное движение.
- •Задача на применение законов сохранения массового числа и электрического заряда.
- •Взаимодействие тел. Сила. Законы динамики Ньютона.
- •Лабораторная работа «Измерение показателя преломления стекла».
- •Импульс тела. Закон сохранения импульса. Проявление закона сохранения импульса в природе и его использование в технике.
- •Задача на определение периода и частоты свободных колебаний в колебательном контуре.
- •Закон всемирного тяготения. Сила тяжести. Вес тела. Невесомость.
- •Задача на применение первого закона термодинамики.
- •Превращение энергии при механических колебаниях. Свободные и вынужденные колебания. Резонанс.
- •Лабораторная работа «Расчет и измерение сопротивления двух параллельно соединенных резисторов»
- •Опытное обоснование положений молекулярно-кинетической теории строения вещества. Масса и размеры молекул.
- •Задача на движение или равновесие частицы в электрическом поле.
- •Идеальный газ. Основное уравнение молекулярно-кинетической теории идеального газа Температура и ее измерение. Абсолютная температура.
- •Задача на определение индукции магнитного поля (по закону Ампера или формулы для расчета силы Лоренца).
- •Задача на применение уравнения Эйнштейна для фотоэффекта.
- •Испарение и конденсация. Насыщенные и ненасыщенные пары. Влажность воздуха. Измерение влажности воздуха.
- •Лабораторная работа «Наблюдение дифракции и интерференции света».
- •Кристаллические и аморфные тела. Упругие и пластические деформации твердых тел.
- •Задача на определение показателя преломления прозрачной среды.
- •Внутренняя энергия. Первый закон термодинамики. Применение первого закона термодинамики. Применение первого закона термодинамики к изопроцессам. Адиабатный процесс.
- •Задача на применение закона электромагнитной индукции.
- •Взаимодействие заряженных тел. Закон сохранения электрического заряда.
- •Задача на применение закона сохранения энергии.
- •Конденсаторы. Электроёмкость конденсатора. Применение конденсаторов.
- •Задача на применение уравнения состояния идеального газа.
- •Работа и мощность в цепи постоянного тока. Электродвижущая сила. Закон Ома для полной цепи.
- •Лабораторная работа «Измерение массы тела». Измерение массы тела на рычажных весах
- •Магнитное поле. Действие магнитного поля на электрический заряд и опыты, подтверждающие это действие.
- •Лабораторная работа «Измерение влажности воздуха».
- •Полупроводники. Собственная и примесная проводимость полупроводников. Полупроводниковые приборы.
- •Задача на применение графиков изопроцессов.
- •Электромагнитная индукция. Закон электромагнитной индукции. Правило Ленца.
- •Задача на определение работы газа с помощью графика зависимости давления газа от его объема.
- •Явление самоиндукции. Индуктивность. Электромагнитное поле.
- •Задача на определение модуля Юнга материала, из которого изготовлена проволока.
- •Свободные и вынужденные электромагнитные колебания. Колебательный контур и превращение энергии при электромагнитных колебаниях.
- •Задача на применение закона Джоуля-Ленца.
- •Электромагнитные волны и их свойства. Принципы радиосвязи и примеры их практического использования.
- •Волновые свойства света. Электромагнитная природа света.
- •Задача на применение закона Кулона.
- •Опыты Резердорфа по рассеянию α-частиц. Ядерная модель атома. Квантовые постулаты Бора.
- •Задача на расчет удельного сопротивления материала, из которого изготовлен проводник.
- •Испускание и поглощения света атомами. Спектральный анализ и его применение.
- •Фотоэффект и его законы. Уравнение Эйнштейна для фотоэффекта. Применение фотоэффекта в технике.
- •Задача на применение закона сохранения импульса.
- •Состав ядра атома. Изотопы. Энергия связи ядра атома. Цепная ядерная реакция. Условия ее протекания. Термоядерные реакции.
- •Радиоактивность. Виды радиоактивных излучений и методы их регистрации. Биологическое действие ионизирующих излучений.
- •Лабораторная работа «Оценка массы воздуха в классной комнате при помощи необходимых измерений и расчетов».
Задача на движение или равновесие частицы в электрическом поле.

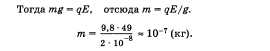 Ответ: масса заряженной
пылинки, находящейся в поле конденсатора,
10^(-7) кг.
Ответ: масса заряженной
пылинки, находящейся в поле конденсатора,
10^(-7) кг.
Билет №7.
Идеальный газ. Основное уравнение молекулярно-кинетической теории идеального газа Температура и ее измерение. Абсолютная температура.
Для объяснения свойств вещества в газообразном состоянии используется модель идеального газа. Идеальным принято считать газ, если: а) между молекулами отсутствуют силы притяжения, т. е. молекулы ведут себя как абсолютно упругие тела; б) газ очень, разрежен, т. е. расстояние между молекулами намного больше размеров самих молекул; в) тепловое равновесие по всему объему достигается мгновенно. Условия, необходимые для того, чтобы реальный газ обрел свойства идеального, осуществляются при соответствующем разрежении реального газа. Некоторые газы даже при комнатной температуре и атмосферном давлении слабо отличаются от идеальных. Основными параметрами идеального газа являются давление, объем и температура.
Одним из первых и важных успехов МКТ было Качественное и количественное объяснение давления газа на стенки сосуда. Качественное объяснение заключается и том, что молекулы газа при столкновениях со стенками сосуда взаимодействуют с ними по законам механики как упругие тела и передают свои импульсы стенкам сосуда.
На основании использования
основных положений молекулярно-кинетической
теории было получено основное уравнение
МКТ идеального газа, которое выглядит
так: ![]() ,
где
,
где ![]() —
давление идеального газа,
—
давление идеального газа, ![]() —
масса молекулы,
—
концентрации молекул,
—
масса молекулы,
—
концентрации молекул, ![]() —
среднее значение квадрата скоростей
молекул. Если представить себе
фантастическую ситуацию, в которой нам
известны скорости всех молекул и единице
объема, то
можно
было бы вычислить по формуле
—
среднее значение квадрата скоростей
молекул. Если представить себе
фантастическую ситуацию, в которой нам
известны скорости всех молекул и единице
объема, то
можно
было бы вычислить по формуле
![]()
Величина
позволяет
ввести представление о сродной
кинетической энергии поступательного
движения молекул идеального газа 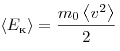 .
Тогда основное уравнение МКТ идеального
газа можно записать в виде:
.
Тогда основное уравнение МКТ идеального
газа можно записать в виде: ![]() .
.
Однако, измерив только
давление газа, невозможно узнать ни
среднее значение кинетической энергии
молекул по отдельности, ни их концентрацию.
Следовательно, для нахождения
микроскопических параметром газа нужно
измерение еще какой-то физической
величины, связанной со средней кинетической
энергией молекул. Такой величиной
является температура. Температура —
скалярная физическая величина, описывающая
состояние термодинамического равновесия
(состояния, при котором не происходит
изменения микроскопических параметров).
Как термодинамическая величина
температура характеризует тепловое
состояние системы и измеряется степенью
его отклонения от принятого за нулевое,
как молекулярно-кинетическая величина
— характеризует интенсивность
хаотического движения молекул, измеряется
их средней кинетической энергией: ![]() где
где ![]() и
называется постоянной
Больцмана.
и
называется постоянной
Больцмана.
Температура всех частей изолированной системы находящейся в равновесии, одинакова. Измеряется температура термометрами в градусах различных температурных шкал. Существует абсолютная термодинамическая шкала (шкала Кельвина) и различные эмпирические шкалы, которые отличаются начальными точками. До введения абсолютной шкалы температур в практике широкое распространение получила шкала Цельсия (за О°С принята точка замерзания воды, за 100°С принята точка кипения воды при нормальном атмосферном давлении).
Единица температуры по абсолютной шкале называется Кельвином и выбрана равной одному градусу по шкале Цельсия 1 К = 1 °С. В шкале Кельвина за нуль принят абсолютный нуль температур, т. е. температура, при которой давление идеального газа при постоянном объеме равно нулю. Вычисления дают результат, что абсолютный нуль температуры равен -273 °С. Таким образом, между абсолютной шкалой температур и шкалой Цельсия существует связь Т = t °С + 273. Абсолютный нуль температуры недостижим, так как любое охлаждение основано на испарении молекул с поверхности, а при приближении к абсолютному нулю скорость поступательного движения молекул настолько замедляется, что испарение практически прекращается. Теоретически при абсолютном нуле скорость поступательного движения молекул равна нулю, т.е. прекращается тепловое движение молекул.
Распространенные ошибки:
1. Не всегда правильно объясняют экзаменуемые различие между идеальными и реальными газами. Были, например, такие ответы: «Идеальный газ — это реальный газ без примесей», «Идеальный газ — это реальный газ при низкой температуре» и т. п.
Слово «идеальный» означает «воображаемый, реально не существующий». Реальный газ отличается от идеального наличием взаимодействия молекул. При малых плотностях в нем преобладают силы притяжения, что приводит к появлению дополнительного давления: газ как бы сжимает сам себя. При больших плотностях действуют силы отталкивания, вследствие чего молекула не допускает проникновения других молекул в занимаемый ею объем. Пренебрегать собственным объемом молекул реального газа нельзя.
При не слишком высоком давлении (например, при атмосферном) и не слишком низкой температуре (например, при комнатной) реальный газ с достаточной степенью точности подчиняется законам идеального газа.
