
Опытные предпосылки квантовой теории света (тепловое излучение, фотоэффект, рассеяние Комптона)
Волна де Бройля.
Принцип неопределенности Гейзенберга, примеры.
Спектры излучения атомов, различные модели строения атомов.
Атом водорода по Бору.
Волновая функция, ее физический смысл и свойства.
Уравнение Шредингера, собственные функции, собственные значения.
Частица в бесконечно глубокой потенциальной яме.
Уравнение Шредингера для атома водорода.
Квантовые числа и их смысл.
Принцип Паули, таблица Менделеева.
Строение ядра.
Энергия связи, дефект масс.
Зависимость энергии связи от атомной массы, деление тяжелых ядер, слияние легких ядер.
Радиоактивность, ее виды.
1)Теплово́еизлуче́ние — электромагнитное излучение с непрерывным спектром, испускаемое нагретыми телами за счёт их тепловой энергии. Примером теплового излучения является свет от лампы накаливания. Мощность теплового излучения объекта, удовлетворяющего критериям абсолютно чёрного тела, описывается законом Стефана — Больцмана. Равновесное излучение — тепловое излучение, находящееся в термодинамическом равновесии с веществом.
Фотоэффе́кт — это испускание электронов вещества под действием света. В конденсированных веществах (твёрдых и жидких) выделяют внешний и внутренний фотоэффект. Внешним фотоэффектом называется испускание электронов веществом под действием электромагнитных излучений. Внутренним фотоэффектом называется перераспределение электронов по энергетическим состояниям в твердых и жидких полупроводниках и диэлектриках, происходящее под действием излучений.
Эффект
Комптона—
явление изменения длины
волныэлектромагнитного
излучения вследствие рассеивания
его электронами.
При рассеянии фотона
на покоящемся электроне
частоты фотона
![]() и
и
![]() (до
и после рассеяния соответственно)
связаны соотношением:
(до
и после рассеяния соответственно)
связаны соотношением:
![]()
где
![]() —
угол рассеяния (угол между направлениями
распространения фотона до и после
рассеяния).
—
угол рассеяния (угол между направлениями
распространения фотона до и после
рассеяния).
2)Во́лны де Бро́йля — волны, связанные с любыми микрочастицами и отражающие их волновую природу.
Для
частиц не очень высокой энергии,
движущихся со скоростью
![]() ,
импульс равен
,
импульс равен
![]() (где
(где
![]() —
масса частицы), и
—
масса частицы), и
![]() .
Следовательно, длина волны де Бройля
тем меньше, чем больше масса частицы и
её скорость. Например, частице с массой
в 1 г, движущейся со скоростью 1 м/с,
соответствует волна де Бройля с
.
Следовательно, длина волны де Бройля
тем меньше, чем больше масса частицы и
её скорость. Например, частице с массой
в 1 г, движущейся со скоростью 1 м/с,
соответствует волна де Бройля с
![]() м
м
3)Принцип неопределённости Гейзенбе́рга в квантовой механике — фундаментальное неравенство (соотношение неопределённостей), устанавливающее предел точности одновременного определения пары характеризующих квантовую систему физических наблюдаемых, описываемых не коммутирующимиоператорами (например, координатыи импульса, тока и напряжения, электрического и магнитного поля). Соотношение неопределенностей задаёт нижний предел для произведения среднеквадратичных отклонений пары квантовых наблюдаемых
4) В нагретом до высокой температуры водороде можно наблюдать характерный линейчатый спектр. Все спектральные линии группируются в серии в зависимости от того, на какой энергетический уровень переходят электроны.
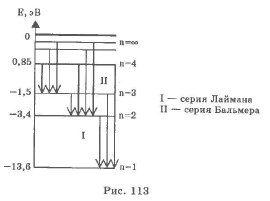
Переходы в первые возбужденные состояния на второй энергетический уровень с верхних уровней образуют серию Бальмера (n = 2), при переходе на первый энергетический уровень с n = 1 образуют серию Лаймана.
Кусочки материи. Демокрит полагал, что свойства того или иного вещества определяются формой, массой, и пр. характеристиками образующих его атомов. Так, скажем, у огня атомы остры, поэтому огонь способен обжигать, у твёрдых тел они шероховаты, поэтому накрепко сцепляются друг с другом, у воды — гладки, поэтому она способна течь. Даже душачеловека, согласно Демокриту, состоит из атомов[2].
Модель атома Томсона (модель «Пудинг с изюмом», англ. Plumpuddingmodel). Дж. Дж. Томсон предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Была окончательно опровергнута Резерфордом после проведённого им знаменитого опыта по рассеиванию альфа-частиц.
Ранняя планетарная модель атома Нагаоки. В 1904 году японский физик ХантароНагаока предложил модель атома, построенную по аналогии с планетой Сатурн. В этой модели вокруг маленького положительного ядра по орбитам вращались электроны, объединённые в кольца. Модель оказалась ошибочной.
Планетарная модель атома Бора-Резерфорда. В 1911 году[3] Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Однако такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а, следовательно, терять энергию. Расчёты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно.
5)Атом водородаявляется атомом химического элемента водорода. Он состоит из положительно заряженного протона, который является ядром водородного атома, и единственного отрицательно заряженного электрона. В общем случае, атом водорода описывается двухчастичной матрицей плотности или двухчастичной волновой функцией. Часто в квантовой механике рассматривается электрон в электростатическом поле атомного ядра. В этом случае, электрон описывается редуцированной одночастичной матрицей плотности или волновой функцией. Из-за своей простоты как проблема двух тел атом водорода имеет специальное значение в квантовой механике и релятивистской квантовой механике поскольку соответствующие уравнения допускают точное или приближенное аналитическое решения.
6) Волновая функция, ее физический смысл и свойства.
Волнова́яфу́нкция,
или пси-функция ![]() —комплекснозначная
функция,
используемая в квантовой
механике для
описания чистого состояния системы.
Является коэффициентом разложения вектора
состояния по
базису (обычно координатному):
—комплекснозначная
функция,
используемая в квантовой
механике для
описания чистого состояния системы.
Является коэффициентом разложения вектора
состояния по
базису (обычно координатному):
![]()
где ![]() —
координатный базисный вектор, а
—
координатный базисный вектор, а ![]() —
волновая функция в координатном
представлении.
—
волновая функция в координатном
представлении.
Физический смысл волновой функции заключается в том, что согласно копенгагенской интерпретации квантовой механикиплотность вероятности нахождения частицы в данной точке пространства в данный момент времени считается равнойквадрату абсолютного значения волновой функции этого состояния в координатном представлении.
В
координатном представлении волновая
функция ![]() зависит
от координат (или обобщённых координат)
системы. Физический смысл приписывается
квадрату её модуля
зависит
от координат (или обобщённых координат)
системы. Физический смысл приписывается
квадрату её модуля ![]() ,
который интерпретируется как
плотность вероятности
,
который интерпретируется как
плотность вероятности ![]() (для
дискретных спектров — просто
вероятность) обнаружить систему в
положении, описываемом координатами
(для
дискретных спектров — просто
вероятность) обнаружить систему в
положении, описываемом координатами ![]() в
момент времени
в
момент времени ![]() :
:
![]() .
.
Тогда
в заданном квантовом состоянии системы,
описываемом волновой функцией
,
можно рассчитать вероятность ![]() того,
что частица будет обнаружена в любой
области пространства конечного
объема
того,
что частица будет обнаружена в любой
области пространства конечного
объема ![]() :
: ![]()
![]() .
.
Следует также отметить, что возможно измерение и разницы фаз волновой функции, например, вопыте Ааронова — Бома.
7) Уравнение Шредингера, собственные функции, собственные значения.
Одномерное стационарное уравнение Шрёдингера — линейное обыкновенноедифференциальное уравнение второго порядка вида
![]()
где ![]() — постоянная
Планка,
—
масса частицы,
— постоянная
Планка,
—
масса частицы, ![]() —
потенциальная энергия,
—
потенциальная энергия, ![]() —
полная энергия,
—
полная энергия, ![]() — волновая
функция. Для полной постановки задачи
о нахождении решения 1надо задать
также граничные
условия, которые представляются в
общем виде для интервала
— волновая
функция. Для полной постановки задачи
о нахождении решения 1надо задать
также граничные
условия, которые представляются в
общем виде для интервала ![]()
![]()
![]()
где ![]() —
константы. Квантовая
механика рассматривает решения
уравнения 1 , с граничными условиями 2 и
3.
—
константы. Квантовая
механика рассматривает решения
уравнения 1 , с граничными условиями 2 и
3.
8) Частица в бесконечно глубокой потенциальной яме.
9) Уравнение Шредингера для атома водорода.
Все члены уравнения Шредингера для атома водорода (и водородопо-
добных атомов, имеющих заряд ядра Z и единственный электрон) мы уже
упоминали. Оператор потенциальной энергии в соответствии с законом Ку-
лона
равен

10) Ква́нтовое число́ в квантовой механике — численное значение какой-либо квантованной переменной элементарной частицы, ядра, атома, характеризующее состояние частицы. Задание квантовых чисел полностью характеризует состояние частицы. Некоторые квантовые числа связаны с движением в пространстве и характеризуют пространственное распределение волновой функции частицы.
11)При́нципПа́ули— один из фундаментальных принципов квантовой механики, согласно которому два и более тождественных фермиона не могут одновременно находиться в одном квантовом состоянии.
Принцип Паули можно сформулировать следующим образом: в пределах одной квантовой системы в данном квантовом состоянии может находиться только одна частица, состояние другой должно отличаться хотя бы одним квантовым числом.
В настоящее время Периодический закон Д. И. Менделеева имеет следующую формулировку: «свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов».
Особенность Периодического закона среди других фундаментальных законов заключается в том, что он не имеет выражения в виде математического уравнения. Графическим (табличным) выражением закона является разработанная Менделеевым Периодическая система элементов.
12)
Атомное ядро состоит из нуклонов —
положительно заряженных протонов
и нейтральных нейтронов,
которые связаны между собой при помощи
сильного
взаимодействия.
Протон и нейтрон обладают собственным
моментом количества движения (спином),
равным
![]() и связанным с ним магнитным
моментом.
и связанным с ним магнитным
моментом.
Атомное ядро, рассматриваемое как класс частиц с определённым числом протонов и нейтронов, принято называть нуклидом.
Количество
протонов в ядре называется его зарядовым
числом![]() —
это число равно порядковому номеру
элемента,
к которому относится атом в таблицеМенделеева.
—
это число равно порядковому номеру
элемента,
к которому относится атом в таблицеМенделеева.
Количество
протонов в ядре определяет структуру
электронной
оболочки
нейтрального атома и, таким образом,
химические
свойства
соответствующего элемента. Количество
нейтронов в ядре называется его
изотопическим
числом![]() .
Ядра с одинаковым числом протонов и
разным числом нейтронов называются
изотопами.
.
Ядра с одинаковым числом протонов и
разным числом нейтронов называются
изотопами.
13) Энергия связи — разность между полной энергией связанного состояния системы тел или частиц и энергией состояния, в котором эти тела или частицы бесконечно удалены друг от друга и находятся в состоянии покоя:
![]()
где
![]() —
энергия связи компонентов в системе из
i компонент (частиц),
—
энергия связи компонентов в системе из
i компонент (частиц),
![]() —
полная энергия i-го компонента в
несвязаннном состоянии (бесконечно
удалённой покоящейся частицы) и
—
полная энергия связанной системы.
—
полная энергия i-го компонента в
несвязаннном состоянии (бесконечно
удалённой покоящейся частицы) и
—
полная энергия связанной системы.
Дефе́ктма́ссы — разность между массой покоя атомного ядра данного изотопа, выраженной в атомных единицах массы, и массовым числом данного изотопа. В современной науке для обозначения этой разницы пользуются термином избыток массы. Как правило, избыток массы выражается в кэВ.
![]()
14)Деление тяжёлых ядер — экзотермический процесс, в результате которого высвобождается большое количество энергии в виде кинетической энергии продуктов реакции, а также излучения. Деление ядер служит источником энергии в ядерных реакторах и ядерном оружии.
Слияние ядер, тип ядерной реакции, при которой ядра легких атомов соединяются и образуют одно или несколько более тяжелых ядер, и этот процесс сопровождается выделением большого количества энергии. Происходит на Солнце и других звездах, воспроизведен на Земле при создании ВОДОРОДНОЙ БОМБЫ.
15) Радиоактивность – самопроизвольное превращение одних атомных ядер в другие, сопровождаемое испусканием элементарных частиц. Такие превращения претерпевают только нестабильные ядра. К числу радиоактивных процессов относятся:
Альфа – распад
Бета – распад (электронный захват)
Гамма – излучение ядер
Спонтанное деление тяжелых ядер
Протонная радиоактивность.
