
- •1. Количество σ связей в молекуле этана
- •2. Оптическая изомерия (d-,l- генетические ряды)
- •3. Реакции полимеризации и поликонденсации.
- •4. Вид гибридизации атомов углерода в молекуле пропена (пропилен) .
- •5. Получение спиртов.
- •6. Пятичленные гетероциклы (пиррол , фуран, тиофен) Обоснуйте их ароматичность
- •7.Количество σ-связей у первого углерода в молекуле пропена.
- •8. Реакция нуклеофильного присоединения у альдегидов, их механизм
- •9. Важнейшие полисахариды (крахмал , целлюлоза )
- •10. Вид гибридизации электронных орбиталей атомов углерода в молекуле бутина-2
5. Получение спиртов.
1. Щелочной гидролиз галогеноуглеводородов:
CH3–Br
+ NaOH (водн.)
![]() CH3–OH
+ NaBr
ClCH2–CH2Cl
+ 2 NaOH (водн.)
HOCH2–CH2OH
+ 2NaCl
C6H5Cl
+ NaOH (p, 340°С)
C6H5OH
+ NaCl
CH3–OH
+ NaBr
ClCH2–CH2Cl
+ 2 NaOH (водн.)
HOCH2–CH2OH
+ 2NaCl
C6H5Cl
+ NaOH (p, 340°С)
C6H5OH
+ NaCl
2. Гидратация алкенов:
CH2=CH2 + H2O (кат.) CH3CH2OH
Присоединение воды к несимметричным алкенам идет по правилу Марковникова с образованием вторичных и третичных спиртов:
CH3–CH=CH2 + H2O (кат.) CH3CH(OH)CH3 (CH3)2C=CH2 + H2O (кат.) (CH3)3C–OH
3. Гликоли получают окислением алкенов щелочным раствором KMnO4:
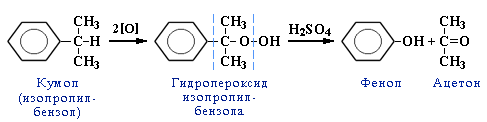
4. Кумольный способ получения фенола (СССР, Сергеев П.Г., Удрис Р.Ю., Кружалов Б.Д., 1949 г.). Преимущества метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время кумольный способ используется как основной в мировом производстве фенола.
6. Пятичленные гетероциклы (пиррол , фуран, тиофен) Обоснуйте их ароматичность
Пиррол, фуран и тиофен являются пятичленными гетероциклическими соединениями с одним гетероатомом.

Нумерация атомов в составе гетероцикла начинается с гетероатома и идет против часовой стрелки. Положения 2- и 5-называют -положениями, 3- и 4- – -положениями.
По формальным признакам эти соединения относятся к ароматическим, так как они представляют собой сопряженные циклические -системы, в состав которых входит 6 электронов – 4 электрона диеновой системы – и пара электронов гетероатома. Цикл является практически плоским, из чего следует, что состояние гибридизации гетероатома близко к sp2.
Характерной особенностью пятичленных гетероциклических соединений является одновременное сочетание у них свойств как ароматического соединения, так и диена. Склонность к реакциям того и другого типов, однако, у них различна и связана с природой гетероатома. Так, “ароматические” свойства убывают в ряду: тиофен > пиррол > фуран. При этом их ароматические системы менее устойчивы, чем у бензола.
7.Количество σ-связей у первого углерода в молекуле пропена.
Пропилен (пропен) СН2=СН-СН3 — непредельный (ненасыщенный) углеводород ряда этилена, горючий газ. Обладает значительной реакционной способностью. Его химические свойства определяются двойной углерод-углеродной связью. π -связь, как наименее прочная и более доступная, при действии реагента разрывается, а освободившиеся валентности углеродных атомов затрачиваются на присоединение атомов, из которых состоит молекула реагента. Все реакции присоединения протекают по двойной связи и состоят в расщеплении π-связи алкена и образовании на месте разрыва двух новых σ-связей. Таким образом при первом углероде (СН2) имеется 3 σ-связи и одна π -связь
8. Реакция нуклеофильного присоединения у альдегидов, их механизм
Альдегидами
называются органические соединения,
содержащие карбонильную группу, в
которой атом углерода связан с радикалом
и одним атомом водорода, то есть общая
формула альдегидов ![]() .
Исключение составляет муравьиный
альдегид
.
Исключение составляет муравьиный
альдегид ![]() ,
в котором, как видно, R=H.
,
в котором, как видно, R=H.
Двойная
связь карбонильной группы по физической
природе сходна с двойной связью между
углеродными атомами, т. е. это сочетание
-
и -
связей, последняя из которых образована
р- электронами атомов углерода и
кислорода. Ввиду большей электроотрицательности
атома кислорода по сравнению с атомом
углерода, связь С=О
сильно поляризована за счет смещения
электронной плотности -
связи к атому кислорода, в результате
чего на атоме кислорода возникает
частичный отрицательный (-),
а на атоме углерода – частичный
положительный (+)
заряды:
![]() .
.
Благодаря поляризации атом углерода карбонильной группы обладает электрофильными свойствами и способен реагировать с нуклеофильными реагентами. Важнейшими реакциями альдегидов являются реакции нуклеофильного присоединения по двойной связи карбонильной группы.
1. Одной из типичных реакций нуклеофильного присоединения альдегидов является присоединение синильной (циановодородной) кислоты, приводящее к образованию - оксинитрилов.
CH3– |
|
+ |
OH I ––KCN CH3–C–CN I H |
|
|
Эта реакция используется для удлинения углеродной цепи и получения - оксикислот.

