
Отношение к молекулярному кислороду
Кислород широко распространен в природе, он входит в состав молекул воды, органических и неорганических соединений, присутствует в современной атмосфере в виде молекулярного кислорода (О2), объемная доля которого составляет 21%.
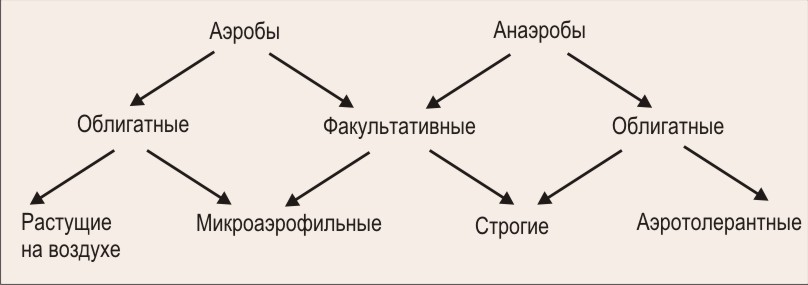
Облигатные аэробы: прокариоты, для роста которых О2 необходим. К ним относится большинство прокариотных организмов.
Микроаэрофилы: не способны к росту при концентрации О2, равной атмосферной, но могут расти, если содержание О2 в окружающей среде будет значительно ниже (порядка 2%). Это некоторые азотфиксаторы (могут расти в среде с молекулярным азотом только при концентрации О2 ниже 2%, т.е. как микроаэрофилы, а в присутствии связанного азота, например аммонийного, - на воздухе. Это объясняется ингибирующим действием молекулярного кислорода на активность нитрогеназы), а также многие водородокисляющие организмы (На среде с органическими соединениями в качестве источника энергии они хорошо растут при атмосферном содержании О2. Если источником энергии является окисление молекулярного водорода, эти же бактерии для роста требуют низкой концентрации О2. Последнее связывают с инактивацией молекулярным кислородом гидрогеназы).
Облигатные анаэробы: прокариоты, для метаболизма которых О2 не нужен. К ним относятся метанобразующие архебактерии , сульфатвосстанавливающие, маслянокислые и некоторые другие эубактерии.
Строгие анаэробы: не выносят присутствия даже незначительных количеств молекулярного кислорода в среде и быстро погибают. К числу строгих анаэробов относятся представители родов Bacteroides , Fusobacterium , Butyrivibrio , Methanobacterium и др.
Аэротолерантные: обладающие метаболизмом только анаэробного типа, но могут расти в присутствии воздуха. Это молочнокислые бактерии рода Lactobacillus , виды маслянокислых бактерий, умеренно ( Clostridium tetani , Сlostridium carnis , Сlostridium tertium , Сlostridium sporogenes ) или достаточно высоко ( Сlostridium perfringens , Сlostridium acetobutylicum ) толерантные к О2.
Факультативные анаэробы или факультативные аэробы: в зависимости от наличия или отсутствия О2 в среде способны переключаться с одного метаболического пути на другой, например с дыхания на брожение, и наоборот. Это дрожжи, энтеробактерии.
Потребность в О2 у аэробов определяется его участием в энергетических и конструктивных процессах. В первом случае О2 служит обязательным конечным акцептором электронов, во втором - участвует в реакциях.
Кислород оказывает также токсическое воздействие на микроорганизмы, окисляя ферменты и метаболиты, приводя к их инактивации. Особо чувствительны нитрогеназа, гидрогеназа и рибулозодифосфаткарбоксилаза.
Токсичные формы кислорода и механизмы защиты от них:
Супероксидный анион: возникает в результате ступенчатого восстановления молекулярного кислорода
O2 + e– ® O2–.
Супероксидные анионы генерируются при взаимодействии с молекулами O2 различных компонентов (восстановленные флавины, хиноны, тиолы, FeS-белки), в процессе фотосинтеза. O2–. могут участвовать в реакциях, приводящих к различным повреждениям: перекисном окислении ненасыщенных жирных кислот, окислении SH-групп белков, повреждении ДНК и др. Многие прокариоты имеют защиту в виде фермента супероксиддисмутазы, осуществляющего перехват ионов O2– .
O2–. + O2–. + 2H+ ® H2O2 + O2.
У некоторых молочнокислых бактерий функцию нейтрализации O2 выполняют ионы Mn2+.
2) Гидроксидный радикал: возникает при взаимодействии супероксиданиона с H2O2 . Превосходит O2–. по окислительной активности и токсичности: O2–. + H2O2 + H+ ® O2 + H2O + OH.. Источником возникновения ОН. могут служить реакции одноэлектронного окисления перекиси водорода, радиолиз воды.
3) Перекись водорода: возникает в результате переноса 2 электронов на O2: O2 + 2H+ + 2e– ® H2O2. Источником H2O2 могут быть реакции автоокисления некоторых негемовых FeS-белков, а также реакции дисмутации супероксидных радикалов. У большинства аэробных прокариот H2O2 быстро разлагается с помощью гемсодержащих ферментов каталазы и пероксидазы. H2O2 вызывает окисление SH-групп в белках, перекисное окисление ненасыщенных жирных кислот.
4) Синглетный кислород – возбуждённое состояние молекулярного кислорода. У большинства источником синглетного кислорода служит дисмутация супероксидных анионов. Синглетный кислород может возникать также при взаимодействии двух радикалов: O2–. + OH. ® OH– + *O2. На свету токсичность молекулярного кислорода повышается. Этому способствуют вещества, поглощающие видимый свет, — фотосенсибилизаторы (хлорофиллы и фикобилипротеины). Окисление биологически важных молекул под влиянием видимого света в присутствии молекулярного кислорода и фотосенсибилизатора получило название фотодинамического эффекта. У прокариот в результате фотодинамического действия индуцируются повреждения многих типов: утрата способности формировать колонии, повреждение ДНК, белков, клеточной мембраны. Причина повреждений — фотоокисление некоторых аминокислот, нуклеозидов, липидов, полисахаридов и других клеточных компонентов. "Тушители" синглетного кислорода - каротиноиды, липиды, аминокислоты, нуклеотиды, токоферолы и др.
5) Озон и атомарный кислород. Молекулярный кислород сильно поглощает свет. Поглощенный фотон вызывает диссоциацию молекулы кислорода на два атома: O2 +hn ® 2O. Затем спонтанно протекает реакция, приводящая к образованию молекулы озона: O2 + O ® O3 Как окислители озон и атомарный кислород сильнее O2. Озон может реагировать практически со всеми типами соединений с образованием радикалов.
