
- •1.3.2. Принципы лечения детей
- •1.3.3. Методики хирургических операций при доброкачественных и злокачественных новообразованиях костей лица
- •1.3.4. Лучевая терапия
- •2.3.1. Опухоли, исходящие из многослойного плоского эпителия
- •2.3.2.2. Злокачественные опухоли
- •3. Фиброматоз десен.
- •2.5.1.2. Фиброангиома основания черепа
- •2.5.2. Опухоли жировой ткани
- •2.5.3. Опухоли мышечной ткани
- •8. Кавернозная гемангиома глубоких отделов околоушно-жевательной области у больного 4 мес.
- •2.5.7.1. Нейрофиброма
- •2.5.7.3. Нейрофиброматоз
- •2.5.7.4. Злокачественные опухоли периферических нервов
- •21. Расположение дермоидной кисты дна полости рта (схема):
- •22. Врожденная боковая киста шеи.
- •2.5.8.3. Фиброзная гамартома младенцев
- •2.6. Опухоли кожи лица
- •3.1. Классификация опухолей костей
- •3.2. Общая клиническая характеристика
- •3.2.2. Рентгенологическое исследование и его задачи
- •3.2.3. Методики получения материала для морфологического исследования
- •29. Остеоид-остеома. Среди одк-оядерных клеток типа остеобластов, окружающих остеоидное вещество, встречаются многоядерные клетки. Окраска гема-токсилин-эозином. Х20.
- •3.3.3. Гигантоклеточная опухоль (остеобластокластома)
- •39. Остеобластокластома — ячеистая форма. Препарат резецированной челюсти.
- •3.3.6.1.2. Десмопластическая фиброма
- •17.09.74 Г. Операция: резекция нижней челюсти с экзартикуляцией и одномоментной костной пластикой аллотрансплантатом. Последний осмотр в 1982 г. Признаков рецидива опухоли нет.
- •53. Миксома правой половины нижней челюсти. Рентгенограмма в прямой проекции.
- •3.3.7.1. Амелобластома
- •3.3.7.2. Одонтома '
- •3.3.7.4. Меланотическая нейроэктодермальная опухоль младенцев
- •3.3.7.6.1. Аневризмальная костная киста
- •3.3.7.7. Эпителиальные кисты
- •3.3.7.8. Воспалительные корневые кисты, исходящие из молочных зубов
- •11 Случаев.
- •63". Фиброзная дисплазия верхней челюсти у больного в., 8 лет.
- •65. Синдром Олбрайта.
- •4.2. Костная пластика нижней челюсти как метод реабилитации детей после удаления костных новообразований
- •4.2.2. Диспансеризация и реабил„тация детей
- •1988, —Vol. 15, n 5. —p. 312—315. Shigera V., Кого m., Rikiga s/1.//j of Orol Maxilofac Surg. — 1989.— Vol. 47,
4.2. Костная пластика нижней челюсти как метод реабилитации детей после удаления костных новообразований
После успешного удаления костного новообразования челюстных костей ребенка нельзя считать здоровым, так как удаление любого костного новообразования связано с образованием дефекта растущей кости. Успешно леченного ребенка с онкологическим заболеванием переводят в другую группу больных,— детей с дефектами челюстных костей, которым необходимо длительное комплексное лечение.
В этом разделе обобщен наш многолетний опыт использования костнопластического материала при восстановительных операциях нижней челюсти после удаления опухолей и опухо-леподобных образований у детей.
Детский хирург-стоматолог и ортодонт используют большой арсенал средств для восстановления формы и функции поврежденных отделов челюстно-лицевой области после удаления новообразований. В активе хирургии и ортодонтии пластический метод: реплантация, аутотрансплантация и аллотранспланта-ция костной ткани, использование костно-пластмассовых эндо-протезов, неагрессивных металлов и протезов сложных конструкций из полимеров. Все это можно объединить в емкое понятие «реконструктивная хирургия челюстно-лицевой области».
Показаниями к костной пластике нижней челюсти у ребенка являются послеоперационные дефекты с нарушением непрерывности кости.
При наличии костного дефекта в процессе роста лицевого скелета оставшаяся часть нижней челюсти как бы распрямляется под действием жевательных мышц и теряет свойственный ей изгиб в подбородочном отделе. Кроме того, вторично деформируется верхняя челюсть за счет развития зубоальвео-лярного удлинения в месте, противоположном дефекту нижней челюсти. Альвеолярный отросток растет вниз до соприкоснове-
267
![]()
70.
(продолжение)
70.
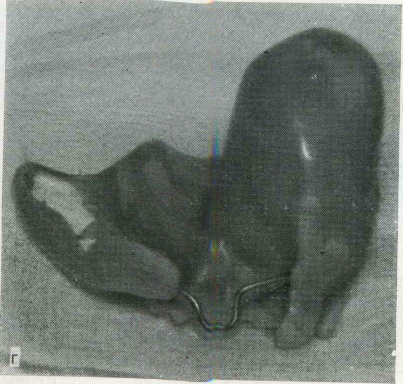
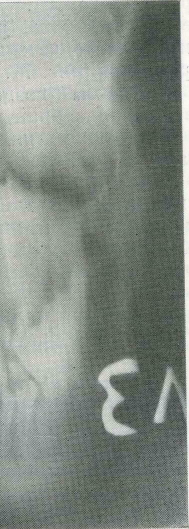
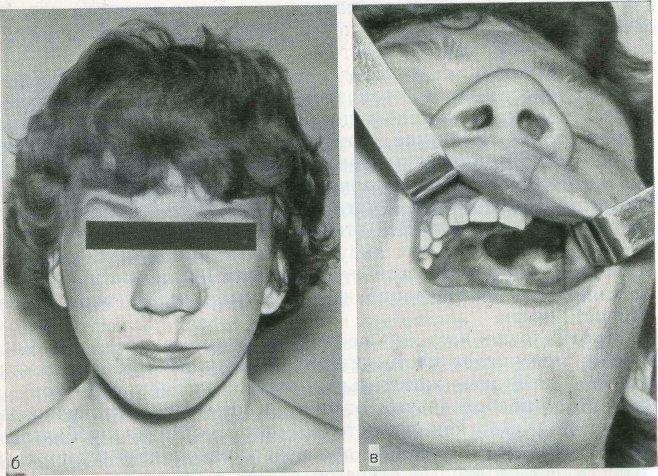
Реабилитация больного с гигантоклеточной опухолью после резекции верхней челюсти.
а — томограмма костей лица больного К., 13 лет, до операции; б — больной после резекции: в — послеоперационный дефект.
г — съемный полый пластмассовый Функциональный аппарат восполняющий дефект кости и зубного ряда.
н
ния с мягкими тканями дна рта. Если реконструктивное вмешательство не проводится в течение несколнышх лет, то на стороне дефекта нижней челюсти меняет свойе положение и деформируется скуловая кость.
Помимо костных деформаций лицевого оскелета, развиваются стойкая дисфункция жевательных и мимических мышц, атрофия мягких тканей лица и шеи в областей рубца, устранить которые после отсроченной костной пластинки оказывается невозможным. Нарушаются функции жеваЫ'ия и артикуляция звуков речи. Изменение внешнего облика Дребенка вырабатывает у него чувство собственной неполноценнности, что приводит к патологической реакции поведения в деэтском коллективе. Эти обстоятельства способствуют расширению показаний и реконструктивным операциям на нижней 'челюсти в детском возрасте. Наш опыт подтверждает, что костгная пластика нижней челюсти должна быть проведена ребеШку независимо от возраста.
С 1954 по 1963 г. в клинике кафедры хирургической стоматологии ММСИ детям проведено 5 восстанОовительных операций аутотрансплантатом (ребром во всю птолщу или гребнем подвздошной кости). Основной причиной маалого числа таких операций было несогласие родителей на дополнительную тяжелую операцию, проводившуюся под местНной анестезией, поскольку в то время в практике хирургичесиких стоматологических клиник (даже ведущих) общее обезбо-оливание не применялось, а также не было опыта использования и возможностей получения консервированной аллокости.
После организации кафедры детской стооматологии с 1964 по 1986 г., т. е. в течение 22 лет, по поводу заболеваний и повреждений нижней челюсти нами произведеено детям 186 ал-•лопластических операций с применением кхостных аллотранс-
269

![]()
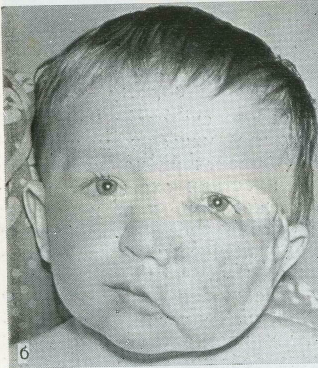
а — больной В., 1 год 1 мес, в процессе лечения; б — через год после лечения гемангиомы.
![]()
плантатов, из них 86 после-удалении опухолей и опухо-леподобных образований нижней челюсти. Ауто-трансплантация кости не проводилась.
Хорошим заменителем, аутокости оказалась консер вированная аллокость, кото рая неограниченно расширя ет возможности костно-пла- стических восстановитель ных операций. Клинически и экспериментально установ лено, что пересаженная ал локость всегда рассасывает ся, замещаясь новой кост ной тканью. Интенсивность процесса зависит от свойств пересаживаемой ткани,, условий, в которые она по падает, и общей реакции ор ганизма на аллотрансплан- тацию. Активная перестрой ка костной ткани при явном преобладании процессов ко- стеобразования над резорб цией обеспечивает успешный исход при использовании аллотрансплантатов для костной пластики у детей [Волков М. В., Бизер В. А., 1969]. В детском возрасте аллотрансплантаты перестраиваются медленнее, чем аутотрансплантаты, и не рассасываются до появления новооб разованной кости (регенерат).
Об использовании аллокости в детской стоматологической клинике сообщается в ряде работ отечественных авторов [Плотников Н. А., Колесов А. А., 1964; Колесов А. А. и др., 1968; Колесов А. А. и др., 1975; Сысолятин П. Г, 1976; Плотников Н. А., 1979; Соловьев М. М. и др., 1979].
Относительно сроков проведения костной пластики нет единого мнения. В нашей клинике пластику называют первичной или одномоментной, если ее проводят сразу после удаления опухоли, отсроченной — через 1 год и более после удаления опухоли, вторичной, или повторной, — после первичной или от-
270
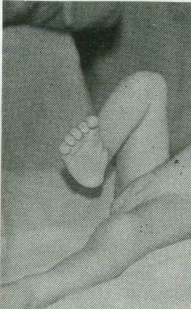
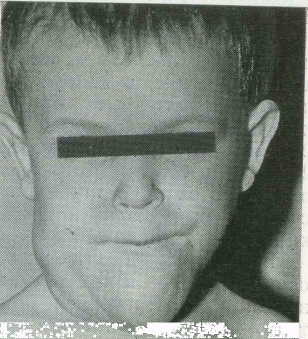
72. Реабилитация больного Д. с лим-фангиомой языка, дна полости рта и шеи.
а — до операции; б — через 6 лет в процессе хирургического и ортодонтического лечения.
сроченной операции, которая была безуспешной вследствие отторжения или рассасывания ранее пересаженного трансплантата.
Первичная, или од номоментная, костная пластика нижней челюсти имеет преимущества перед от сроченной, ибо при ней ребе нок избавлен от дополнитель- i ной травмы — повторной one- -Ш: ] рации.
Воспринимающее ложе трансплантата имеет достаточное количество хорошо васкуляризованных мягких тканей, способствующих приживлению и перестройке аллотрансплантата. Создаются благоприятные условия для раннего протезирования, а следовательно, и функциональной нагрузки. Все это сокращает сроки перестройки трансплантата и лечения больного. Первичная костная пластика в детском возрасте показана после резекции нижней челюсти по поводу доброкачественных опухолей и опухолеподобных образований, т. е. в тех случаях, когда отсутствует опасность рецидива опухоли и имеется достаточно мягких тканей и слизистой оболочки рта для свободного (без натяжения) укрытия трансплантата. При недостатке мягких тканей и особенно слизистой оболочки рта лучше выполнить отсроченную костную пластику.
271
При значительном дефиците мягких тканей после удаления обширных доброкачественных или злокачественных опухолей для создания ложа трансплантата приходится использовать филатовский стебель.
Отсроченная костная пластика проводится после удаления обширных доброкачественных новообразований, иссечение которых связано с образованием дефицита слизистой оболочки рта, и злокачественных опухолей. В отдельных случаях отсроченная костная пластика проводилась детям, направленным в клинику из других лечебных учреждений, где была произведена резекция нижней челюсти без замещения дефекта кости трансплантатом.
При отсроченной костной пластике биологические условия для приживления трансплантата менее благоприятны. Трансплантат помещают в рубцовый массив между склерозирован-ными концами фрагментов челюсти. Если при одномоментной пластике неизбежно возникает сообщение ложа трансплантата с полостью рта, то при отсроченной такое сообщение крайне нежелательно.
Оптимальные сроки для отсроченной костной пластики следующие: 1) после удаления доброкачественных опухолей — через 3—4 мес, в период наиболее активных репаративных процессов, когда еще нет грубых Рубцовых изменений в мягких тканях и склерозирования концевых фрагментов челюсти; 2) после удаления злокачественных опухолей — не ранее 1,5— 2 лет (в отсутствие рецидива и метастазов). При необходимости подготовки воспринимающего ложа для трансплантата за счет местных тканей или филатовского стебля указанные сроки следует увеличить.
Вторичная (повторная) костная пластика
•осуществляется в тех случаях, когда ранее произведена первичная или отсроченная костная пластика, закончившаяся отторжением трансплантата или его рассасыванием. После отторжения трансплантата пластика показана через 6—8 мес, когда снижается иммунологическая активность, вызванная
•трансплантацией аллокости. При вторичном (повторном) замещении дефектов нижнечелюстной кости у детей создаются
•особенно тяжелые условия, существенно влияющие на исход
•операции.
При первичной, отсроченной и вторичной костной пластике дефектов нижней челюсти у детей аллотрансплантат выполняет следующие функции: 1) анатомическую — восстанавливает непрерывность нижней челюсти и ее форму, что улучшает
•функцию жевательного аппарата и эстетический вид больного; 2) механическую — удерживает костные фрагменты в правильном анатомо-физиологическом взаимоотношении, предупреждая деформацию прикуса и костей всего лицевого скелета; 3) биологическую — стимулирует остеопластические процессы, способствуя более быстрой консолидации его с воспри-
272
нимающим ложем, а также образованию регенерата в области дефекта.
В период с 1964 по 1986 г. костная пластика дефектов нижней челюсти после удаления доброкачественных опухолей и опухолеподобных процессов произведена у 81 ребенка, злокачественных— у 5 детей: по поводу фиброзной дисплазии — у 13, гигантоклеточной опухоли — у 30, фибром — у 21, амело-бластомы (адамантиномы)—у 3, миксомы — у 2, обширных костных кист — у 4, ангиофибромы — у одного, костной формы гемангиомы — у 4, гемангиоэндотелиомы — у 4, саркомы — у 5 детей.
По возрасту больные распределялись следующим образом: от 1 года до 4 лет—11, от 4 до 7 лет — 9, от 7 до 12 лет — 39, от 12 до 15 лет — 27 детей. Большинство больных были в возрасте 7—12 и 12—15 лет, что совпадает с наиболее высокой частотой костных опухолей в детском возрасте.
Первичная костная пластика произведена 68 детям, отсроченная— 18, вторичная — 9 (из них у одного 3 раза, у одного— дважды). Всего выполнено 98 трансплантаций.
В качестве пластического материала использовали 29 лио-филизированных трансплантатов, полученных в лаборатории консервации тканей МОНИКИ, 51 трансплантат, консервированный методом глубокого замораживания, заготовленный нами и полученный в лаборатории консервации тканей ЦИТО, 27 трансплантатов, консервированных другими методами (в слабых растворах формалина и полиэфирных смолах), один костно-пластмассовый эндопротез (рис. 73). При замещении дефектов нижней челюсти использовано 37 ортотопических трансплататов, 58 — кортикальной кости, 2 — гребня подвздошной кости и один костно-пластмассовый эндопротез.
4.2.1. Особенности костной пластики у детей
В реконструктивной хирургии челюстно-лицевой области у •детей особое значение имеют выбор вида пластического материала, размеры трансплантируемой ткани, расположение алло-|трансплантата в костной ране, способы его фиксации, иммобилизация челюстных костей, а также реабилитация при диспансерном наблюдении в возрасте до 15 лет.
I Анализ отдаленных результатов лечения 186 детей на про-ггяжении 22 лет, которым реконструктивные операции на нижней челюсти с применением аллотрансплантатов были выполнены по поводу различных патологических процессов, позволяет выделить некоторые особенности костной пластики в детском возрасте.
Как известно, наилучшие условия для формирования репа- эативного регенерата создаются при аллотрансплантации ко- Ьтной ткани одинакового анатомического строения с костью реципиента [Надеин А. П., 1969; Плотников! Н. А., 1979]. В этом Г18—901 273
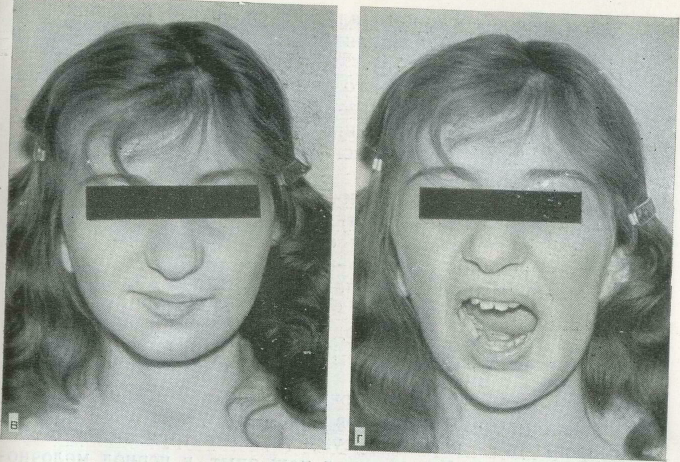
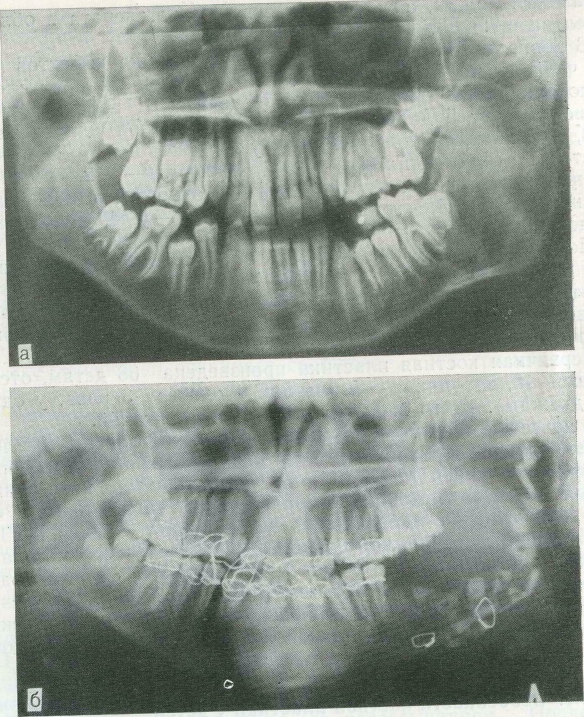
73. Реабилитация больной после резекции нижней челюсти по поводу осси-фицирующей фибромы левой ветви с одномоментным замещением дефекта костно-пластмассовым эндопротезом.
а — ортопантомограмма больной К-, 12 лет, до операции; б— через 30 дней после операции; в, г — больная через 3 года после операции.
плане костные ортотопические трансплантаты более приемлемы для замещения дефектов нижней челюсти. Однако значительные различия в детском возрасте таких параметров нижней челюсти, как мыщелковый отросток, ветвь и угол челюсти, не позволяют использовать этот вид трансплантата у детей младшего возраста. Необходимость уменьшать размеры такого трансплантата приводит к обнажению губчатого вещества, нарушению его архитектоники, следствием чего является активная резорбция аллотрансплантата, часто без построения полноценного репаративного регенерата.
Анализ нашего клинического материала показал, что ортотопические аллотрансплантаты целесообразно использовать
274
при костной пластике обширных дефектов нижней челюсти у детей старше 7 лет, а при пластике подбородочного отдела — в любом возрасте. При дефектах любой другой локализации, независимо от возраста ребенка, могут быть успешно применены не только ортотопические, но и кортикальные трансплантаты, смоделированные по форме замещаемого дефекта.
Экспериментальное обоснование достоинств неортотопиче-ских аллотрансплантатов, которые приобретают анатомическое строение, характерное для костной ткани реципиента, дано А. П. Надеиным (1969).
Аллотрансплантаты губчатого строения для замещения дефектов нижней челюсти в детском возрасте применять нецелесообразно, так как они быстро резорбируют без построения регенерата.
Вторая важная особенность костной пластики у детей — размер аллотрансплантата. В связи с возрастными изменениями строения челюстных костей и окружающих тканей, их непрерывным и неравномерным ростом, сопровождающимся интенсивной дифференцировкой тканей, размер используемого аллотрансплантата должен значительно превышать размеры дефекта. Это необходимо для создания гиперкоррекции размеров нижней челюсти в области восстанавливаемого участка, благодаря которой в последующие периоды роста ребенка обеспечивается равномерное развитие здоровой ее половины и постепенное выравнивание оперированной. Чем в более раннем возрасте ребенку производится костная пластика нижней челюсти, тем больших размеров должен быть аллотрансплантатг У всех оперированных нами больных костная пластика произ-'
ЛОЛ
18
275
I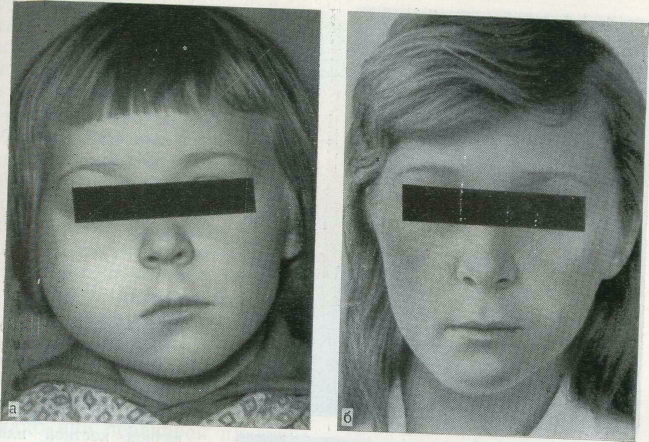
Особенности анатомического строения нижнечелюстной ко--сти (тонкий и мало минерализованный слой кости, наличие в "теле челюсти зачатков постоянных зубов) предопределяют единственно возможный способ расположения трансплантата в костной ране — «внакладку».
Из-за малых размеров челюсти ребенка площадь воспринимающего ложа на концах костных фрагментов редко составляет 1x1 см. Чаще приходится формировать воспринимающее ложе более экономно.
Способы фиксации трансплантата в ране в детском возрасте также имеют особенности. Фиксация трансплантата в костной ране производится чаще одинарным, реже двойным швом кости, проволочной лигатурой марки 1Х18Т9Ю, диаметр которой не более 0,6 мм.
Особенности строения молочного и сменного прикуса (тре-мы и диастемы, наличие зубов с резорбирующимися или несформированными корнями) существенно затрудняют иммобилизацию челюстей. Как показал наш опыт, в период молочного и сменного прикуса прочную иммобилизацию костных фрагментов челюсти обеспечивают назубные капповые аппараты из рластмассы с зацепными петлями. Для иммобилизации челюстей после 98 костных пластик по поводу опухолей использовались назубные шины: каппы с зацепными петлями — у 71, аппарат Рудько —у 9, проволочные шины с зацепными петлями— у 8, шина типа Ванкевич в сочетании с пращевидной повязкой— у 10 детей.
Накостные аппараты у детей практически неприменимы, поскольку травмируют зоны роста кости и зачатки зубов. Кроме того, постоянное давление крючков накостных аппаратов на мало минерализованную костную ткань приводит к появлению вокруг них очагов деструкции, в результате чего возникает патологическая подвижность фрагментов челюсти и аллотран-
еплантата.
Ортодонтическое лечение после костной пластики необходимо проводить до окончания роста костей лицевого скелета. Это возможно только при диспансерном наблюдении хирурга и ортодонта за ребенком до достижения им 15 лет. При необходимости лечение продолжают и в более старшем возрасте.
Предоперационная подготовка ребенка к костной пластике— один из факторов, определяющих исход лечения. Наиболее подробное описание предоперационной подготовки к рекон-структивно-восстановительной операции опорно-двигательного аппарата ребенка приводят М. Д. Дмитриев и соавт. (1974).
Специфика челюстно-лицевой области в возрастном аспекте, особенности местных изменений при свежих и старых дефектах нижней челюсти потребовали разработки системы об-
276
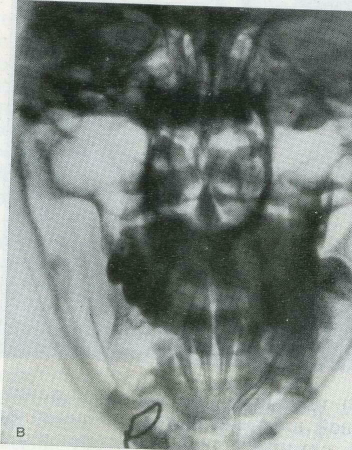
74.
Реабилитация больной после резекции по поводу фиброзной дисплазии нижней челюсти и первичной костной пластики аналогичным ал-лотрансплантатом. а — больная М., 5 лет, до операции; б-через 23 года после операции (лечилась у ортодонта, протезирована); в — рентге нограмма тон же больной через 4А года после операции.
щих и специальных мероприятий, которые мы считаем необходимыми при подготовке ребенка к первичной, отсроченной и вторичной костной пластике нижней челюсти.
Общая подготовка ребенка предусматривает:
1) тщательный анализ анамнеза, определение давности перенесенных заболеваний;
277
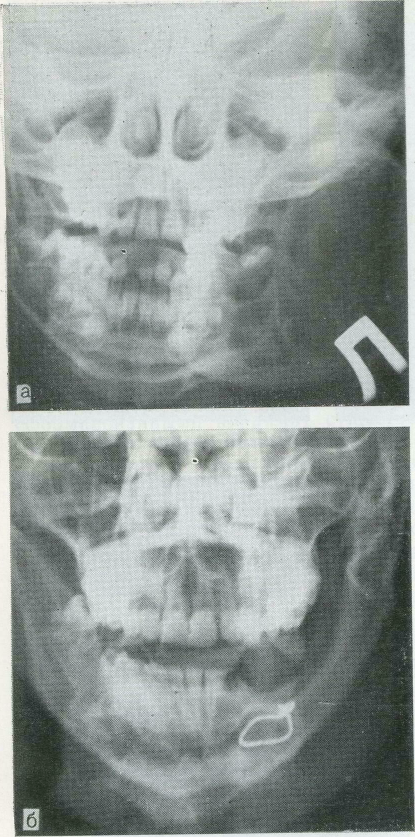
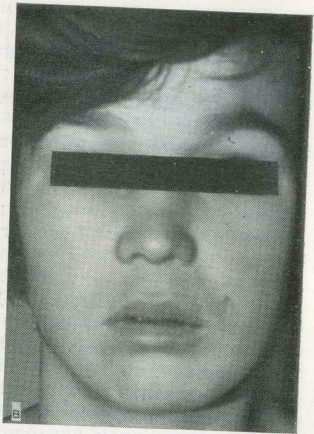
Реабилитация больной после резекции нижней челюсти по поводу первичной (примордиаль-ной) нагноившейся кисты нижней челюсти с.пер-вичной костной пластикой аналогичным алло-трансплантатом.
а — рентгенограмма больной в возрасте 6 лет до операции; б — через 20 лет после операции;
2) выделение группы заболеваний, при которых проведение костной пластики нецелесообразно (активные формы туберкулеза, сахарный диабет, системные костные заболевания, болезни крови, хронические заболевания паренхиматозных органов в стадии декомпенсации);
3) выявление заболеваний, требующих обязательного лечения в предоперационном периоде (воспалительные заболевания ЛОР-органов, острые и хронические заболевания верхних дыхательных путей, гиповитаминозы, анемии и др.).
В связи с анатомической и функциональной незрелостью ряда органов и систем (ЦНС, паренхиматозные органы, тер-
278
75. (продолжение)
морегуляция, водно-солевой баланс и т. д.) при подготовке к операции необходимо учитывать высокую чувствительность ребенка к воздействию внешней и внутренней среды. Чем моложе ребенок, тем ярче проявляются эти особенности. В противном случае в послеоперационном периоде общие симптомы любого заболевания начинают преобладать над местными, что сказывается на исходе костной пластики. Общие санационные мероприятия желательно проводить не позднее чем за 1—2 мес до костной пластики. Это осуществимо при планировании отсроченной и вторичной пластики. Однако при первичной пластике, когда операцию' нельзя откладывать из-за интенсивного роста доброкачественной опухоли или
опухолеподобного процесса, вы- • полнить указанные мероприятия
в полном объеме не представляется возможным. В таких случаях санацию осуществляют во время специальной подготовки и в послеоперационном периоде.
В зависимости от того, будет ли пластика первичной, отсроченной или вторичной, специальная предоперационная подготовка различна по продолжительности и объему мероприятий.
К специальным мероприятиям, проводимым независимо от вида костной пластики, относятся:
1) санация рта: лечение кариеса зубов, его осложнений,
снятие зубных отложений, удаление молочных зубов с резор-
бированными корнями, лечение заболеваний и травматических
' повреждений слизистой оболочки не менее чем за 3—4 нед до
первичной костной пластики;
2) клиническое и рентгенологическое исследование костей лицевого скелета и нижней челюсти для определения протяженности будущего или имеющегося дефекта;
3) изготовление контрольных гипсовых моделей, по которым также можно определить величину дефекта, степень деформации челюстей, зубных рядов, положение зубов и установить степень требуемой «гиперкоррекции» трансплантата;
4) фотографирование больного до операции, что позволяет проследить динамику восстановления контуров лица;
5) выбор способа фиксации трансплантата в костной ране;
279
6) выбор конструкции иммобилизирующего аппарата и его изготовление;
7) подбор аллотрансплантата по структуре ткани, виду и размеру.
До проведения отсроченной и вторичной костной пластики обязательны обследование и ортодонтическое лечение. Последнее должно предшествовать хирургическому и не может быть перенесено на послеоперационный период.
Конструкцию ортодонтического аппарата выбирают в зависимости от результатов рентгенологического исследования и контрольных моделей челюстей.
Совместная работа хирурга, ортодонта и терапевта-стоматолога— обязательное условие на всех этапах проведения ребенку костной пластики: в предоперационном, послеоперационном периодах и в дальнейшем.
Планируя лечение, детей с послеоперационными дефектами и деформациями нижней челюсти после удаления опухолей можно разделить на три группы.
1. Дети, которым костная пластика проводится одновременно с удалением опухоли нижней челюсти. Этих детей готовит к операции группа в составе хирурга-стоматолога, ортодонта, терапевта-стоматолога, педиатра, анестезиолога и по показаниям других специалистов. Время подготовки не более 3—4 нед, иногда меньше, что зависит от темпов роста опухоли, давности ее обнаружения, общего состояния ребенка.
2. Дети, которым по показаниям костная пластика не планируется как одномоментная. С момента выписки их из лечебного учреждения этих больных должен лечить ортодонт. Ребенку изготовляют функциональный ортодонтический аппарат, удерживающий фрагмент или фрагменты челюсти в правильном анатомическом положении до проведения реконструктив-но-восстановительной операции и предупреждающий вторичную деформацию челюстей. В зависимости от характера проведенного ранее лечения период диспансерного наблюдения до операции продолжается от 4—8 мес до 1,5 года. В остальном объем предоперационной подготовки не отличается от такового в первой группе.
3. Дети, которым после удаления опухоли не проводились костная пластика и ортодонтическое лечение. Длительное время перед операцией они должны подвергаться ортодонтиче-скому лечению для нормализации соотношения зубных рядов и прикуса. Результат лечения зависит от времени, прошедшего после удаления опухоли нижней челюсти, возраста больного и состояния прикуса. Сроки костной пластики у таких больных планируются строго индивидуально и зависят от результатов ортодонтического лечения. В дальнейшем подготовка ведется так же, как в первой группе.
К первичной костной пластике все 68 детей были подготовлены по данной схеме.
280
Из 18 детей, которым выполнена отсроченная костная пластика, 4 оперированным в нашей клинике и 2 оперированным в-других клиниках в течение всего периода подготовки к .операт-ции проводилось ортодонтическое лечение. Десяти детям, которые обращались в нашу клинику через 2—3 года и более после удаления опухоли нижней челюсти, ортодонтическое лечение раньше не проводилось, в результате чего были выявлены значительные изменения костных фрагментов и вторичная деформация верхней челюсти. У них обнаружены уменьшение размеров дефекта за счет рубцов, деформация прикуса, аномалии положения зубов, обнажение корня зуба, расположенного-по краю дефекта, с резорбцией альвеолы зуба, значительное изменение внешнего вида. Ортодонтическое лечение в предоперационном периоде полного эффекта не дало.
Из 9 детей, которым проведена вторичная костная пластика, 7 детей, ранее лечившихся в нашей клинике, в период до-повторной операции систематически получали ортодонтическое лечение.
Лечение после реконструктивно-восстановительных операций предусматривает:
1) послеоперационную терапию и профилактику инфекции;
2) иммобилизацию челюстей, наблюдение за послеоперационной раной;
3) клинико-рентгенологический контроль за репаративной регенерацией и качеством формирования регенерата;
4) ортодонтическое лечение и рациональное протезирование;
5) диспансерное наблюдение до окончания роста костей лицевого скелета с постоянной ортодонтической коррекцией прикуса.
Всем больным после костной пластики на 12—14 дней назначали курс антибактериальной, десенсибилизирующей, об-щеукрепляющей терапии и при необходимости повторяли его.
Окончательную иммобилизацию челюстей проводили на второй день после операции и продолжали 50—56 дней, т. е. до> наступления прочной консолидации фрагментов с трансплантатом, что контролировали серией рентгенограмм. Особенности-детского возраста исключают возможность сокращения сроков-, иммобилизации, так как недостаточная минерализация костной ткани, даже при условии более быстрого образования костной мозоли, чем у взрослых, под влиянием функциональной нагрузки может быть причиной неполного формирования регенерата или его резорбции.
В течение всего послеоперационного периода проводили-тщательный уход за полостью рта (многократное орошение полости рта слабыми растворами антисептиков), контролировали степень фиксации иммобилизующих аппаратов. После снятия швов назначали охранительный режим.
После снятия иммобилизующей аппаратуры всем детям изготавливали шины типа Ванкевич или ее модификации, в ре-
28В
зультате чего, начиная с периода прекращения неподвижной
•фиксации, частично разгружалась оперированная нижняя челюсть.
Дозировать функциональную нагрузку на оперированную нижнюю челюсть очень трудно: и избыточная, и недостаточная
•функциональная нагрузка могут быть причиной неполной пере-
•стройки трансплантата или его резорбции. Этот вопрос требует изучения.
После первичной костной пластики при условии полноценного восстановления длины нижней челюсти гиперкоррекцией эстетические результаты операции у детей в возрасте 10— 12 лет и старше всегда хорошие. У детей более раннего возраста (до 10 лет) за счет значительной гиперкоррекции в здоровую сторону поначалу эстетический вид лица неудовлетворительный. Однако после выравнивания нижней челюсти, которое происходит в течение последующих лет, создается хорошая форма лица, вполне удовлетворяющая требованиям, предъявляемым к анатомической форме костей лицевого скелета.
После отсроченной и вторичной костной пластики, независимо от возраста ребенка, оперированная сторона остается несимметричной, что особенно заметно при дефектах половины нижней челюсти и подбородочного отдела. Чем больше времени прошло между основным оперативным вмешательством (удаление опухоли) и костной пластикой, тем труднее устранить эти изменения.
Результаты наших исследований позволяют утверждать, что показания к первичной костной пластике у детей независимо
•от возраста должны быть максимально расширены.
Своевременное возмещение дефекта нижней челюсти алло-костью в сочетании с элементами гиперкоррекции трансплантата приводит к полному восстановлению анатомо-физиологиче-ских свойств зубочелюстной системы и правильному формированию костей лицевого скелета с ростом ребенка.
Наши наблюдения подтверждают, что формирование репа-ративного регенерата продолжается 3—4 года. Скорость и качество его формирования зависят от способа костной пластики, местных условий, размеров трансплантата и в меньшей.
•степени от способа консервации аллотрансплантата. Наиболее активно процесс репаративной регенерации протекает после первичной костной пластики, особенно в тех случаях, когда аллотрансплантат располагается поднадкостнично, менее активно— при отсроченной и вторичной пластике.
строго индивидуальное больного [Виноградо-
полученных результа-
Костный аллотрансплантат, постепенно рассасываясь, замещается костным регенератом, исходящим из тканей воспринимающего костного и мягкотканного ложа. Образующийся репаративный регенерат приобретает строение, характерное для данного ва Т. П., Лаврищева Г. И., 1974J.
Клинико-рентгенологический анализ
282
тов позволяет различать характерные стадии формирования репаративного регенерата нижней челюсти при аллотрансплан-тации.
I стадия — через 50—60 дней после костной пластики на рентгенограмме определяется плотное спаяние воспринимающего костного ложа с аллотрансплантатом. Трансплантат полностью сохраняет первоначальную форму. По верхнему и нижнему краям определяется нежный остеопороз, в результате чего края кажутся слегка неровными.
II стадия — через 120—180 дней (4—6 мес) в области спаяния трансплантата с воспринимающим костным ложем появляется участок структурной костной ткани, идентичной данному участку нижнечелюстной кости. По верхнему и нижнему краям трансплантата усиливаются явления остеопороза. Края трансплантата неровные, а на всем его протяжении появляется множество очажков остеопороза: трансплантат становится пятнистым и как бы фрагментируется.
III стадия — через 8—12 мес плотность трансплантата на всем протяжении постепенно увеличивается, но он остается фрагментированным. По верхнему и нижнему краям трансплантата отчетливо определяется формирование замыкатель-ной кортикальной пластины кости.
IV стадия — через 14—18 мес по краю трансплантата четко прослеживается кортикальная пластинка кости. Площадь фрагментированных участков по всей поверхности трансплантата становится меньше. Участки бесструктурной новообразованной кости располагаются по всему трансплантату.
V стадия — через 1,5 года и более структура в области репаративного регенерата сходна со структурой губчатого вещества кости нижней челюсти больного. Окончательное моделирование формы и внутренней архитектоники репаративного регенерата происходит под воздействием функции. Он приобретает изгибы и конфигурацию, свойственные возмещенному отделу нижней челюсти.
Ортодонтическое лечение детей после костно-пластических реконструктивных операций в послеоперационный период направлено на коррекцию прикуса и должно завершиться рациональным съемным протезированием.
Последовательность ортодонтических мероприятий зависит от возраста ребенка, способа костной пластики, локализации дефекта, степени перестройки аллотрансплантата.
В послеоперационном периоде в течение 4—6 мес дети пользуются аппаратами типа шины Ванкевич, которые удерживают нижнюю челюсть в правильном анатомическом положении и обеспечивают дозированную мышечную нагрузку на трансплантат. Затем при условии прочного спаяния костного трансплантата с воспринимающим ложем ортодонт приступает к исправлению прикуса, используя общепринятые методы лечения индивидуально для каждого больного.
283
Результаты экспериментального исследования [ЕрадзеЕ. ГЦ 1970] свидетельствуют, что консолидация кости реципиента и> трансплантата наступает раньше, чем это выявляется рентгеног-логически. Положительная динамика в перестройке трансплантата, выявляемая при рентгенологическом исследовании, позволяет расширить объем функциональных воздействий на оперированную нижнюю челюсть и своевременно приступить к ор-тодонтическому лечению и рациональному протезированию.
Исходы костной пластики нижней челюсти оценивались нами на основании результатов клинико-рентгенологического обследования детей в разные сроки после лечения. Возможны следующие исходы формирования репаративного регенерата: •
1) аллотрансплантат полностью перестраивается, замещаясь регенератом, который приобретает структуру утраченного отдела нижней челюсти; .
2) аллотрансплантат полностью перестраивается, но не достигает объема, соответствующего утраченному отделу;
3) аллотрансплантат частично рассасывается, в результате чего не восстанавливается непрерывность нижней челюсти, образуется ложный сустав;
, 4) аллотрансплантат полностью рассасывается или отторгается.
При оценке исходов костной пластики учитывали также эстетические и функциональные результаты лечения. Хорошим' результат считали тогда", когда наблюдали полное восстановление непрерывности нижней челюсти за счет образовавшегося-регенерата, хороший эстетический вид ребенка и постепенное выравнивание размеров нижней челюсти к окончанию периода детства, удовлетворительным — если также наблюдали* перестройку трансплантата и восстановление непрерывности' нижней челюсти, но из-за неполного объема регенерата и задержки «роста» челюсти эстетический вид больного оставался-неудовлетворительным, неудовлетворительным — когда происходило рассасывание или отторжение трансплантата, образовывался ложный сустав, возникал перелом трансплантата.
Отдаленные результаты (от 1 года до 20 лет) прослежены у 71 из 86 детей. В 59 случаях результаты первичной, отсроченной и вторичной костной пластики были хорошими, в 8 — удовлетворительными, в 4 — неудовлетворительными. Поскольку условия первичной, отсроченной и вторичной костной пластики различны, мы проанализировали исходы лечения больных каждой из этих групп.
После 68 операций первичной костной пластики отторжение трансплантата произошло у 7 детей: у 6 в связи с развитием нагноения трансплантата и у одного ребенка 3 лет в результате иммунологического конфликта.
Анализ осложнений при первичной костной пластике показал, что недостаточно развитая система иммунной защиты, особенно у детей раннего возраста, играет решающую роль в раз-
284
I' витии и активном течении воспя
' возможность сохранения аллогенн.НИЯ> ЧТ° Часто ис'КЛ1°чает стентного к воздействию инфекции тРансплантата, нерези-
В 2 случаях после первичной 'кортнпй п
плохой иммобилизации челюстей тнои пластики вследствие трансплантата. В качестве иммобили™Г°ШеЛ пеРелом алл°- детей была применена шина Ван!, эппарата у этих видной повязкой. Другие способ^ В сочетании с праще- вать не удалось из-за ранней Si ИММобилизаЦии использо- результате кариеса и его осложнен^ЖесТВеннои потеРи 3Уб°в в
После 18 операций отсроченной
перестройка трансплантата наблю1™яС™°И чпластики неполная его-у 3, перелом трансплантата^ пУ ' ^астичныи лизис жекие трансплантата произошло у о J • больного- °ТТОР-
После вторичной костной пляп етеи-
тата отмечено у 4 из 9 больных. Ики отторжение трансплан-Высокий процент осложнений пг^п„
ной костной пластики — следствие * отсР°ченнои и вторич- рубцовых изменений в области л1 л неблагоприятного влияния ной регенерации. К такому же вк«РеКТа Н3 пРоцесс репаратив- [Кабаков Б. Д., 1968; Чаклин В Т" Ж™?! MH°™e ^^ 1979J. Грубые рубцы и склеооз \Г" 70; Пло™иков Н. А., фрагментов мешают развитию copv?1^* отделов костных щей перестройке аллотранс^а^Зй Тт ?™' СпособствУю- сплантата не становится полноценна РУбЦ°в°е ложе тран- вания. В результате этого нарушЛ^ источником костеобразо- генерации, что и приводит к опирЛ РИ™ РепаРативной ре- Разработанные в настоящее вое».о ВЫШе осложнениям. нижней челюсти у детей алло^ины/™" костной пластики . ляют получить надежные результат трансплантатами позво- туров нижней челюсти и лица восотяНД°биться УлУчщения кон- люстной системы. Однако vcoBenmJ Ления ФУНК«ИИ зубоче- ченной и вторичной костной пласта^"™"™6 МеТ°^°В ОТСР°' нейших проблем, требующей hhti»« является одной из важ-
j щ, пп^нсивного изучения.
