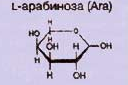
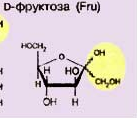
- •Вопрос 1. Полисахариды: характеристика, строение, классификация и функции.
- •Вопрос 2. Крахмал. Гидролиз крахмала (кислотный и ферментативный). Технология производства крахмала. Модифицированные крахмала и их применение.
- •Механизм действия различных типов амилаз на крахмал:
- •- Замещенные крахмалы:
- •Вопрос 3. Структурные полисахариды
Тема 3 Полисахариды. Лекция 3
Вопрос 1. Полисахариды: характеристика, строение, классификация и функции.
Вопрос 2. Крахмал. Технология производства крахмала. Модификация крахмала и их применение. Гидролиз крахмала (кислотный и ферментативный).
Вопрос 3. Структурные полисахариды.
Вопрос 1. Полисахариды: характеристика, строение, классификация и функции.
Полисахариды - высокомолекулярные продукты поликонденсации моносахаридов, связанных с друг другом гликозидными связями и образующих линейные или разветвленные цепи.
Полисахариды широко распространены в природе и составляют преобладающую массу биополимеров на земле. Растения содержат 80-90% всех полисахаридов и являются основными источниками их получения.
Полисахариды разнообразны по своему строению:
-полисахариды, построенные из моносахаридных звеньев одного типа, называются гомогликаны (крахмал, целлюлоза, инулин),
- полисахариды построенные из различных моносахаридных звеньев — гетерогликаны (пектиновые вещества, камеди, слизи). Оба полимера могут быть линейными или разветвленными.
По функциональным свойствам полисахариды подразделяются на три группы:
- структурные - придают клеткам, oрганам и целым организмам механическую прочность;
- водорастворимые - высоко гидратированы и предохраняют от высыхания клетки и ткани;
- резервные - служат энергетическим ресурсом, из которого по мере необходимости в организм поступают моносахариды, являющиеся клеточным "топливом".
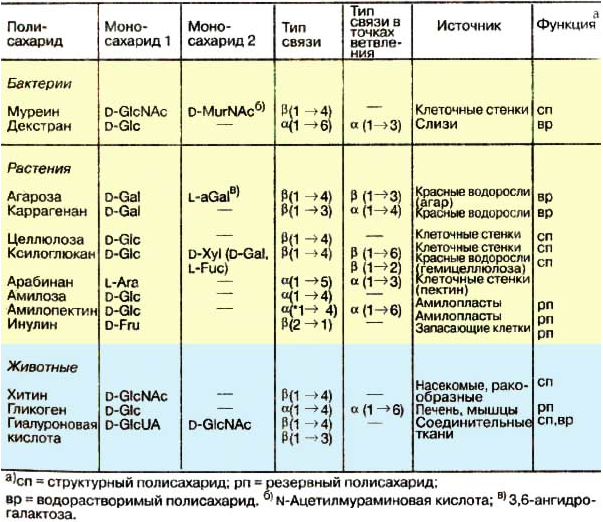
Благодаря полимерной природе резервные полисахариды осмотически неактивны и поэтому могут накапливаться в клетках в больших количествах. В таблице приведены важнейшие представители полисахаридов:
|
|
Вопрос 2. Крахмал. Гидролиз крахмала (кислотный и ферментативный). Технология производства крахмала. Модифицированные крахмала и их применение.
Крахмал – это главный резервный полисахарид растений, являющийся наиболее важным углеводным компонентом пищевого рациона. Запасается крахмал в семенах хлебных злаков, клубнях, корневищах в виде крахмальных зерен, которые в зависимости от вида растения имеют различную форму (сферическая, яйцевидная, чечевицеобразная или неправильная) и размер (1 до 150 мкм, в среднем 30-50 мкм).
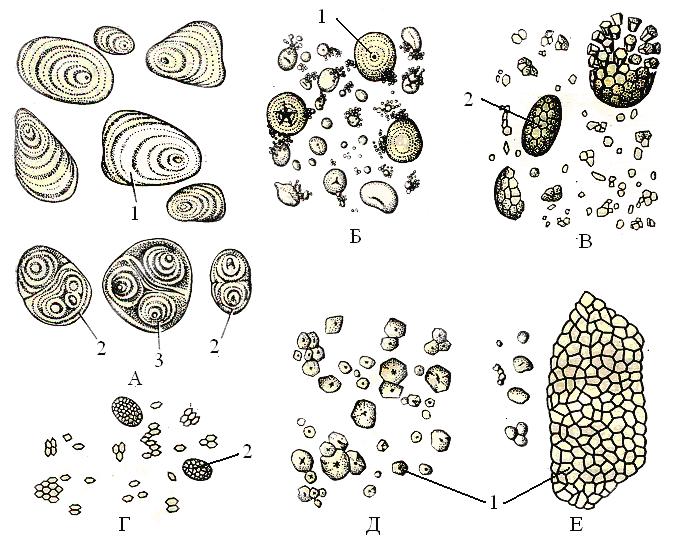
Крахмальные зерна различных видов растений:
А - картофель; Б - пшеница; В - овес; Г - рис; Д - кукуруза; Е - гречиха.
1 - простое крахмальное зерно, 2 - сложное, 3 - полусложное.
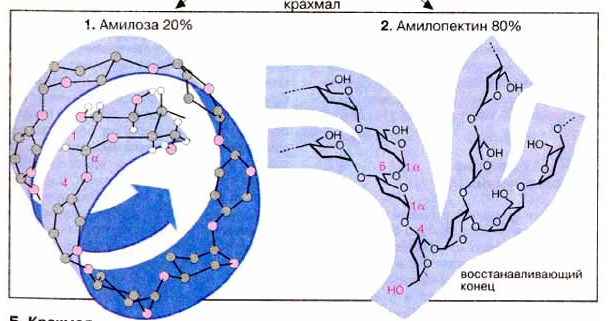
Крахмал имеет сложное строение и состоит из двух гомополисахаридов: растворимой в воде амилозы и нерастворимого амилопектина. Их соотношение в крахмале может различаться в зависимости от растения и типа ткани, из которой он был выделен (амилоза 13-30%; амилопектина 70-85%).
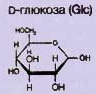
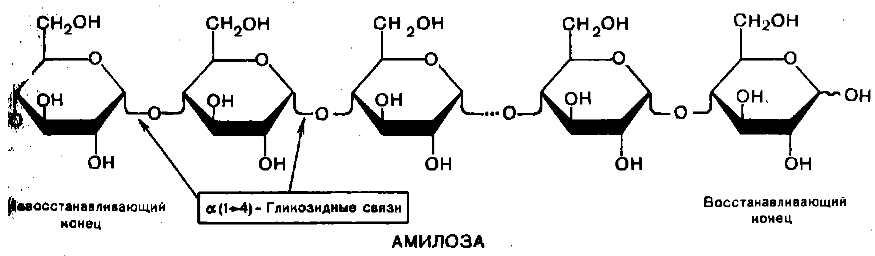
Амилоза состоит из неразветвленных (линейных) цепей, включающих 200-300 остатков глюкозы, связанных α(1→4) гликозидной связью. Благодаря α-конфигурации при С-1, цепи образуют спираль диаметром 13 нм, в которой на один виток приходится 6-8 остатков глюкозы. Молекулярная масса составляет 50000Да.
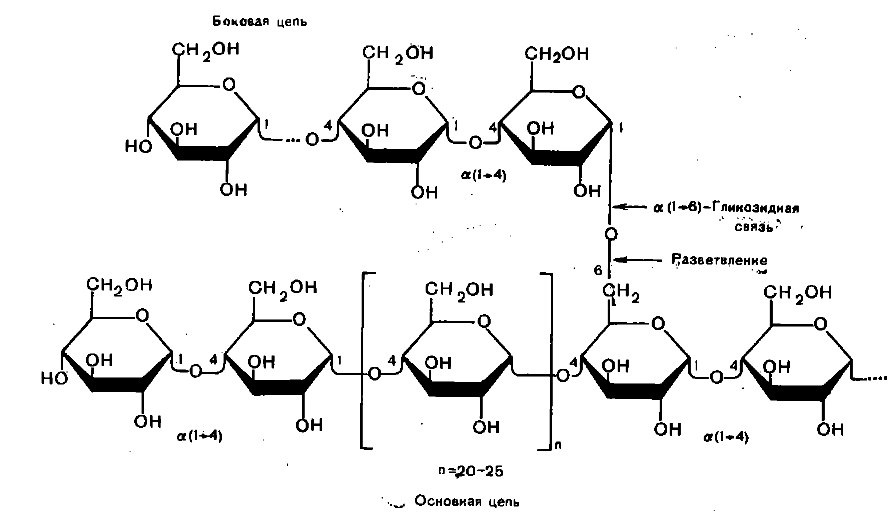
Амилопектин имеет разветвленную структуру, у которой в среднем один из 20-25 остатков глюкозы содержит боковую цепь, присоединенную α(1→6) гликозидной связью. При этом формируется древовидная структура. Молекулярная масса составляет достигает 1-6 млн. Да.
Гидролиз крахмала присутствует во многих пищевых технологиях как один из необходимых процессов, обеспечивающих качество конечного продукта. Например:
- в хлебопечении – процесс тестоприготовления и выпечки хлеба;
- в производстве пива – получение пивного сусла и сушка солода;
- в производство кваса;
- в производстве спирта – подготовка сырья для брожения;
- в получении различных сахаристых крахмалопродуктов – глюкозы, патоки, сахарных сиропов.
Существует два метода гидролиза крахмала:
- кислотный – под действием минеральных кислот;
- ферментативный - под действием ферментных препаратов.
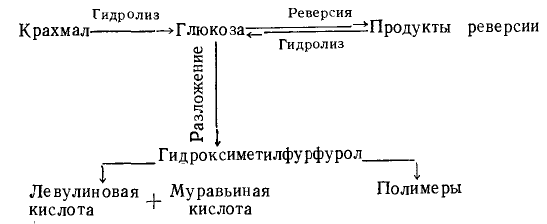
При гидролизе крахмала под действием кислот сначала имеет место ослабление и разрыв ассоциативных связей между макромолекулами амилозы и амилопектина. Это сопровождается нарушением структуры крахмальных зерен и образованием гомогенной массы. Далее идет разрыв α(1→4) и α(1→6)-гликозидных связей с присоединением по месту разрыва молекулы воды. В процессе гидролиза нарастает число свободных альдегидных групп, уменьшается степень полимеризации. На промежуточных стадиях образуются декстрины, три и тетрасахара, мальтоза. Конечным продуктом гидролиза является глюкоза. Кислотный гидролиз имеет ряд существенных недостатков, обуславливаемых использованием высоких концентраций кислот и высокой температуры (свыше 100 °С), что приводить к образованию продуктов термической деградации и дегидратации углеводов, реакциям трансгликозилирования и реверсии.
![]()
![]()
По сравнению с кислотным гидролизом ферментативный гидролиз является более перспективным и имеет следующие преимущества:
Высокое качество изготовляемого продукта, т.к. образуется меньше побочных продуктов;
Специфичность действия ферментов позволяет получить продукт с заданными физическими свойствами (например сладостью);
Достигается высокий выход продукта с меньшими экономическими затратами.
Ферментативный гидролиз крахмала осуществляется с помощью амилолитических ферментов. К этой группе относятся α-амилаза, β-амилаза, глюкоамилаза, пуллуланаза и некоторые другие ферменты. Каждый из них имеет свои специфические особенности.
α-амилаза – эндофермент, гидролизующий α (1-4)-гликозидные связи внутри молекулы амилозы или амилопектина, в результате образуются декстрины – продукты неполного гидролиза крахмала и малое количество глюкозы и мальтозы:
![]()
α-амилаза найдена у животных (слюна и поджелудочная железа), у высших растений (проросшие семена ячменя, пшеницы, ржи, проса) и у микроорганизмов (грибов рода Aspergillus, Rhizopus, бактерий рода Bacillus subtilis).
β-амилаза – экзофермент, гидролизует α (1-4)-гликозидные связи с нередуцирующих концов молекулы амилозы, амилопектина с образованием мальтозы (54-58%), т.е. проявляет выраженную осахаривающую активность. Другим продуктом реакции является β-декстрин (42-46%). Данный фермент распространен в тканях высших растений.
![]()
Глюкоамилаза является экзоферментом, действуя с нередуцирующих концов молекулы амилозы и амилопектина, отщепляет молекулы глюкозы гидролизуя α (1-4)- и α (1-6)-гликозидные связи. Данный фермент наиболее часто встречается у микромицетов рода Aspergillus, Rhizopus.