
Лекция 8
Физика атомного ядра и элементарных частиц
В древности считалось, что простейшими частицами вещества являются атомы. Развитие физики показало, что это не так. Была обнаружена субатомная структура материи.
Ядро простейшего атома – атома водорода – состоит из одного протона. Ядра всех остальных атомов состоят их двух видов частиц – протонов и нейтронов – которые называются нуклонами.
Протон (p)обладает зарядом +е и массой m=1.67*10-27 кг , Е0= 938,28 МэВ, mp=938.28 МэВ/с2 ( в ядерной физике принято выражать массы в единицах энергии, умножая их для этой цели на с2). Для сравнения укажем, что масса покоя электрона mе=0.511 МэВ, следовательно, mp= 1836 mе..
Нейтрон (n) обладает зарядом +е и массой m=1.68*10-27 кг , Е0= 939,57 МэВ.
У протона и нейтрона спин равен ½.
Разность масс покоя нейтрона и протона составляет 1.3 МэВ, т.е. 2.5 mе. В свободном состоянии нейтрон нестабилен (радиоактивен), он самопроизвольно распадается и превращается в протон, испуская электрон (е-) и антинейтрино (*).
Период полураспада, т.е. время, за которое распадается половина первоначального количества нейтронов, равен примерно 16 мин. Схему распада можно написать следующим образом :
n p + e- + * .
Заметим, что масса нейтрона превышает суммарную массу частиц в правой части схемы распада на 1.5 mе ( масса нейтрино равна нулю), следовательно, энергия 0.78 МэВ выделяется при распаде нейтрона в виде кинетической энергии образующихся частиц.
Характеристики атомного ядра.
Одной их важнейших характеристик атомного ядра является зарядовое число Z, равное количеству протонов, входящих в состав ядра. Z определяет заряд ядра, который равен +Ze, а также номер химического элемента в периодической системе Менделеева. Число нуклонов ( т.е. суммарное число протонов и нейтронов) в ядре обозначается буквой А и называется массовым числом ядра. Число нейтронов в ядре равно N = A – Z. Для обозначения ядер применяется символ ZAX, где под X подразумевается химический символ данного элемента. Ядра с одинаковыми Z, но разными А называются изотопами. Большинство химических элементов имеет несколько стабильных изотопов. Например, водород имеет три изотопа : обычный водород, или протий 11Н, тяжелый водород, или дейтерий 12Н, и тритий 13Н. Протий и дейтерий стабильны, а тритий радиоактивен.
Известно около 1500 ядер, различающихся либо Z, либо А, либо и тем и другим. Примерно 1/5 часть этих ядер устойчива, остальные радиоактивны. В природе встречаются элементы с атомными номерами Z от 1 до 92 (исключая технеций и прометий), остальные трансурановые элементы получены искусственным путем с помощью ядерных реакций. Размер ядра соответствует размеру шара с радиусом R1.3 A1/3 фм, 1 фм=10-11см.
Масса и энергия связи ядер.
Масса ядра всегда меньше суммы масс входящих в него частиц. Это обусловлено тем, что при объединении нуклонов в ядро выделяется энергия связи нуклонов друг с другом. Энергия покоя частицы связана с ее массой соотношением Е0=mc2. Следовательно, энергия покоящегося ядра меньше суммарной энергии невзаимодействующих покоящихся нуклонов на величину
Есв = с2 { [ Zmp+ (A – Z ) mn ] – mя }. (1)
Эта величина и есть энергия связи нуклонов в ядре. Она равна работе, которую необходимо совершить, чтобы разделить ядро на нуклоны и удалить их на такие расстояния, на которых они практически не взаимодействуют друг с другом ( при этом считается, что в конечном состоянии кинетическая энергия нуклонов равна нулю).
Энергия связи, приходящаяся на один нуклон Есв / А, называется удельной энергией связи нуклонов в ядре. Величина
m = [ Zmp+ (A – Z ) mn ] – mя
называется дефектом массы ядра. Дефект массы связан с энергией связи соотношением m = Есв / с2.
Пример. Энергия связи в ядре атома гелия.
Есв=(2*938.3+2*939.6)-3726.028 МэВ
Рис.
1.
Удельная
энергия связи в зависимости от числа
нуклонов в ядре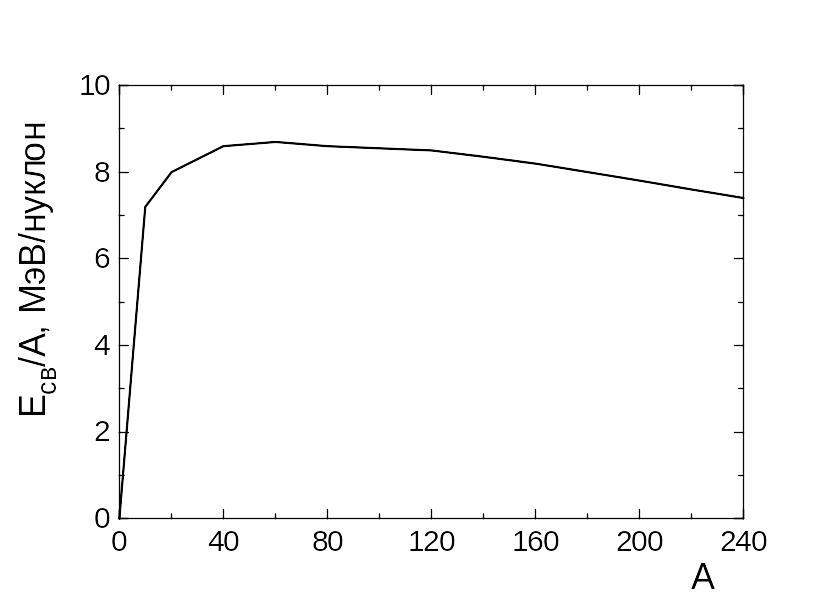
На рис. 1 изображен график, показывающий зависимость удельной энергии связи Есв/A от массового числа А. Сильнее всего связаны нуклоны в ядрах с массовыми числами порядка 50-60 ( для элементов от Cr до Zn ). Такая зависимость делает энергетически выгодными два процесса: 1) деление тяжелых ядер на несколько более легких ядер и 2) слияние легких ядер в одно ядро. Оба процесса должны сопровождаться выделением большого количества энергии. Так, деление одного ядра с массовым числом А=240 (Есв/A =7.5 МэВ) на два ядра с массовыми числами А=120 (Есв/A =8.5 МэВ) привело бы к высвобождению энергии в 240 МэВ. Слияние двух ядер тяжелого водорода 12Н в ядро гелия 24Не привело бы к выделению энергии равной 24 МэВ.
Ядра со значениями А от 50 до 60 являются наиболее устойчивыми. Почему ядра с другими значениями А оказываются стабильными? Для того чтобы тяжелое ядро разделилось на несколько частей, оно должно пройти ряд промежуточных состояний, энергия которых превышает энергию основного ядра. Следовательно, для начала процесса деления ядру необходима дополнительная энергия (энергия активации). В обычных условиях ядро не получает энергии активации, поэтому спонтанного деления тяжелых ядер не происходит.
Энергия активации может быть передана тяжелому ядру захваченным им дополнительным нейтроном. Процесс деления ядер урана или плутония под действием захватываемых ядрами нейтронов лежит в основе действия ядерных реакторов и атомной бомбы. Что касается легких ядер, то для их слияния в одно ядро они должны подойти друг к другу на весьма близкое расстояние ( 10-13 см ). Такому сближению ядер препятствует кулоновское отталкивание между ними. Для преодоления этого отталкивания ядра должны иметь очень большую кинетическую энергию, соответствующую температурам порядка нескольких миллионов Кельвинов. Поэтому процесс синтеза легких ядер называется термоядерной реакцией. Термоядерные реакции протекают в недрах Солнца и других звезд. В земных условиях пока были осуществлены только неуправляемые термоядерные реакции
при взрывах водородных бомб.
