5.2. Расчет и анализ данных, или анализ результатов наблюдений
При повышении
температуры цвет раствора в пробирке
светлеет, а при уменьшении становиться
ярко-синий (голубой) относительно
контрольной пробирке.
При изменении
температуры изменяется как прямая, так
и обратная реакция, но в разной степени.
Для определения
направления смещения равновесия
необходимо определить тепловой эффект
процесса.

Если энергия
активации прямой реакции больше энергии
активации обратной, что характерна для
эндотермической реакции (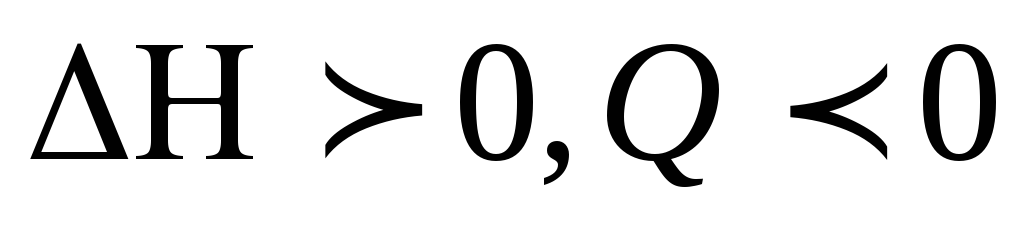 ),
то с увеличением температуры скорость
прямой реакции увеличивается больше
чем скорость обратной (
),
то с увеличением температуры скорость
прямой реакции увеличивается больше
чем скорость обратной ( следствие из уравнение Аррениуса).
Следовательно, повышение температуры
увеличивает константу равновесия
эндотермической реакции, т.к. увеличивается
отношение
следствие из уравнение Аррениуса).
Следовательно, повышение температуры
увеличивает константу равновесия
эндотермической реакции, т.к. увеличивается
отношение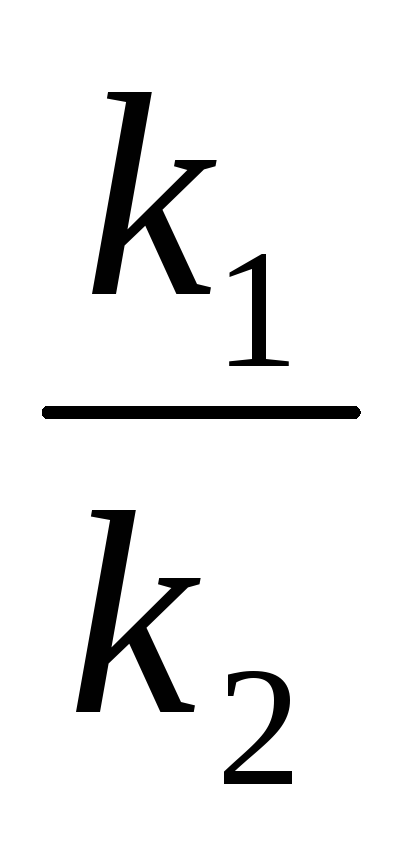 .
.
В нашем случае
энергия активации прямой реакции, меньше
энергии активации обратной, т.е. реакция
экзотермическая (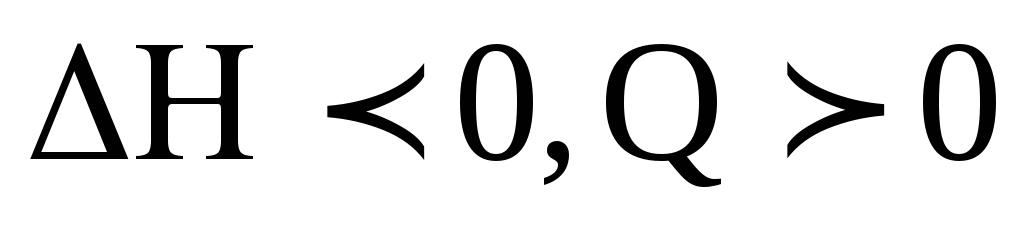 ).
С увеличением температуры скорость
обратной реакции увеличивается больше,
чем скорость прямой (
).
С увеличением температуры скорость
обратной реакции увеличивается больше,
чем скорость прямой (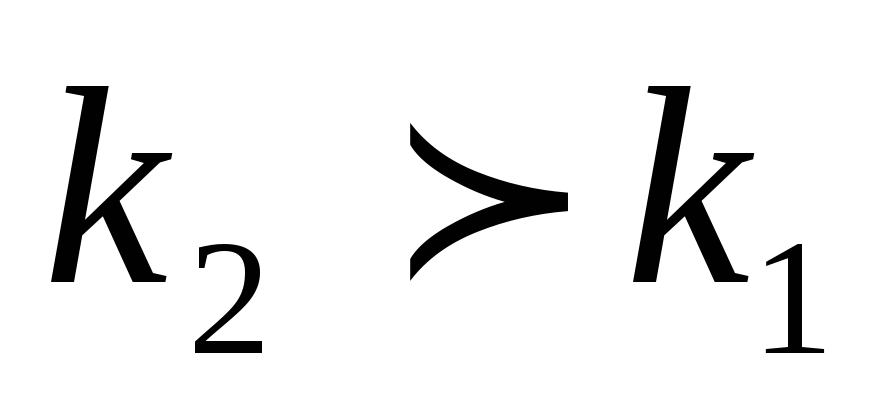 ).
Следовательно повышение температуры
уменьшает константу равновесия
экзотермической реакции, т.к. отношение
).
Следовательно повышение температуры
уменьшает константу равновесия
экзотермической реакции, т.к. отношение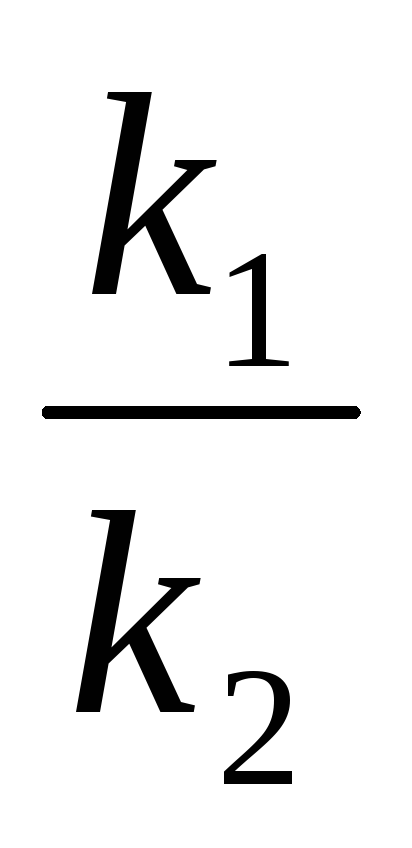 .
.
5.3. Вывод
При
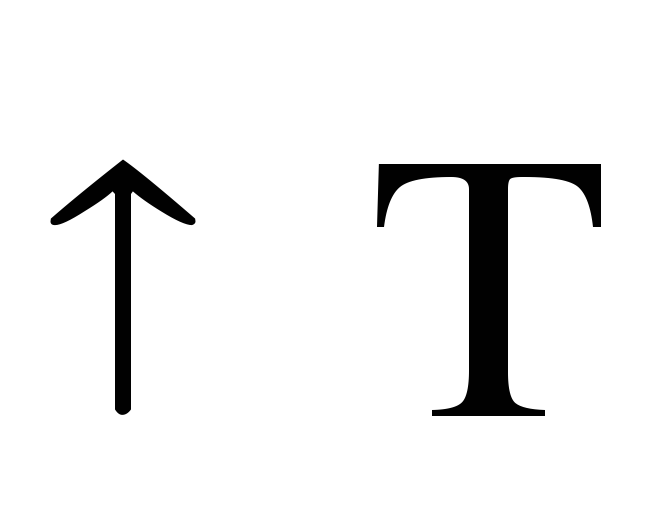 равновесие смещается в сторону
эндотермической реакции(
равновесие смещается в сторону
эндотермической реакции( ),
а при
),
а при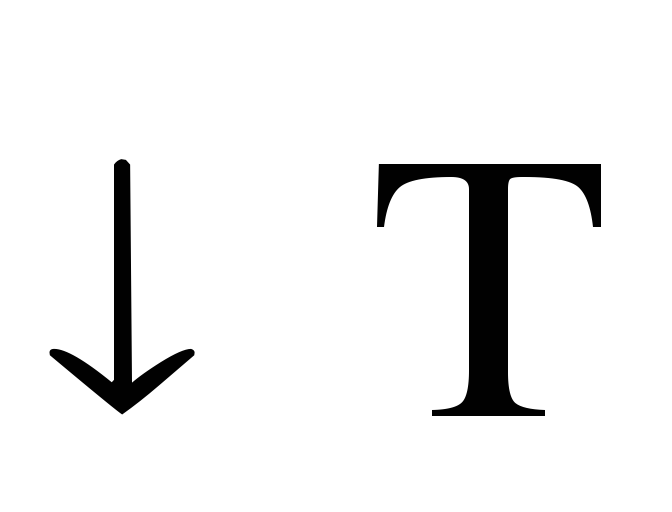 в сторону экзотермической (
в сторону экзотермической (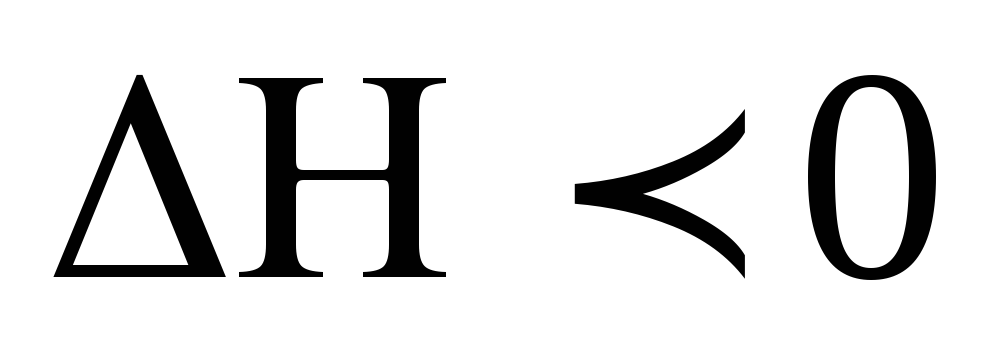
 )
)

