
- •Сборник контрольных работ по курсу общей химии
- •1. Основные классы неорганических соединений
- •Назовите следующие вещества и укажите, к какому классу химических соединений они относятся:
- •Напишите формулы следующих соединений:
- •Составьте уравнения реакций получения следующих соединений и рассчитайте массы реагентов, необходимых для получения 1 г вещества:
- •1.4. Напишите уравнения соответствующих реакций, учитывая, что другие вещества можно использовать только в качестве катализаторов:
- •1.5. Изобразите графические (структурные) формулы следующих соединений:
- •2. Основные законы химии
- •2.1. Рассчитайте давление в сосуде:
- •2.2. Вычислите эквивалентную массу:
- •2.3. Определите простейшую формулу вещества, если оно содержит (по массе):
- •2.4. Расставьте стехиометрические коэффициенты в приведенных схемах реакций и рассчитайте, какую массу второго реагента нужно взять на 1 г первого, чтобы реакция прошла до конца:
- •Определите, какие продукты и в каком количестве (по массе) получатся при взаимодействии (обратите внимание на избыток одного из реагентов):
- •3. Строение атома и химическая связь
- •3.2. Определите, относится ли данная электронно-ячеечная формула к основному, возбужденному или невозможному состоянию атома, назовите химический элемент и укажите его порядковый номер:
- •Напишите уравнения ядерных реакций:
- •4.1. Пользуясь справочными данными, вычислите тепловой эффект (изменение энтальпии) реакций:
- •4.2. Не производя вычислений, определите знак изменения энтропии в следующих реакциях:
- •4.3. Вычислите изменение свободной энергии Гиббса и определите возможность протекания реакции при стандартных условиях:
- •5. Химическая кинетика и равновесие
- •5.1. Определите порядок реакции и рассчитайте, как изменится начальная скорость гомогенных химических реакций согласно закону действующих масс:
- •5.2. Рассчитайте, как изменится скорость реакции при изменении температуры:
- •5.3. Определите, в каком направлении сместится равновесие гомогенных химических реакций, для оценки влияния температуры на степень смещения химического равновесия рассчитать δн реакции:
- •5.4. Найдите константы равновесия гомогенных химических реакций и исходные концентрации реагентов, если в закрытом сосуде установились следующие равновесные концентрации:
- •6. Растворы
- •6.1. Определите массовую долю (в процентах) и молярную концентрацию раствора, содержащего:
- •6.2. Определите массовую долю (в процентах) и моляльную концентрацию растворов, полученных:
- •6.3. Определите относительное понижение давления пара над раствором, содержащим:
- •6.4. Найдите температуру кипения раствора, содержащего:
- •6.5. Найдите температуру замерзания раствора, содержащего:
- •7. Теория электролитической диссоциации
- •7.2. Определите pH следующих растворов электролитов (изменением объема при смешении растворов пренебречь):
- •7.4. Рассчитайте степень диссоциации в следующих растворах слабых электролитов, пользуясь справочными данными о Ка (для много-основных кислот учитывайте только первую ступень диссоциации):
- •8. Окислительно-восстановительные реакции
- •8.1. Определите степени окисления элементов в веществах:
- •8.2. Укажите, какие атомы окисляются, а какие восстанавливаются в указанных схемах, и определите, как изменяется их степень окисления:
- •8.3. Расставьте коэффициенты в уравнениях окислительно-восстановительных реакций ионно-электронным способом:
- •8.4. Определите, в каком направлении протекает реакция в системе, используя справочные данные о стандартных восстановительных потенциалах полуреакций:
- •9. Электрохимические процессы и системы
- •Вычислите электродные потенциалы металлов, находящихся в контакте с растворами их солей заданной концентрации, при 25с:
- •Напишите уравнения электродных реакций на катоде и аноде и вычислите эдс гальванических элементов при 25с, для которых указаны концентрации ионов металла в растворах:
- •Каковы катодные и анодные процессы (угольный анод) при электролизе водного раствора, содержащего смесь солей:
- •9.5. Напишите уравнения, отражающие анодный и катодный процессы при электрохимической коррозии в указанных ниже системах:
- •10. Примеры решения типовых задач
- •11. Примеры задач повышенной трудности
- •Литература
- •Издательство «Экоцентр»
Казанский государственный технический университет им. А.Н. Туполева
Сборник контрольных работ по курсу общей химии
Учебное пособие
H(реакции)=
=Hf (продуктов)– Hf (реагентов)
Казань – 2006
Печатается по рекомендации УМЦ КГТУ им. А.Н. Туполева
Рецензенты:
проф. Будников Г.К.
(Казанский государственный университет)
проф. Евгеньев М.И.
(Казанский государственный технологический университет)
Авторы: А.Н. Глебов, А.Р. Буданов, О.В. Лавриненко,Н.М. Воеводина,
И.П. Оранская, И.Г. Григорьева, С.А. Мальцева, А.И. Шамкаева,
А.А. Кулаков, Н.В. Кремлева, Э.В. Гоголь, А.Г. Мельникова,
А.В. Желовицкая, Р.Р. Гумерова, А.И. Юнусова, Д.В. Фролов,
Е.П. Чеклаукова, С.М. Шавалеева, Е.Н. Офицеров
Сборник контрольных работ по курсу общей химии: Учебное пособие для студентов всех форм обучения/Под редакцией проф. А.Н. Глебова. – 3-е изд., перераб. и доп. – Казань: «Экоцентр», 2006. – 44 стр.
Учебное пособие предназначено для студентов технического университета, изучающих общую химию по дневной, вечерней и заочной формам обучения. Пособие составлено в соответствии с учебным планом, программой курса общей химии. «Сборник контрольных работ» способствует более полному освоению изучаемого материала и развитию навыков самостоятельной работы студентов. В пособии приведены контрольные задания по основным темам курса общей химии, необходимые расчетные формулы, даны решения типовых задач. Необходимые справочные данные приведены в «Практикуме по общей химии» Часть I, Казань, изд-во «Экоцентр», 2003 г., 88 с.
Издательство «Экоцентр», 2006 г.
1. Основные классы неорганических соединений
Классификация химических соединений базируется на реагентах и продуктах одной из основных химических реакций — реакции нейтрализации: оксиды (кислотные и основные), кислоты, основания, соли. Взаимосвязь между основными классами неорганических веществ можно упрощенно представить в виде схемы:
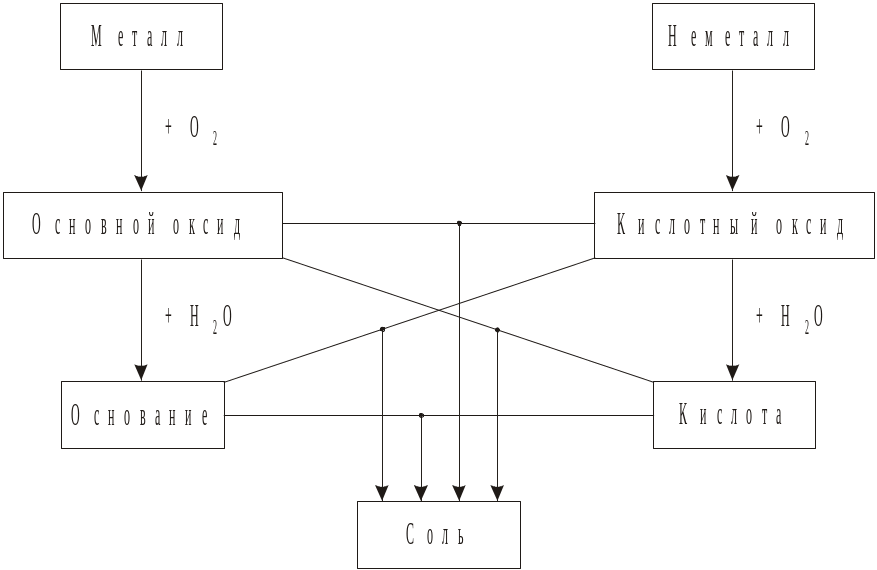
Химические свойства основных классов неорганических соединений:
|
Металл |
Основной оксид |
Основание |
Соль |
Неметалл |
Fe + S =FeS |
— |
— |
2NaBr + Cl2 = 2NaCl + Br2 |
Кислотный оксид |
— |
CaO + CO2 = CaCO3 |
2NaOH + CO2 = Na2CO3 + H2O |
— |
Кислота |
Fe + 2HCl = FeCl2 + H2 |
CaO + H2SO4 = CaSO4 + H2O |
NaOH + HCl = NaCl + H2O |
BaCl2 + H2SO4 = BaSO4↓ + 2HCl |
Соль |
Zn + CuSO4= Cu + ZnSO4 |
— |
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4 |
AgNO3 + NaCl = AgCl↓ + NaNO3 |
