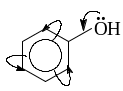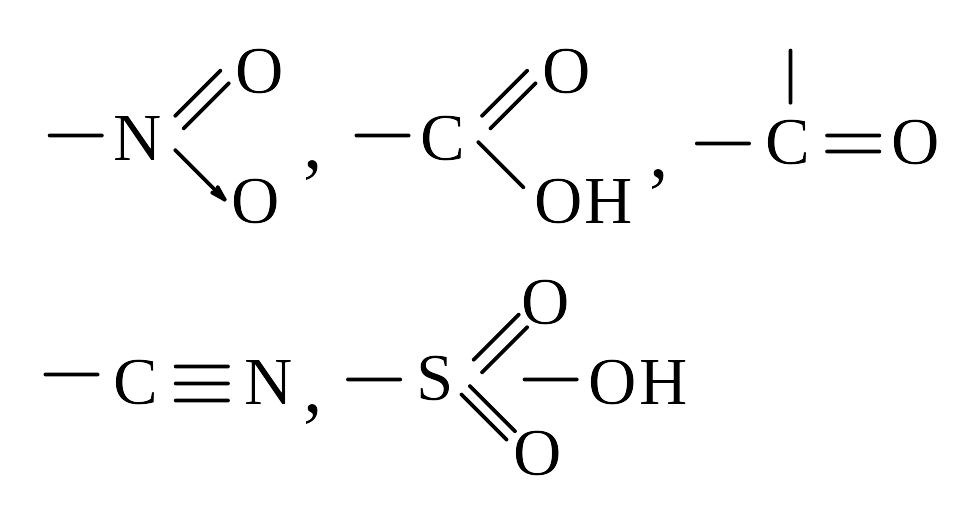- •Ароматичность
- •Взаимное влияние атомов в молекуле
- •Индуктивный эффект
- •Мезомерный эффект
- •Классификация органических реакций
- •Вопросы для самоконтроля:
- •Упражнения
- •Тесты для самостоятельной работы студентов Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Ответы к тестам “ Взаимное влияние атомов в молекуле.”
- •Кислотность и основность органических соединений
- •Органические кислоты
- •Зависимость кислотности от гетероатома.
- •Влияние углеводородного радикала и присутствующих в нем заместителей
- •Влияние растворителя.
- •Основность органических соединений.
- •Факторы, влияющие на основность
- •Вопросы для самоконтроля
- •Упражнения
Модуль I
Занятие №1: “ Взаимное влияние функциональных групп в молекулах биологически активных поли- , гетерофункциональных и высокомолекулярных органических соединений. Особенности химического поведения поли- и гетерофункциональных соединений: кислотно – основные, хелатообразование.”
Цель занятия: изучение электронного строения органических соединений и способов передачи взаимного влияния атомов в их молекулах.
Студент должен знать:
- теорию электронных эффектов,
- объяснять влияние заместителей на электронную плотность молекулы, их влияние на реакционный центр;
- теорию кислотно-основных свойств органических соединений.
Студент должен уметь
- на основании взаимного влияния функциональных групп в молекулах биологически важных веществ сравнивать и предсказывать их реакционную способность;
- сравнивать кислотность и основность поли- и гетерофункциональных соединений, объяснять различия в этих свойствах.
Сопряженные системы
В простейшем случае сопряженные системы – это системы с чередующимися двойными и одинарными связями. Они могут быть открытыми и закрытыми. Открытая система имеется в диеновых углеводородах (УВ).
П
-электрон
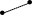
 римеры:
римеры:
С 4Н6
4Н6
С
 Н2
= СН – СН = СН2
Н2
= СН – СН = СН2
 Бутадиен-1,
3
Бутадиен-1,
3


Все атомы С находится в состоянии sp2 – гибридизации. Четыре негибридные (р-орбитами), перекрываясь между собой, образуют единую электронную систему. Этот вид сопряжения наз-ся , -сопряжением.
С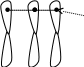
 2Н3Сl
2Н3Сl
Х
р-электроны
СН2 = СН – Сl
Здесь происходит сопряжение -электронов с р-электронами. Этот вид сопряжения наз-ся р, -сопряжением.
Закрытая система имеется в ароматических УВ.
С 6Н6
6Н6
Б
Сопряжение –
процесс энергетически выгодный, энергия
(Е) при этом выделяется.
Энергия сопряжения
бутадиена-1,3 составляет 15 кДж/моль,
энергия сопряжения бензола – 228 кДж/моль.
Ароматичность
Это понятие, включающее различные свойства ароматических соединений. Условия ароматичности: 1) плоский замкнутый цикл, 2) все атомы С находятся в sp2 – гибридизации, 3) образуется единая сопряженная система всех атомов цикла, 4) выполняется правило Хюккеля: “В сопряжении участвуют 4n+2 -электронов, где n = 1, 2, 3... ”
Простейший представитель ароматических УВ – бензол. Он удовлетворяет всем четырем условиям ароматичности.
Правило Хюккеля: 4n+2 = 6, n = 1.
Нафталин |
Нафталин – ароматическое соединение Правило Хюккеля: 4n+2 = 10, n = 2. |
Пиридин |
Пиридин – ароматическое гетероциклическое соединение. |
Взаимное влияние атомов в молекуле
В 1861 г русский ученый А.М. Бутлеров высказал положение: «Атомы в молекулах взаимно влияют друг на друга». В настоящее время это влияние передается двумя путями: индуктивным и мезомерным эффектами.
Индуктивный эффект
Это передача электронного влияния по цепи -связи. Известно, что связь между атомами с различной электроотрицательностью (ЭО) поляризована, т.е. смещена к более ЭО атому. Это приводит к появлению на атомах эффективных (реальных) зарядов (). Такое электронное смещение наз-ся индуктивным и обозначается буквой I и стрелкой .
![]() ,
X = Наl
,
НО ,
НS
,
NН2
и др.
,
X = Наl
,
НО ,
НS
,
NН2
и др.
Индуктивный эффект может быть положительным или отрицательным. Если заместитель Х притягивает электроны химической связи сильнее, чем атом Н, то он проявляет – I. I(Н) = О. В нашем примере Х проявляет – I.
Если заместитель Х притягивает электроны связи слабее, чем атом Н, то он проявляет +I. Все алкилы (R = СН3 , С2Н5 и т.д.), Меn+ проявляют +I.
Мезомерный эффект
М езомерный
эффект (эффект сопряжения) – это влияние
заместителя, передаваемое по сопряженной
системе -связей.
Обозначается буквой М и изогнутой
стрелкой . Мезомерный эффект может
быть «+» или «–».
езомерный
эффект (эффект сопряжения) – это влияние
заместителя, передаваемое по сопряженной
системе -связей.
Обозначается буквой М и изогнутой
стрелкой . Мезомерный эффект может
быть «+» или «–».
Выше было сказано, что имеется два вида сопряжения , и р, .
Примеры:
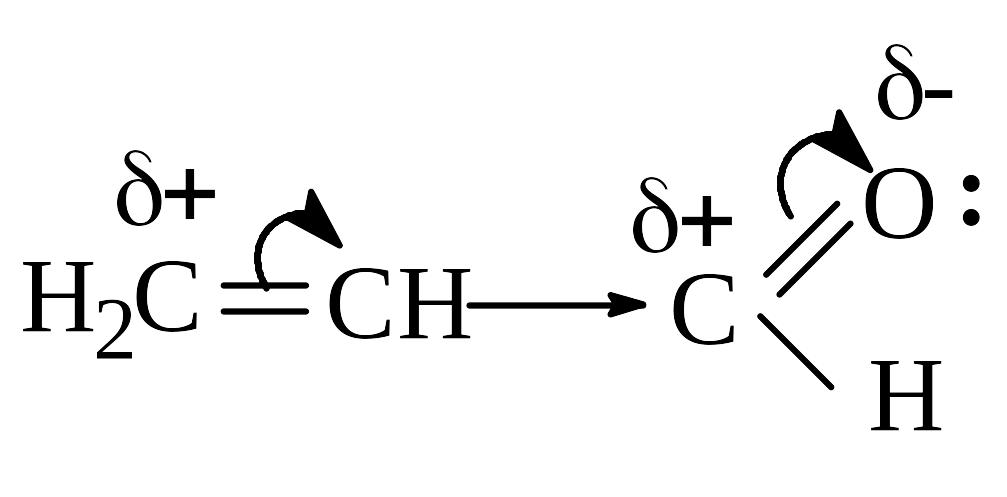
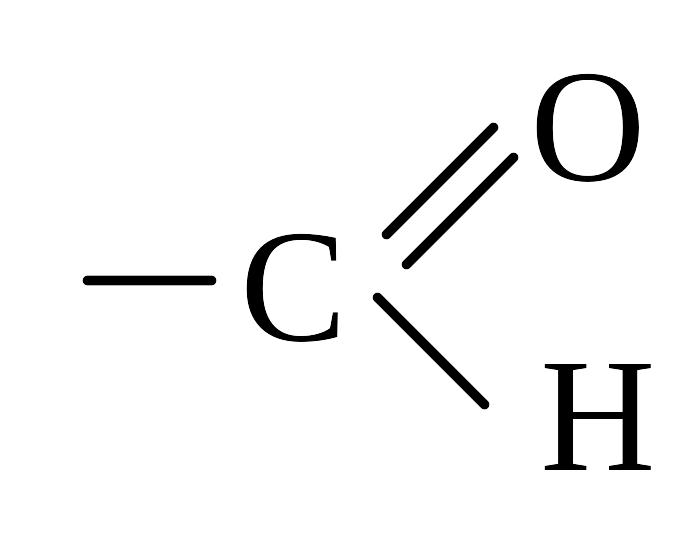
Акролеин |
Альдегидная группа проявляет – М. |
Фенол |
р, -сопряжение Гидроксильная группа –ОН проявляет +М. |
З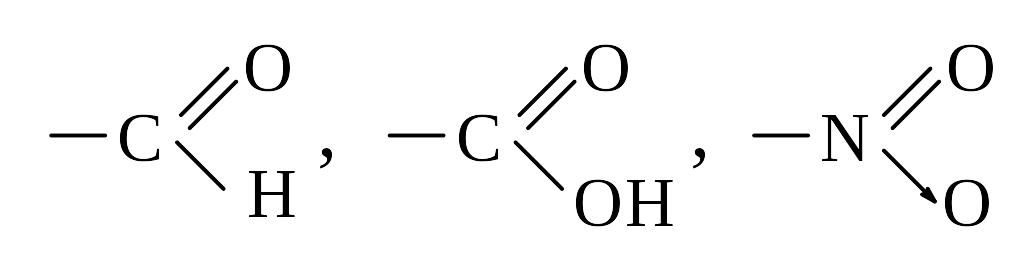 аместитель,
притягивающий электроны из сопряженной
системы, проявляет –М и наз-ся
электроноакцептором (ЭА). Это заместители,
имеющие двойную связь и др.
аместитель,
притягивающий электроны из сопряженной
системы, проявляет –М и наз-ся
электроноакцептором (ЭА). Это заместители,
имеющие двойную связь и др.
З![]() аместитель,
отдающий электроны в сопряженную
систему, проявляет +М и наз-ся
электронодонором (ЭД). Это заместители
с одинарными связями, имеющие неподеленную
электронную пару
аместитель,
отдающий электроны в сопряженную
систему, проявляет +М и наз-ся
электронодонором (ЭД). Это заместители
с одинарными связями, имеющие неподеленную
электронную пару
и др.
Таблица 1 Электронные эффекты заместителей
Заместители |
Ориентанты в С6Н5-R |
I |
М |
Аlk (R-): СН3-, С2Н5-... |
Ориентанты I рода: направляют ЭД заместители в орто- и пара- положения |
+ |
|
– |
– |
+ |
|
– |
– |
+ |
|
–Н |
– |
+ |
|
ЭА |
Ориентанты II рода: направляют заместители в мета- положения |
– |
– |
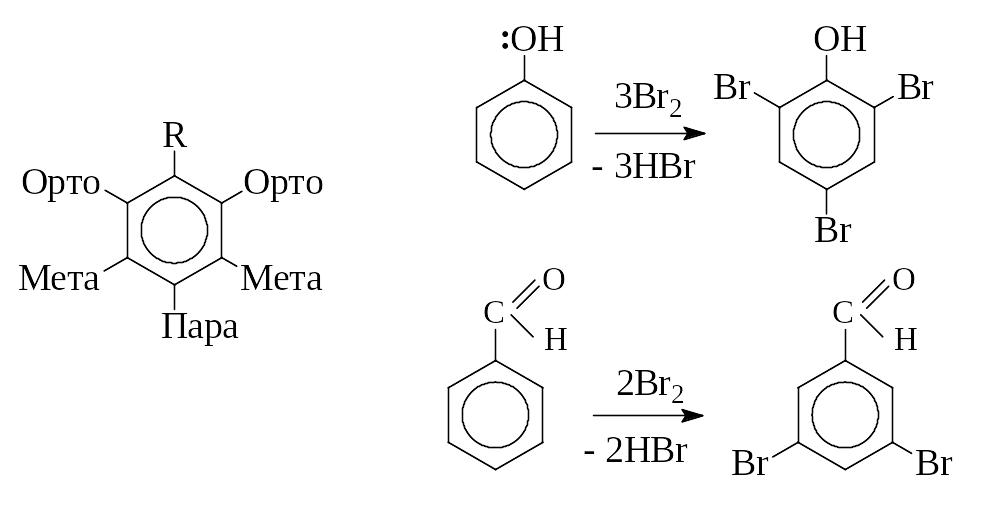
Примеры:


 ,
- сопряжение
,
- сопряжение