
- •Курс лекций по дисциплине «Химия»
- •Омск- 2006 г. Оглавление
- •Периодическое изменение свойств атомов химических элементов
- •Общие представления о химической связи.
- •Характеристики химической связи.
- •Природа химической связи.
- •Типы связей.
- •Метод валентных связей
- •Понятие о методе молекулярных орбиталей
- •Первый закон термодинамики
- •Первое начало термодинамики
- •Энтальпия. Закон Гесса.
- •Тепловые эффекты химических реакций
- •Скорость химической реакции
- •Закон действующих масс.
- •Энергия активации химической реакции
- •Зависимость скорости реакции от катализатора
- •Фундаментальные постоянные
- •П.1. Наименование неорганических веществ
- •Общие понятия об электролизе.
- •Ионная теория электролиза.
- •Электролиз расплавов
- •Количественные законы электролиза.
- •Практическое значение электролиза.
Количественные законы электролиза.
В 30-х годах XIX века М. Фарадеем были установлены следующие количественные законы электролиза:
1. Масса, образующегося при электролизе вещества пропорциональна количеству прошедшего электричества.
Данный закон вытекает из сущности электролиза. Так как электролиз обеспечивается отдачей и принятием электронов, при котором происходит разложение и образование веществ, то его количество всегда будет пропорционально числу прошедших по цепи электронов.
2. При электролизе различных химических соединений равные количества электричества приводят к электрохимическому превращению эквивалентных количеств веществ.
Возникает естественный вопрос – почему при электролизе различных веществ, они выделяются в химически эквивалентных количествах. Это нетрудно понять, если рассмотреть электролиз с точки зрения электронной теории. Для примера рассмотрим электролиз хлорида меди(II). При выделении меди из раствора каждый ион меди получает от катода два электрона, и в то же время два хлорид-иона отдают электроны аноду, превращаясь в атомы хлора. Следовательно, число выделившихся атомов меди всегда будет вдвое меньше числа выделившихся атомов хлора, то есть массы меди и хлора будут относиться друг к другу, как их молярные массы эквивалентов.
Измерениями установлено, что количество электричества, обуславливающее электрохимическое превращение одной молярной массы эквивалентов вещества, равно 96485 кулонам.
Второй закон электролиза позволяет определить эквиваленты различных веществ.
Математическое выражение первого и второго законов электролиза имеет вид
mB = (Mэкв(В)∙I∙t)/F (10),
где I – сила тока, t – время в секундах, F – постоянная Фарадея (её округленно принимают равной 96500 К/моль), Mэкв(В) – молярная масса электрохимических эквивалентов вещества В, mB – масса разложившегося или образованного вещества.
Молярная масса электрохимических эквивалентов вещества рассчитывается как частное деления молярной массы вещества на число электронов, перемещаемых при окислении или восстановлении, то есть
Mэкв(В) = M/n (11).
Например, при окислении воды
2Н2О - 4е- = О2 + 4Н+ (12),
молярная масса эквивалента равна
Mэкв(Н2О) =18/2= 9 г/моль (13),
а при её восстановлении
2Н2О + 2е- Н2 + 2ОН- (14),
молярная масса эквивалента равна
Mэкв(Н2О) = 18/1 = 18 г/моль (15).
Практическое значение электролиза.
Электролиз применяется для решения следующих технических задач: извлечение металлов, очистка металлов, нанесение гальванических покрытий.
Извлечение металлов 1-й и 2-й групп периодической системы осуществляется с помощью электролиза из расплавленных галогенидов этих металлов. Например, натрий получают электролизом расплава хлорида натрия. Сведения о металлах, получаемые таким способом приведены в таблице 1.
Таблица 1
Электролитическое получение металлов
Металл |
Сырьё |
Электролит |
Алюминий |
Бокситная руда |
Al2O3, растворенный в расплавленном криолите |
Натрий |
Каменная соль |
NaCl |
Магний |
Доломит и морская вода |
MgCl2 |
Цинк |
ZnS – руда (цинковая обманка) |
ZnSO4 |
Очистка металлов с помощью электролиза называется рафинирование. Рассмотрим данный процесс на примере меди. Для очистки меди используют два электрода, опущенных в раствор CuSO4. На аноде находится неочищенная медь, на катоде – чистая медь. При электролизе на аноде протекает реакция
Cu(тв.) → Сu2+ (водн.) + 2е- (16).
Примеси, высвобождаемые при электрохимическом растворении неочищенной меди на аноде, опускаются на дно электролизёра, образуя анодный ил. Переходящие в раствор ионы меди разряжаются на чистом медном катоде
Cu2+(водн.) → Cu (тв) + 2е- (17).
Нанесение гальванических покрытий осуществляется на катоде, за счёт так называемого электроосаждения. Катод погружают в электролит, который содержит ионы электроосаждаемого металла. В качестве анода используется пластина, либо стержень из того металла, которым наносят покрытие (например, хром, никель).
Для нанесения покрытий также применяют анодирование. Анодирование – процесс покрытия алюминиевых предметов оксидом алюминия. В данном процессе покрываемый предмет является анодом, а в качестве электролита используется разбавленная серная кислота H2SO4.
Лекция 15. Коррозия металлов.
Химическая коррозия металлов. Газовая коррозия. Электрохимическая коррозия металлов. Электрохимическая коррозия с кислородной и водородной деполяризацией. Факторы, влияющие на скорость электрохимической коррозии. Виды электрохимической коррозии.
Общие понятия коррозии.
Коррозия – это разрушение конструкций и изделий из металлических материалов, происходящее вследствие их физико-химического взаимодействия с окружающей средой, которую называют коррозионной или агрессивной, а образовавшиеся химические соединения – продуктами коррозии. В результате коррозии металлические изделия теряют свои технические свойства, вследствие чего большое значение имеет защита металлов и сплавов от коррозии.
Коррозионные среды бывают жидкими и газообразными, токопроводящими и неэлектролитами, естественными и искусственными. К газообразным средам относятся природная атмосфера и газы, образующиеся при сгорании топлива или выделяющиеся в химических процессах на производстве. Жидкие – это жидкие электролиты и жидкие неэлектролиты. Среди жидких электролитов наиболее часто встречаются такие как, водные растворы солей, кислот, щелочей, морская вода. Жидкими неэлектролитами являются нефть, бензин, керосин. К естественным коррозионным средам относится почва и вода.
Причина коррозии металлов и сплавов заключается в их термодинамической неустойчивости. Коррозионные процессы протекают самопроизвольно и сопровождаются убылью энергии Гиббса
∆G < 0 (1).
Чем меньше значение ∆G коррозионного процесса, тем выше вероятность его протекания.
Химическая коррозия металлов. Газовая коррозия.
По механизму процесса, коррозию подразделяют на химическую и электрохимическую. Химическая коррозия характерна для сред, не проводящих электрический ток. В зависимости от вида среды различают химическую коррозию в жидких неэлектролитах и химическую газовую коррозию. При такой коррозии не возникает электрического тока. Она протекает по механизму гетерогенных окислительно-восстановительных реакций.
Жидкие неэлектролиты малоагрессивны в чистом виде, но в них обычно присутствуют примеси. Даже небольшие количества примесей резко увеличивает агрессивную активность таких сред. Например, сероводород H2S, содержащийся в сырой нефти, вызывает коррозию железа, меди, никеля, серебра, олова, свинца.
Газовая коррозия происходит при взаимодействии металлов с газами. Она происходит при повышенных температурах, когда конденсация влаги на поверхности металла невозможна. Газовой коррозии подвергаются сопла ракетных двигателей, арматура печей, детали двигателей внутреннего сгорания, лопатки газовых турбин. Газовой коррозии подвергаются металлы при их термической обработке.
К газовым агрессивным агентам относятся O2, CO2, SO2, H2O, H2S, Cl2. Они имеют не одинаковую агрессивность по отношению к металлам. Скорость окисления возрастает в ряду H2O → CO2 → O2 → SO2 (при температуре 900 0С для железа, кобальта, никеля). Причем в атмосфере этих газов скорость коррозии убывает в ряду Fe → Co → Ni. Уравнения для этих процессов окисления имеют вид
Fe + H2O → FeO + H2 (2)
Fe + CO2 → FeO + CO (3)
Fe + H2O + SO2 → FeSO3 + H2 (4)
2Fe + O2 → 2FeO (5)
3Fe + SO2 → 2FeO + FeS (6).
Механизм газовой коррозии обусловлен протеканием на поверхности раздела твердой и газовой фаз двух сопряженных реакций. Одна из них это окисление металла, другая – восстановление газообразного окислителя, причем в пространстве данные процессы не разделены. В этом же месте накапливаются продукты реакции окисления. В процессе образования продуктов коррозии атомы и ионы металла, с одной стороны, и атомы или ионы кислорода с другой, диффундируют сквозь постепенно утолщающуюся пленку продуктов коррозии. В результате этого на поверхности металла образуются соответствующие соединения, например, оксиды, сульфиды.
Газовой коррозии подвергаются, стали, чугуны, железо, которые взаимодействуют с кислородом. Они теряют прочность и твердость, особенно при температурах выше 300 0С. При этом образуются продукты в соответствии с реакцией
Fe + O2 → FeO + Fe3O4 + Fe2O3 (7).
Образующаяся смесь продуктов называется окалиной. Одновременно с этим происходит обезуглероживание металлов
Fe3C + O2 → Fe + CO2 (8).
Обезуглероживание происходит и в атмосфере водорода
Fe3C + 2H2 → 3Fe + CH4↑ (9).
Иногда этот вид газовой коррозии называют водородной. Наряду с обезуглероживанием одновременно осуществляется и наводороживание, которое заключается в проникновении атомарного водорода в материал и последующее его растворение в нем, что приводит к заметному снижению пластичности материала. Данное явление иногда называют водородное охрупчивание.
Термодинамический анализ показывает, что давление кислорода играет определяющую роль для существования коррозии и образования оксидной пленки. Чтобы исключить возможность протекания коррозии, требуется обеспечить очень низкие парциальные давления кислорода, которые невозможно создать в реальных условиях. Поэтому для предотвращения коррозии используют обескислороженную атмосферу.
Рост толщины оксидной пленки может происходить в направлении металла и газовой среды, либо в обоих направлениях одновременно, либо преимущественно в одном из них. Если рост осуществляется в направлении газовой среды, то наблюдается существенное увеличение размера детали, например, при оксидировании.
Направление роста оксидной пленки определяется соотношением между скоростями процессов встречной диффузии ионов металла MZ+ и кислорода О2- внутри пленки. Если скорости диффузии ионов металла и кислорода различаются, то рост оксидной пленки происходит преимущественно в одном направлении. Если коэффициент диффузии ионов кислорода меньше коэффициента диффузии ионов металла, то рост оксидной пленки будет происходить в направлении газовой среды. Если коэффициент диффузии ионов кислорода будет больше коэффициента диффузии ионом металла, то рост оксидной пленки будет происходит в сторону металла.
В большинстве случаев, скорости диффузии ионов металла и ионов кислорода практически одинаковы. По мере утолщения оксидной пленки процессы встречной диффузии ионов и электронов затрудняются при этом рост пленки прекращается.
Оксидные пленки толщиной до 40 нм оптически прозрачны и невидимы. Достигая толщины 40 – 500 нм, становятся видимыми. Они приобретают цвета побежалости: красный, оранжевый, желтый, зеленый, голубой, синий, фиолетовый. Цвет образуется на поверхности металла за счет интерференции в них световых лучей. Цвет пленки определяется её толщиной.
Если оксидная пленка препятствует дальнейшему проникновению коррозионной среды к поверхности металла, то её называют защитной. Металл с защитной пленкой на поверхности становится химически неактивным. Это объясняется тем, что начальная стадия образования защитной пленки – исключительно химический процесс. Дальнейшее протекание процесса роста определяется скоростью встречной диффузии ионов металла и кислорода внутри пленки. В защитных пленках определенной толщины и совершенством структуры, когда отсутствуют трещины, поры, вакансии, процессы встречной диффузии прекращаются. Чтобы обладать защитными свойствами, оксидная пленка должна быть сплошной, непористой, химически инертной к агрессивной среде, иметь высокую твердость, износостойкость и близкий к металлу коэффициент термического расширения.
Электрохимическая коррозия металлов. Виды электрохимической коррозии. Электрохимическая коррозия с кислородной и водородной деполяризацией
Электрохимическая коррозия сопровождается возникновением электрического тока и протекает в средах с хорошей ионной проводимостью. К электрохимической коррозии относится коррозия в водных растворах. Электрохимической коррозии подвергаются подводные части судов, паровые котлы, проложенные в земле трубопроводы. К электрохимической коррозии относится: коррозия в электролитах, атмосферная коррозия, электрокоррозия, коррозия под напряжением.
В результате электрохимической коррозии окисление металлов может приводить как к образованию нерастворимых продуктов (ржавчины), так и к переходу металла в раствор в виде ионов.
Растворенный кислород, ионы водорода, молекулы воды – это важнейшие окислители, вызывающие электрохимическую коррозию металлов.
Все металлы делят на пять групп по степени термодинамической устойчивости. Такое деление соответствует их положению в ряду напряжений.
К группе повышенной термодинамической нестабильности относятся металлы, имеющие значение стандартного электродного потенциала меньше, чем потенциал водородного электрода при рН = 7 (-0,413 В), а именно Li, Rb, Cs, Ba, Sr, Ca, Na, Mg, Al, Ti, Zr, Mn, Cr, Zn, Fe. Данные металлы могут коррозировать даже в нейтральных средах, то есть могут окисляться водой. Естественно эти металлы коррозируют и в кислых средах. Металлы могут окисляться кислотой, кислородом, а также под действием других окислителей, при этом протекает процесс, описываемый уравнением
M – ne- = Mne+ (10).
Процесс электрохимической коррозии – это совокупность двух процессов, одновременно протекающих на поверхности металла:
-анодного, сопровождающегося окислением атомов металла, протекающего по уравнению (10);
- катодного, сопровождающегося восстановлением окислителя коррозионной среды, протекающего по уравнению
Окисленная форма + ne- = Восстановленная форма (11).
Окислители электрохимической коррозии называют деполяризаторами. Приведем возможные процессы восстановления окислителей:
2Н2О + 2е- = 2ОН- + Н2 , φ = -0,413 В (рН = 7) (12)
2Н+ + 2е- = Н2, φ = 0 В (рН = 0) (13)
О2 + 2Н2О + 4е- = 4ОН-, φ = 0,816 В (рН = 7) (14)
О2 + 4Н+ + 4е- = 2Н2О, φ = 1,229 В (рН = 0) (15).
Коррозию, сопровождающуюся восстановлением (ионизацией) молекул кислорода (14), (15), называют коррозией с поглощением кислорода или коррозией с кислородной деполяризацией. С кислородной деполяризацией протекают следующие виды электрохимической коррозии: атмосферная, подземная, в пресной и морской воде, в растворах солей, в аэрированных растворах органических кислот.
Коррозию, сопровождающуюся восстановлением молекул воды и ионов водорода (12), (13), называют коррозией с выделением водорода или коррозией с водородной деполяризацией.
Металлы термодинамически нестабильные имеют значения стандартных электродных потенциалов больше, чем металлы группы повышенной термодинамической нестабильности, но не выше нуля. К этой группе относятся металлы: Cd, In, Tl, Co, Ni, Mo, Pb, W. Эти металлы не окисляются водой при рН = 7, но окисляются в кислых средах и в любых средах в присутствии кислорода.
Группа металлов промежуточной термодинамической стабильности: Bi, Sb, Re, Tc, Cu, Ag, Rh. Данные металлы имеют положительные значения стандартных электродных потенциалов, но не превышающие значения электродного потенциала, связанного с окисляющим действием кислорода в нейтральной среде (14). Эти металлы будут устойчивы в любых кислых и нейтральных средах в отсутствие кислорода.
Металлы высокой стабильности устойчивы во влажной атмосфере, то есть в присутствии кислорода в нейтральной среде. К данным металлам относятся Hg, Pd, Ir, Pt. Стандартные электродные потенциалы этих металлов находятся в интервале между значениями двух электродных потенциалов, характеризующих окисляющее действие кислорода в нейтральной и кислой средах, то есть от 0,816 В до 1,229 В.
Металлом полной стабильности является золото. Оно не может окисляться рассмотренными выше окислителями и у него максимальный электродный потенциал.
Чтобы получить уравнения реакций, лежащих в основе электрохимической коррозии металлов в различных средах, которые называются коррозионные токообразующие реакции, суммируют (10) поочередно с (12) – (15). Если уравнять число отданных и принятых электронов, то получим следующие уравнения
4M + nO2 + 2nH2O → 4M(OH)n (16)
4M + nO2 + 4nH+ → 4Mn+ + 2nH2O (17)
2M + 2nH2O → 2M(OH)n + nH2↑ (18)
2M + 2 nH+ → 2Mn+ + nH2↑ (19).
Причинами возникновения электрохимической коррозии служат различные виды неоднородностей как самой поверхности металла или сплава, так и коррозионной среды. В результате вся поверхность, соприкасающаяся с токопроводящей коррозионной средой, разделяется на катодные и анодные участки, которые имеют очень маленькие размеры и чередуются друг с другом. В такой среде они представляют собой совокупность огромного числа короткозамкнутых коррозионных гальванических микроэлементов. Коррозия осуществляется в результате протекания анодного процесса или коррозионного окисления металла и катодного процесса или восстановления окислителя, находящегося во влажной среде.
Рассмотрим различные случаи возникновения коррозионных гальванических пар.
1. Контакт с электролитом двух разных металлов в случае сочетания в одном узле или детали металлов различной активности в данной среде, или в случае применения сплава эвтектического типа из двух металлов разной активности,
Контакт металла и его соединения, обладающего металлообразными или полупроводниковыми свойствами. В любом случае свободный металл имеет отрицательный электрический заряд, а соединение — положительный заряд, так как в нем часть электронов проводимости связана. Это также справедливо и для интерметаллидов.
Различные концентрации электролитов или воздуха, растворенного в жидком электролите.
Различный уровень механических напряжений в одной и той же детали.
Механизм электрохимической коррозии, определяемый разностью потенциалов пассивных (катодных) и активных (анодных) участков, сводится к работе гальванического элемента, однако результат коррозионных разрушений может быть различен.
На механизм низкотемпературной коррозии влияет много различных причин: переменная температура и влажность воздуха, переменный состав газовой и электролитной среды и даже бактериальная флора, например при почвенной коррозии, так как некоторые виды бактерий способствуют окислению железа. Развитие коррозии в результате контакта разных металлов можно иллюстрировать схемой, представленной на рис. 1. Наибольшее коррозионное разрушение наблюдается рядом с контактом, так как здесь сопротивление наименьшее и, следовательно, наибольшая плотность тока.

Рис. 1. Разрушение в месте контакта разных металлов
Если возникновение разности потенциалов вызвано применением эвтектических сплавов, состоящих из металлов различной активности, то не всегда можно руководствоваться данными по стандартным потенциалам растворения, так как активность изменяется в зависимости от состава электролита и рН среды.
Так, например, стандартный потенциал алюминия меньше стандартного потенциала цинка, а в растворе поваренной соли получается наоборот — εА1 > εZn и в данной паре цинк будет анодом. При контакте эвтектического сплава с электролитом может быть два случая:
1) коррозия сведется к вытравливанию из поверхностного слоя одного из компонентов (селективная коррозия);
2) коррозия может перейти в интеркристаллитную, если наиболее активный элемент входит только в состав эвтектики, разделяющей кристаллические зерна металлов. В сплавах металлов А и В, обладающих разной активностью (Sa<Sb), сплав состава 1—1 будет подвергаться селективной коррозии, а сплав состава 2—2 — интеркристаллитной, потому что активный металл А весь входит в состав.
Ввиду малой поверхности зерен А в эвтектике плотность тока будет большая и разрушение эвтектики пойдет в глубину. Поэтому рекомендуется в коррозионных средах применять только сплавы типа твердого раствора (JI-61, IX18H10).
Различные концентрации электролита могут вызвать коррозию, создавая гальваническую пару даже с одинаковыми металлами. Различное содержание кислорода также приводит к образованию гальванической пары — менее окисленный и более окисленный металл. Примером может служить коррозия металла под каплей воды (точечная коррозия, переходящая в питтинг): схема этого процесса приведена на рис. 2. Поверхностные слои воды содержат больше кислорода, чем внутренние, и поэтому средняя часть смоченного металла оказывается более активной (анод), чем внешняя (катод). После высыхания капли в ее центре появляется довольно глубокое пятно ржавчины. Если взять достаточно тонкую (0,2—0,1 мм) пластинку, например, стали, то можно получить сквозное отверстие. Такие процессы часто наблюдаются при атмосферной и почвенной коррозии.
Коррозионные пары могут возникать при действии внешних или внутренних механических напряжений. Такая коррозия встречается при сварке и происходит под действием остаточных напряжений. Если пластинку стали, дюраля или титанового сплава согнуть и в напряженном состоянии погрузить в коррозионную среду, то на растянутом слое (внешнем) через относительно короткое время возникнут трещины, а внутренний сжатый слой будет оставаться без изменений. Растягивающие усилия особенно опасны, так как в этом случае металл повышает свою активность.
Если согнутую упруго пластинку термически обработать и упругие деформации перейдут в пластические, то разности потенциалов нe возникает. Таким образом, при изготовлении деталей и узлов машин для снятия остаточных напряжений всегда следует термически обрабатывать изделия, если эти изделия предназначены для работы в сильно коррозионных средах.

Рис. 2. Коррозия стали под неподвижной каплей воды
Эксплуатация деталей и узлов машин в коррозионной среде под действием наложенной разности потенциалов встречается редко. Обычно такой вид коррозии имеет место в случае случайного возникновения разности потенциалов за счет нарушения изоляции и утечки тока из соседних электрических линий. Эти случайно наложенные разности потенциалов могут приводить к опасным коррозионным разрушениям. Очень часто возникновение падения в почвах создается за счет электрического рельсового транспорта.
Рассмотрим коррозионное разрушение закладных металлических конструкций (трубы, детали фундаментов, кабель) под действием утечки тока, например, с трамвайного рельсового пути, который заглублен в грунт и может иметь высокое электрическое сопротивление за счет стыков рельс, которые плохо проводят электрический ток. Такой вид коррозии называется коррозия за счет блуждающих токов. В этом случае при хорошо проводящей влажной почве возможно разветвление тока, причем часть его пойдет через почву кратчайшим путем.
На пути так называемого «блуждающего» тока может находиться металлическое сооружение — плохо изолированная труба. Примем условно, что электролит, пропитывающий почву, содержит ионыС1-, Fe3+ и Na+. Электроны, выходящие из металла (рельса), по электролиту перемещаться не могут и в месте выхода их из рельса разряжают ионы Н+ или Fe3+. Ионы хлора будут перемещаться по почве, подходить к трубе и, разряжаясь, переводить металл в раствор. На выходе электронов из металла (трубы) не будет коррозии, тогда как на входе в рельс ионы хлора будут вызывать коррозию. Аналогичные явления могут наблюдаться и при переменном токе, но они менее опасны.
Тщательное соблюдение требований к электрической изоляции (битум, полиэтилен) закладных изделий и правильной эксплуатации электрических сетей может исключить электрокоррозию.
Лекция 16. Защита металлов от коррозии.
Методы защиты металлов от коррозии. Защитные покрытия: металлические (анодные, катодные) и неметаллические. Электрохимическая защита: протекторная, катодная, анодная. Химические покрытия.
Методы защиты металлов от коррозии.
Защита от коррозии – это комплекс мероприятий, направленных на предотвращение и замедление коррозионных процессов, сохранение и поддержание работоспособности узлов и агрегатов машин, оборудования и сооружений. Выделяют следующие способы защиты от коррозии: методы воздействия на металл и саму конструкцию (легирование, обработка поверхности, нанесение защитных покрытий, рациональное конструирование), методы воздействия на коррозионную среду и условия эксплуатации (ингибирование, обработка среды, электрохимическая защита, герметизация, осушка воздуха, создание искусственной атмосферы), а также комбинированные методы.
Способы защиты от коррозии выбирают на стадии конструирования и осуществляют в процессе изготовления и эксплуатации объектов.
Рациональное конструирование изделий включает учет следующих факторов:
- правильный выбор материалов для изделий и конструкций, которые должны быть стойкими в данной коррозионной среде, не способны впитывать влагу, не выделять коррозионно-активных агентов в процессе эксплуатации;
- рациональное сочетание и компоновка в одном узле деталей, изготовленных из металлов, отличающихся значениями электродных потенциалов, которое достигается предотвращением их непосредственного контакта друг с другом и с коррозионной средой, путем изоляции соприкасающихся материалов, применения прокладок, уплотнительных мастик и герметиков;
- оптимальная форма деталей и изделий, включающих дренажные отверстия и проветриваемые полости, минимум коррозионно-опасных мест: углублений, пазов, щелей, канавок, зазоров, застойных зон;
- минимальная слитность сечения, то есть отношения периметра сечения к его площади, характеризующая поверхность соприкосновения конструкций с коррозионной средой;
- характер соединения элементов в сборке (сварные соединения предпочтительнее клепанных и болтовых), так как они приводят к возникновению больших внутренних напряжений и пор;
- возможность нанесения и возобновления различных покрытий в процессе эксплуатации.
Легирование металлов – способ повышения их стойкости к воздействию агрессивных сред. В данном методе в металл или сплав вводят добавки, которые вызывают их пассивацию.
Изменение состава и свойств коррозионной среды, с целью уменьшения её агрессивности, осуществляют либо введением в неё специальных веществ – ингибиторов коррозии, либо соответствующей её обработкой. Ингибиторами называют химические соединения, введение которых в небольших количествах в коррозионную среду резко снижает скорость коррозии. По химическому составу различают органические и неорганические ингибиторы. По условиям применения различают жидкофазные ингибиторы для растворов и летучие ингибиторы, которые дают защитный эффект в условиях атмосферной коррозии. По механизму действия различают катодные, анодные и экранирующие ингибиторы.
Механизм защитного действия ингибиторов заключается в адсорбции их на поверхности и последующем торможении анодных (анодные ингибиторы), катодных (катодные ингибиторы) процессов электрохимической коррозии, а также в образовании защитных и пассивирующих пленок. Анодные ингибиторы – это неорганические соединения, обладающие окислительными свойствами. Такими свойствами обладают хроматы, нитриты, молибдаты. Они восстанавливаются на катодных участках поверхности, обеспечивающих пассивацию анодных участков с образованием на них защитных пленок из оксидов или малорастворимых солей.
Катодные ингибиторы по защитному действию менее эффективны, чем анодные. Они тормозят протекание катодных процессов. Это достигается:
- путем уменьшения концентрации растворенного кислорода посредством связывания его в химическое соединение (в случае коррозии с кислородной деполяризацией);
- за счет повышения перенапряжения катодного выделения водорода добавлением в растворы определенных солей (при коррозии с водородной деполяризацией);
- за счет уменьшения площади катодных участков посредством экранирования.
Анодные и катодные ингибиторы оказывают защитное действие только в нейтральных и щелочных растворах. В сильнокислотных растворах используют экранирующие ингибиторы. В качестве экранирующих ингибиторов используются органические соединения, содержащие в своем составе атомы серы, кислорода, азота (альдегиды, фенолы, меркаптаны, амины, соли ароматических карбоновых кислот). За счет того, что они имеют полярные группы или неподелённые электронные пары у атомов O, S, N, одни из них затрудняют протекание катодной реакции, другие анодной.
Ингибиторы атмосферной коррозии подразделяют на нелетучие – контактные и летучие – парофазные. Нелетучие ингибиторы применяют при хранении изделий на складе. Их наносят на поверхность изделий или на его упаковку. Летучие ингибиторы используют для защиты, как в сухой, так и во влажной атмосфере. Обычно это нетоксичные вещества, с невысоким давлением паров при обычных температурах. Испаряясь, они заполняют окружающую воздушную среду. Пары адсорбируются на поверхности металла и образуют пленки с анодным и катодным механизмами защитного действия. К летучим ингибиторам относятся нитриты и карбонаты замещенных аминов, а также сложные эфиры карбоновых кислот.
Практическое использование ингибитора определяется его эффективностью, токсичностью и ущербом, наносимым окружающей среде.
Для защиты металлоизделий от атмосферной коррозии используют ингибированные смазки – нефтяные масла, воск, вазелин, ланолин.
Электрохимическая защита: протекторная, катодная, анодная.
Электрохимическая защита основана на снижении скорости коррозии торможением анодных или катодных реакций посредством поляризации защищаемой конструкции постоянным током. В зависимости от вида поляризации (изменения потенциала) различают катодную и анодную защиты.
В основе катодной защиты лежит катодная поляризация, то есть смещение потенциала защищаемого металла в отрицательную сторону. Такую поляризацию можно осуществить двумя способами:
- подключением металла защищаемой конструкции к отрицательному полюсу внешнего источника постоянного тока; такую защиту называют иногда защитой внешним (наложенным) потенциалом;
- присоединением к металлу защищаемой конструкции жертвенного электрода (анода или протектора), материал которого имеет меньший электродный потенциал, чем у металла защищаемой конструкции; такую катодную защиту иногда называют протекторной (гальванической) защитой или защитой жертвенным анодом.
При протекторной защите жертвенный анод растворяется, поэтому его необходимо время от времени заменять на новый. В качестве материалов используют магний и его сплавы, реже – алюминий и цинк. В воде и грунте алюминий и цинк склонны к образованию на поверхности плотных оксидных пленок, которые нарушают токоотдачу. Для их растворения в засыпку вводят хлориды или другие компоненты. Это приводит, с одной стороны, к уменьшению скорости растворения протектора (жертвенного электрода), но с другой к сокращению радиуса защитного действия. Достоинством протекторной защиты является отсутствие необходимости во внешнем источнике постоянного тока.
Катодную защиту широко используют для борьбы с коррозией трубопроводов, кабельных установок и металлоконструкций в морской и речной воде, грунте.
Основой анодной защиты является анодная поляризация. Анодная поляризация – это смещение потенциала металла защищаемой конструкции в положительную сторону. Её осуществляют присоединением защищаемой конструкции к положительному полюсу внешнего источника постоянного тока, а вспомогательного электрода – к отрицательному. При этом конструкция является анодом, а вспомогательный электрод – катодом.
При анодной защите ток противоположен по направлению току при катодной защите. Достоинства анодной защиты: высокая рассеивающая способность – возможность защиты на большом удалении от катода, гораздо большем, чем в случае катодной защиты; невысокая защитная плотность тока, то есть небольшое электропотребление. Недостатками являются ограниченность области применения, так как анодная защита не осуществима для магния, кадмия, серебра, меди и медных сплавов.
Защитные покрытия: металлические (анодные, катодные) и неметаллические. Химические покрытия.
Защитные покрытия предохраняют изделия от коррозии и одновременно придают поверхности ценные свойства, такие как паяемость, отражательная способность, изностойкость. Защитные покрытия подразделяют на металлические и неметаллические
По механизму защитного действия металлические защитные покрытия подразделяют на катодные (коррозионно-стойкие) и анодные (протекторные). Металлы катодных покрытий имеют более положительные значения электродных потенциалов, чем значение потенциала металла, на который они нанесены. Например, серебряное (φ0 = 0,779 В) или никелевое (φ0 = -0,250 В) покрытие на железе (φ0 = -0,440 В). Такие покрытия защищают поверхность изделия лишь механически, поэтому основным требованием, предъявляемым к ним, является герметичность. В случае нарушения герметичности происходит разрушение металла с повышенной скоростью коррозии, вследствие возникновения и функционирования коррозионного гальванического элемента, в котором покрытие выступает в качестве катода.
Металлы анодных покрытий имеют более отрицательные значения потенциалов, чем потенциал металла, на который они нанесены. Поэтому цинковое (φ0 = -0,763 В) или алюминиевое (φ0 = -1,662 В) покрытие на железе (φ0 = -0,440 В) является анодным. Анодное покрытие защищает изделие не только механически, но и электрохимически. Это означает, что при повреждении покрытия, оно будет играть роль анода в образующемся в коррозионной среде гальваническом элементе и, следовательно, данное покрытие разрушаться не будет. Поэтому требование герметичности для анодных покрытий не существенно. Подвергаясь растворению в процессе эксплуатации изделия, анодное покрытие генерирует контактный ток, который, протекая между ним и изделием, катодно поляризует последнее, то есть смещает потенциал защищаемого металла в сторону меньших значений. Таким образом, поведение изделия с анодным покрытием аналогично механизму катодной защиты протектором. Поэтому анодное покрытие иногда называют протекторным.
Органические защитные слои. При консервации изделий применяется смазка неокисляющимися маслами (углеводороды, устойчивые к окислению). Масла наносятся при повышенной температуре (для улучшения смачивания, понижения вязкости). Застывая, образуется слой, защищающий металл от электролитной среды и воздуха. Особенно устойчива такая защита при добавлении в состав смазок ингибиторов. Неудобство консервирования смазкой состоит в необходимости удаления масла с поверхности металла при последующих операциях.
Лакирование— нанесение высокомолекулярных соединений, растворенных в летучем растворителе, на поверхность металла. После испарения растворителя на металле остается полимерный слой, не пропускающий окислитель и обладающий электроизоляционными свойствами. Лаки изготавливают из естественных смол (шеллак) или из синтетических полимеров (фенолальдегидные, глифталевые, силиконовые). При испарении растворителя могут образоваться поры в лаковом покрытии, и поэтому чаще всего употребляются многослойные покрытия, вероятность образования сквозных пор в которых значительно меньше.
Окраска металлических поверхностей сопровождается образованием полимера непосредственно на поверхности металла в процессе нанесения краски и ее отвердевании. Масляная краска представляет собой смесь частично окисленного масла (олифа) и пигмента-красителя. При нанесении краски тонким слоем на зачищенную до блеска поверхность металла, масло быстро окисляется кислородом воздуха и затвердевает, образуя на поверхности металла плотную пленку, которая и защищает металл от коррозии.
Нанесение полимеров на металл создает защитные слои с особыми свойствами (изолирующие, декоративные). Например, нанесение слоя резины на поверхность стали для изготовления различной химической аппаратуры. В настоящее время выпускается заводами готовая сталь с нанесенным полимерным слоем, которая является химически коррозионно-стойкой.
Защитные слои возможны с помощью оксидирования металлов. Оксидирование металлов сводится к созданию на поверхности металла слоя оксида, через который диффузия кислорода была бы ничтожно малой. Известны следующие методы нанесения оксидных слоев: термические, химические, электрохимические.
Электрохимическое оксидирование использует окислительные процессы на аноде электролизера. Обезжиренные и освобожденные от оксидных пленок изделия помещают на анод электролизера с окисляющим электролитом (SO 42-, Сr2О 7, СrО42-) и через очень короткое время изделие покрывается плотной оксидной пленкой:
на аноде: SO42- + H2O -2e →SO42- +2H+ +O
на катоде: Ме +О → МеО.
Фосфатирование металлической поверхности представляет собой процесс осаждения нерастворимых фосфатов этого металла. Сущность процесса фосфатирования сводится к усреднению дигидрофосфатов до фосфатов, нерастворимых в воде, за счет растворения поверхности металла:
Fe (Н2РО4)2 + 2Fc2+ → Fe3 (РО4}2 + 4Н+.
Нерастворимые фосфаты в виде мелких кристаллов прочно связаны с поверхностью металла. Однако покрытие получается пористое и может быть использовано как грунт для нанесения лакокрасочных покрытий, что широко используется в машиностроении и приборостроении.
Металлические защитные покрытия. Методы нанесения металлических защитных слоев на поверхность металлов весьма разнообразны, и их можно разделить условно на «горячие» или высокотемпературные и электрохимические.
Высокотемпературные методы. Метод окунания. Он применим для нанесения покрытий из легкоплавких металлов на более тугоплавкие. Так покрывают стальные листы оловом, цинком или свинцом. Сущность метода сводится к тому, что в расплавленный металл, из которого хотят приготовить покрытие, через слой флюса, закрывающий поверхность жидкого металла, погружают стальной лист и вынимают его также через слой флюса или масла для того, чтобы поверхность сразу не окислилась. Схема такого процесса показана на рис. 1. Цинк и олово в жидком состоянии хорошо смачивают поверхность стали. Для покрытия стали свинцом необходимо добавлять к нему некоторое количество олова, гак как свинец плохо смачивает стальную поверхность. Цинк, смачивая поверхность железа, взаимодействует с ним, образуя интерметаллиды (FeZп3, FeZn7), обладающие значительной хрупкостью. Поэтому процесс ведут быстро, с тем чтобы слой интерметаллидов был максимально тонким и не вызвал хрупкости всего защитного слоя. Олово растворяет железо с образованием твердого раствора, и интерметаллида FeSn2 обычно не образуется. Оловянный слой на луженом железе очень пластичен, так же как и свинцовый. Оценивая свойства луженого и оцинкованного железа, следует раздельно рассматривать механические

Рис. 1. Нанесение металлических покрытий окунанием.
свойства покрытия и его физико-химические свойства. Цинк по отношению к железу, представляет собой анод, и будет разрушаться в первую очередь сам, защищая железо от растворения, в то время как олово будет по отношению к железу катодом и повреждение покрытия вызовет усиленную коррозию железа.
Однако из этого не следует, что всегда оцинкованное железо лучше луженого, так как при этом получаются разные механические свойства нанесенного покрытия. В процессе цинкования между железом и цинком образуются хрупкие прослойки интерметаллидов, которые могут при перегибе листа дать трещины, приводящие к отслаиванию покрытия и его повреждению. При лужении железа слой олова получается пластичным, покрытие оказывается более прочным и выносит многократные перегибы листа без повреждения слоя.
Металлизация—это нанесение металлических покрытий на поверхность изделия распылением жидкого металла. Проволока металла, который наносится в качестве защитного слоя, подается в ацетиленокислородное пламя, в дуговой или плазменный разряд, при этом металл плавится и частично испаряется. Мельчайшие капли и пары металла струей газа транспортируются на поверхность изделия и соприкасаясь с ней, кристаллизуются. Поверхность изделия должна быть, тщательно очищена, так как иначе не будет прочного сцепления нанесенного слоя с металлом изделия.
Защитные слои можно создавать также вакуумным испарением. Покрытия, наносимые этим способом, не только защищают металл от коррозии, но и упрочняют его поверхность. Этот метод используют в ремонтно-восстановительных работах для наращивания изношенного слоя металла.
Плакирование— нанесение пленок защитного металла путем совместного проката. Метод приемлем только для листов и некоторых профилей проката (пруток, угольник).
Этот способ нанесения покрытий очень удобен, но при изготовлении из плакированного металла изделий встречаются технологические трудности. Сейчас наша промышленность выпускает дюраль и АМг-6, плакированные чистым алюминием, что значительно повышает коррозионную стойкость этих материалов. Выпускается также сталь, плакированная нержавеющей сталью (Х18Н10) и другие аналогичные материалы.
Электрохимические методы нанесения металлических покрытий основаны на электролизе. Металлические защитные слои в этом случае осаждаются на поверхности изделия, которое в электролизере представляет собой катод и находится под отрицательным потенциалом. Покрытие должно иметь мелкокристаллическую структуру и быть сплошным — без пор и трещин. Разработаны определенные режимы осаждения, обеспечивающие эти качества покрытий: температура, плотность тока и состав электролита. Для получения мелкозернистой структуры в состав электролита вводят поверхностно-активные вещества и органические добавки, препятствующие росту отдельных кристаллических зерен (например, декстрин, ализариновое масло).
Лекция 17. Конструкционные и электротехнические материалы.
Конструкционные материалы на основе легких и тяжелых металлов. Свойства конструкционных материалов, применяемых в технике. Электротехнические материалы: полупроводники, диэлектрики, проводники, сверхпроводники.
Конструкционные материалы на основе легких и тяжелых металлов. Свойства конструкционных материалов, применяемых в технике.
Под материалами понимают вещества, идущие на изготовление чего-либо или используемые при эксплуатации других веществ. Материалы, предназначенные для изготовления деталей машин и аппаратов, приборов, технических конструкций, подвергающихся механическим нагрузкам, называются конструкционными. Среди конструкционных материалов выделяют прочные, износостойкие, упругие, легкие, коррозионно-стойкие, жаропрочные. Материалы разделяют по магнитным, электрическим и другим свойствам.
Однако основы современной технике – машины и механизмы – изготовляют в основном из металлических материалов – металлов, сплавов металлов друг с другом и с некоторыми неметаллами.
В настоящее время сплавы железа подразделяют, на углеродистые стали, чугуны, легированные стали и стали с особыми свойствами.
Углеродистые стали – это сплавы железа с углеродом. В зависимости от содержания углерода в железе и температуры, получаются различные стали, отличающиеся микроструктурой. Такие стали обладают различными кристаллическими и механическими свойствами и могут превращаться одна в другую.
Твердое железо обладает способностью растворять в себе многие элементы. В частности, растворяется в железе и углерод. Его растворимость зависит от кристаллической модификации железа и температуры. Углерод растворяется в γ-железе гораздо лучше, чем в других полиморфных модификациях железа. Раствор углерода в γ-железе термодинамически устойчив в более широком интервале температур, чем чистое γ-железо. Твердый раствор углерода в α-, β-, δ-железе называется ферритом, твердый раствор углерода γ-железе – аустенитом.
Феррит является твердым раствором внедрения углерода в объемно-центрированную кубическую решетку железа. В связи с малыми расстояниями меду атомами железа в кристаллической решетке атомы углерода вынуждены размещаться в дефектах решетки (вакансиях, дислокациях).
Аустенит представляет собой фазу внедрения атомов углерода между атомами железа в гранецентрированной кубической решетке γ-железа. Но в связи с большим значением параметра кристаллической решетки γ-железа, чем у его остальных модификаций, содержание углерода значительно больше (до 2,14 % (масс.).
Другой фазой, образуемой железом и углеродом, является карбид железа, или цементит, Fe3C. Цементит имеет сложную кристаллическую структуру, содержит 6,67 % (масс.) углерода и характеризуется высокой твердостью (близкой к твердости алмаза) и значительной хрупкостью.
Механические свойства феррита и аустенита зависят от содержания в них углерода. Однако при всех концентрациях углерода феррит и аустенит менее тверды и более пластичны, чем цементит.
Железоуглеродные сплавы, содержащие меньше 2,14 % углерода, называются сталями, а содержащие больше 2,14 % углерода – чугунами.
Наиболее совершенный промышленный способ получения стали – плавка в электрических печах. Этим способом выплавляют в настоящее время большинство сортов специальных сталей. В электрической печи легко обеспечивается быстрый подъем и точное регулирование температуры, в ней можно создавать окислительную, восстановительную или нейтральную атмосферу. Это позволяет получать сталь с наименьшим количеством вредных примесей и заданного состава с высокой точностью.
При всех процессах выплавки жидкая сталь содержит небольшое количество растворенного кислорода (до 0,1 %). При кристаллизации стали, кислород взаимодействует с растворенным углеродом, образуя оксид углерода (II). Этот газ (а также некоторые другие растворенные в жидкой стали газы), выделяется из стали в виде пузырей. Кроме того, по границам зерен стали выделяются оксиды железа и металлических примесей. Все это приводит к ухудшению механических свойств стали. На качество стали, сильно влияют содержащиеся в ней газы (кислород, водород, азот) и вредные примеси (сера, фосфор). Кислород, азот и водород снижают пластичность и способствуют, хрупкому разрушению стали. Сера придает хрупкость стали при горячей обработке давлением (красноломкость), присутствуя в ней в виде сульфидов FeS. Крайне нежелательная примесь – фосфор, который вызывает хладноломкость: хрупкость стали при пониженных температурах. Сталь обыкновенного качества содержат до 0,015 % S и 0,045 % P, высококачественные стали содержат серы не более 0,015 %, а фосфора – не более 0,025 % масс.
Для удаления из сталей кислорода её еще в процессе получения, в жидком состоянии, подвергают раскислению. Раскисление – процесс удаления из жидкого металла кислорода добавлением марганца, кремния, алюминия, титана. Эти элементы активно связывают кислород, содержащийся в стали, в виде оксидов, которые переходят в шлак. Если кислород из стали не удалять, то при деформации при высоких температурах сталь подвергается хрупкому разрушению. Марганец также связывает серу в виде MnS и способствует, таким образом, устранению красноломкости стали:
![]()
Термической обработкой стали называется изменение ее структуры, а следовательно, и свойств, достигаемое нагреванием до определенной температуры, выдерживанием при этой температуре и охлаждением с заданной скоростью. Термическая обработка стали – важнейшая операция в технологии стали. Она может очень сильно изменить свойства стали. Ей подвергают как готовые изделия, главным образом инструменты и детали машин, так и полуфабрикаты, например, отливки. Применяются различные виды термической обработки, придающие стали различные свойства. Важнейшими являются закалка и отпуск.
Закалка – это нагревание стали до температуры, несколько превышающей температуру превращения перлита в аустенит. Закалка придает, стали твердость, прочность, но в то же время делает ее хрупкой. Поэтому закаленную сталь обычно подвергают еще одной операции – отпуску. Данная операция состоит в нагревании стали до температуры, при которой еще не достигается превращение в аустенит, выдержке при этой температуре и сравнительно медленном охлаждении. Отпуск – конечная операция термической обработки. В результате закалки и отпуска сталь получает требуемые механические свойства.
Механические свойства медленно охлажденной углеродистой стали, сильно зависят от содержания в ней углерода. Медленно охлажденная сталь состоит из феррита и цементита, причем количество цементита пропорционально содержанию углерода. Твердость цементита намного выше твердости феррита. Поэтому при увеличении содержания углерода в стали, ее твердость повышается. Кроме того, частицы цементита затрудняют движение дислокаций в основной фазе – в феррите. По этой причине увеличение количества углерода снижает пластичность стали.
Легированные стали. Элементы, специально вводимые в сталь в определенных концентрациях для изменения ее свойств, называются легирующими элементами, а сталь, содержащая такие элементы, называется легированной сталью. К важнейшим легирующим элементам относятся хром, никель, марганец, кремний, ванадий, молибден.
Различные легирующие элементы по-разному изменяют структуру и свойства стали. Так, некоторые элементы образуют твердые растворы в γ-железе, устойчивые в широкой области температур. Например, твердые растворы марганца или никеля в γ-железе при значительном содержании этих элементов стабильны от комнатной температуры до температуры плавления. Сплавы железа с подобными металлами называются, поэтому аустенитными сталями или аустенитными сплавами.
Феррит – твердый раствор внедрения углерода в кристаллическую решетку полиморфной модификации α-железа, в конструкционных сталях составляет не менее 90 % по объему. Он во многом определяет свойства стали. Легирующие элементы, растворяются в феррите и упрочняют его. Особенно сильно повышают твердость феррита Si, Mn и Ni, склонные к образованию иных кристаллических решеток, чем объемно-центрированная кубическая решетка α-Fe. Слабее влияют Mo, W, Cr, изоморфные α-Fe. Наиболее ценным и дефицитным легирующим элементом является никель. Вводя никель в сталь в количестве от 1 до 5 %, добиваются уменьшения порога перехода в хрупкое состояние стали на 60-80 0С и более.
По своему назначению стали делятся на конструкционные, инструментальные и стали с особыми свойствами. Конструкционные стали применяются для изготовления деталей машин, конструкций и сооружений. В качестве конструкционных, могут использоваться как углеродистые, так и легированные стали. Конструкционные стали обладают высокой прочностью и пластичностью. В то же время они должны хорошо поддаваться обработке давлением, резанием, хорошо свариваться. Основные легирующие элементы конструкционных сталей – это хром (около 1 %), никель (1-4 %) и марганец (1-1,5 %).
Марганцовистая сталь, содержащая до 15 % Mn, обладает высокими твердостью и прочностью. Из нее изготовляют рабочие части дробильных машин, шаровых мельниц, железнодорожные рельсы.
Инструментальные стали – это углеродистые и легированные стали, обладающие высокой твердостью, прочностью и износостойкостью. Их применяют для изготовления режущих и измерительных инструментов, штампов. Необходимую твердость обеспечивает содержащийся в этих сталях углерод (в количестве от 0,8 до 1,3 %). Основной легирующий элемент инструментальных сталей – хром, иногда в них вводят также вольфрам и ванадий. Особую группу инструментальных сталей составляет быстрорежущая сталь, сохраняющая режущие свойства при больших скоростях резания, когда температура рабочей части резца повышается до 600-700 0С. Основные легирующие элементы этой стали – хром и вольфрам.
Стали с особыми свойствами. К этой группе относятся нержавеющие, жаростойкие, жаропрочные, магнитные и некоторые другие стали. Нержавеющие стали устойчивы против коррозии в атмосфере, влаге и в растворах кислот, жаростойкие – в коррозийно-активных средах при высоких температурах. Жаростойкие стали сохраняют высокие механические свойства при нагревании до значительных температур, что важно при изготовлении лопаток газовых турбин, деталей реактивных двигателей и ракетных установок. Важнейшие легирующие элементы жаропрочных сталей – это хром (15-20 %), никель (8-15 %), вольфрам. Жаропрочные стали принадлежат к аустенитным сплавам.
Магнитные стали используют для изготовления постоянных магнитов и сердечников магнитных устройств, работающих в переменных полях. Для постоянных магнитов применяют высокоуглеродистые стали, легированные хромом или вольфрамом. Они хорошо намагничиваются, и длительное время сохраняют остаточную индукцию. Сердечники магнитных устройств изготавливают из низкоуглеродистых (менее 0,005 % С) сплавов железа и кремния. Эти стали легко перемагничиваются и характеризуются малым значением электрических потерь.
К чугунам относят сплавы железа с углеродом, содержащие более 2,14 % углерода. Различают чугуны: белые, серые, высокопрочные и ковкие. Чугун отличается от стали своими свойствами. Он в очень малой степени способен к пластической деформации, но обладает хорошими литейными свойствами. Чугун дешевле стали. В зависимости от условий кристаллизации, чугун может содержать углерод в виде цементита, графита или в виде их смеси. Форма образующегося графита также может быть различной.
Белый чугун содержит весь углерод в виде цементита. Из-за большого содержания углерода (6,69 % (масс.)) белые чугуны характеризуются высокой твердостью, хрупкостью. Поэтому в качестве конструкционного материала белые чугуны применяются в виде белого упрочняющего слоя на поверхности серого чугуна для изготовления прокатных валков, лемехов плугов, тормозных колодок и др.
В сером чугуне углерод содержится главным образом в виде пластинок графита. Эти низкопрочные пластинчатые включения углерода пронизывают металлическую основу материала и служат центрами разрушения серого чугуна при растяжении. Это влияние графита гораздо меньше сказывается при сжатии чугуна. Поэтому прочность чугуна при сжатии примерно в четыре раза больше прочности при растяжении. Поэтому серый чугун применяют при изготовлении деталей, работающих на сжатие, или для ненагруженных деталей (станины станков, корпуса редукторов и насосов, поршневые кольца двигателей и др.).
Высокопрочный чугун содержит графит в шаровидной (глобулярной) форме в интервале 3,0-3,6 %. Для этого в чугун вводят магний (до 0,08 %). Шаровидный углерод меньше снижает прочность чугуна, чем пластинчатый. Такие чугуны дешевле сталей и их часто применяют для замены стальных деталей и конструкций. Из высокопрочного чугуна изготавливают коленчатые валы, крышки цилиндров, детали прокатных станков, прокатные валки, насосы, вентили.
Медные и другие сплавы.
Латуни содержат медь до 45 % цинка. Различают простые и специальные латуни. В состав последних, кроме меди и цинка, входят другие элементы, например, железо, алюминий, олово, кремний. Латуни находят разнообразное применение. Из них изготавливают трубы для конденсаторов и радиаторов, детали механизмов, в частности часовых. Некоторые специальные латуни обладают высокой коррозийной стойкостью в морской воде и применяются в судостроении. Латунь с высоким содержанием меди – томпак – благодаря своему внешнему сходству с золотом используется для ювелирных и декоративных изделий.
Медноникелевые сплавы подразделяются на конструкционные и электротехнические. К конструкционным относятся мельхиоры и нейзильберы. Мельхиоры содержат 20-30 % никеля и небольшие количества железа и марганца, а нейзильберы содержат 5-35 % никеля и 13-45 % цинка. Благодаря стойкости против коррозии в воде, в том числе морской, конструкционные медноникелевые сплавы получили широкое распространение в судостроении и в энергетической промышленности. Из них изготавливают радиаторы, трубопроводы, дистилляционные установки для получения питьевой воды из морской.
Сплавы на основе никеля можно разделить на жаропрочные, магнитные и сплавы с особыми свойствами. Жаропрочные сплавы никеля используются в современных турбинах и реактивных двигателях, где температура достигает 850-900 0С. К важнейшим жаропрочным сплавам никеля относятся нимоник, инконель, хастеллой. В состав этих сплавов входит свыше 60 % никеля, 15-20 % хрома и другие металлы. Производятся также металлокерамические жаропрочные сплавы, содержащие никель в качестве связующего металла. Эти сплавы выдерживают нагревание до 1100 0С. К сплавам никеля с особыми свойствами принадлежат монель-металл, никелин, константан, инвар, платинит. Монель-металл (сплав никеля с 30 % меди) широко используется в химическом аппаратостроении, так, как по механическим свойствам он превосходит никель, а по коррозийной стойкости почни не уступает ему.
Износостойкие материалы.
Одним из необходимых условий создания износостойкого материала является обеспечение высокой твердости его поверхности. Такими свойствами обладают многие карбиды металлов. Карбиды металлов входят в составы сплавов карбидообразующих элементов (Cr, W, Ti) с углеродом (до 40 % С). Их применяют для изготовления литых и наплавочных материалов.
Упрочнения поверхности стали можно добиться специальными методами, такими как поверхностной закалкой с нагревом токами высокой частоты и химико-термической обработкой в виде цементации и азотирования. Цементация и азотирование – процессы диффузионного насыщения поверхностного слоя детали углеродом и азотом, соответственно. Данной обработке подвергают такие детали машин и аппаратов, которые должны иметь износостойкую рабочую поверхность и вязкую сердцевину (зубчатые колеса, коленчатые валы, кулачки, червяки).
Легкие конструкционные материалы. Для современной техники характерно снижение массы машин, аппаратов, приходящиеся на единицу используемой мощности. Для этого используют материалы с высокой удельной прочностью. Удельная прочность – отношение прочности материала к его плотности.
Современные материалы, применяемые в автомобилях, судах, авиации, космической технике, должны обладать большой удельной прочностью и достаточной пластичностью. Однако большинство пластичных материалов не обладает термической прочностью, а высокопрочные материалы – недостаточно пластичны.
В качестве конструкционных материалов из легких металлов применяются только Be, Mg, Al, Ti и сплавы на их основе. Данные металлы являются химически стойкими веществами, благодаря наличию плотных защитных оксидных слоев.
Сплавы на основе бериллия и магния обладают наряду с малой плотностью ценными упруго-прочностными свойствами. Бериллий обладает, прочностью легированной стали, а его удельная прочность одна из наивысших среди металлов. Бериллий является одним из лучших материалов для изготовления жестких и легких конструкций. Главными недостатками бериллия являются хрупкость, высокая стоимость и токсичность.
Прибавка к магнию небольших количеств других металлов существенно улучшает его твердость, прочность и сопротивляемость к коррозии. Достоинством магниевых сплавов является их малая плотность, составляющая 1,8 г/см3. Они используются в ракетной технике, в авиастроении, при изготовлении автомобилей, мотоциклов, приборов. Недостатком сплавов магния являются низкая стойкость против коррозии во влажной атмосфере и, особенно в морской воде.
Сплавы алюминия характеризуются высокой удельной прочностью, которая сравнима с прочностью высокопрочных сталей. Сплавы алюминия имеют низкую плотность, составляющую 2,5 – 2,8 г/см3. Они также имеют такие достоинства как удовлетворительную стойкость против атмосферной коррозии, простоту получения и обработки.
Электротехнические материалы: полупроводники, диэлектрики, проводники, сверхпроводники.
По электрическим свойствам материалы делятся на диэлектрики, полупроводники, проводники и сверхпроводники. Они отличаются друг от друга электрической проводимостью и её механизмом, характером зависимости электрического сопротивления от температуры.
Диэлектрики. Это вещества, которые не обладают хорошей электронной проводимостью и поэтому являются изоляторами. Диэлектрики имеют удельное электрическое сопротивление в интервале от 108 до 1016 Ом∙м. Некоторые из них также как и металлы имеют кристаллическую структуру. Вид химической связи в диэлектриках, в основном, ионный или ковалентный. Свободные носители заряда отсутствуют. Между валентной зоной и зоной проводимости находится широкая запрещенная зона. К диэлектрикам относятся полимерные материалы: соли, оксиды, полиэтилен, резина, текстильные материалы.
Диэлектрики, такие как керамика, стекло, пластмассы обладают высокой диэлектрической проницаемостью, значения которой находятся в пределах от 2 до 20. Но отдельные диэлектрики имеют значения относительной диэлектрической проницаемости около тысячи и выше. Такие диэлектрики называются сегнетоэлектриками.
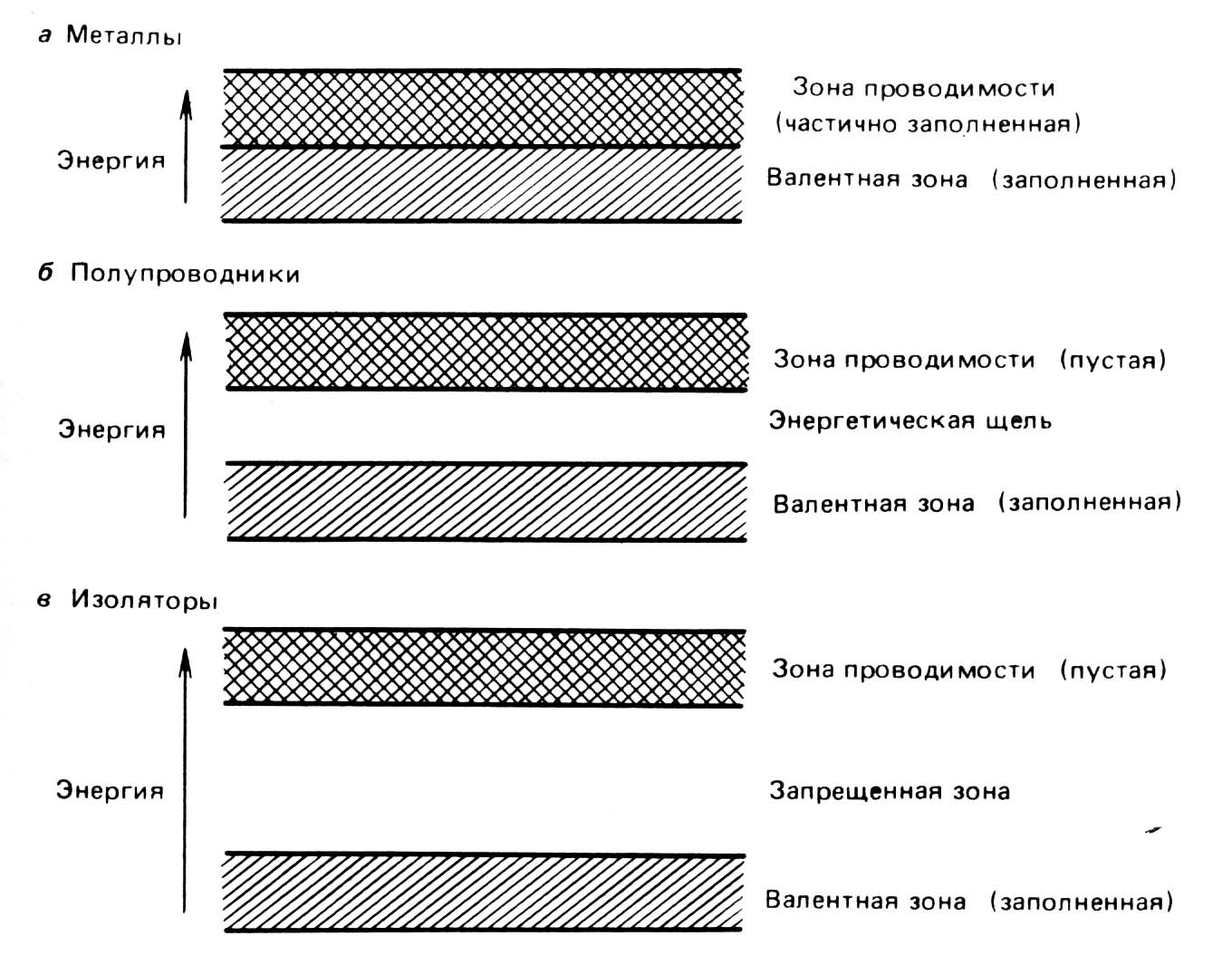
Рис. 1. Схема расположения энергетических зон в металле (а), полупроводнике (б),
изоляторе (в).
Полупроводники. Полупроводники занимают промежуточное положение между изоляторами и проводниками, они отличаются как от металлов, так и от изоляторов. При низких температурах электрическое сопротивление полупроводников велико и они в этом отношении похожи на диэлектрики, хотя зависимость удельного электрического сопротивления от температуры у них отличается от таковой для изоляторов. При нагревании электрическая проводимость полупроводников растет, достигая величин, характерных для металлов.
Полупроводники имеют удельное электрическое сопротивление от 10-5 до 108 Ом∙м. К полупроводникам относятся B, C, Si, Ge, Sn, P, As, Sb, S, Se, Te, I. Полупроводниками являются такие бинарные соединения ZnO, FeO, ZnS, CdS, GaAs, ZnSb, SiC, а также более сложные соединения.
Ширина запрещенной зоны в полупроводниках изменяется от 0,08 эВ (у металла Sn) до 5,31 эВ (неметалла алмаз). Зависимость электрических свойств полупроводников от температуры и освещенности объясняется электронным строением их кристаллов. У них, как и у изоляторов, валентная зона отделена от зоны проводимости запрещенной зоной (рис. 1). Однако ширина запрещенной зоны в случае полупроводников существенно меньше, чем у диэлектриков. Благодаря этому при действии облучения или при нагревании, электроны, занимающие верхние уровни валентной зоны, могут переходить в зону проводимости и участвовать в переносе электрического тока. С повышением температуры и увеличением освещенности число электронов, переходящих в зону проводимости, возрастает, что приводит к росту электрической проводимости полупроводника.
В полупроводниках с ковалентной связью появление электрона в зоне проводимости одновременно создает его вакансию в валентной зоне. Данные вакансии называются дырками. Они могут участвовать в движении под действием электрического поля. Поэтому электрический ток в полупроводниках определяется движением электронов в зоне проводимости и движением дырок в валентной зоне. В первом случае электроны переходят на незанятые молекулярные орбитали, во втором – на частично занятые молекулярные орбитали.
Из простых полупроводников наиболее распространены кремний и германий. Полупроводники применяются в радиоэлектронных приборах.
Проводники. Это вещества, которые проводят электрический ток. К проводникам относятся металлы. Удельное электрическое сопротивление проводников изменяется от 10-8 до 10-5 Ом∙м. С повышением температуры электрическое сопротивление увеличивается, этим они и отличаются от полупроводников. Носителями заряда в проводниках являются электроны. Валентная зона и зона проводимости электронной структуры металлов пересекаются (рис. 1 а). Это позволяет электронам из валентной зоны переходить при небольшом возбуждении на молекулярные орбитали зоны проводимости.
Проводники применяются для передачи электрической энергии на большие расстояния, в качестве резисторов, нагревательных элементов, осветительных приборов.
Сверхпроводники. Материалы, у которых электрическое сопротивление при некоторой критической температуре резко уменьшается до нуля, называются сверхпроводниками. У обычных веществ падение электрического сопротивления практически до нуля возможно только при низких температурах. Например, у ртути она составляет 4,2 К. Поэтому широкое практическое использование сверхпроводимости нецелесообразно, так как связано с большими энергетическими затратами на охлаждение до очень низких температур.
В 1988 году было открыто явление высокотемпературной сверхпроводимости. Найдены такие вещества, которые проявляют сверхпроводящие свойства при достаточно высоких температурах порядка 90 – 135 К. Такие температуры могут быть достигнуты в среде жидкого азота. Это открывает возможности практического использования явления сверхпроводимости.
Высокотемпературные свойства обнаружены у следующих веществ: Y-Ba-Cu-O (Tc = 90 K), Bi - Ca – Cu – O (Tc = 110 K), Hg – Ba – Ca – Cu – O (Tc = 135 K).
В настоящее время ведутся поиски новых систем, которые могли бы находиться в сверхпроводящем состоянии при температурах кипения диоксида углерода, которая равна 194,7 К.
