
- •Основные положения координационной теории
- •Получение комплексных солей
- •Классификация комплексных частиц
- •Содержит атомы не менее трех сортов (кроме водорода);
- •В качестве центрального атома выступает ион металла. Номенклатура комплексных соединений
- •Химическая связь в комплексных соединениях и их строение
- •Устойчивость комплексных соединений в растворе
- •Задания для отработки умения составлять уравнения реакций образования и разрушения гидроксокомплексов
Химическая связь в комплексных соединениях и их строение
В кристаллических комплексных соединениях с заряженными комплексами связь между комплексом и внешнесферными ионами ионная, связи между остальными частицами внешней сферы – межмолекулярные (в том числе и водородные). В молекулярных комплексных соединениях связь между комплексами межмолекулярная.
В большинстве комплексных частиц между центральным атомом и лигандами связи ковалентные. Все они или их часть образованы по донорно-акцепторному механизму (как следствие – с изменением формальных зарядов). В наименее прочных комплексах (например, в аквакомплексах щелочных и щелочноземельных элементов, а также аммония) лиганды удерживаются электростатическим притяжением. Связь в комплексных частицах часто называют донорно-акцепторной или координационной связью.
Рассмотрим ее образование на примере аквакатиона железа(II). Этот ион образуется по реакции:
FeCl2кр + 6H2O = [Fe(H2O)6]2+ + 2Cl-
Электронная формула атома железа – 1s22s22p63s23p64s23d6. Составим схему валентных подуровней этого атома:
![]()
При образовании двухзарядного иона атом железа теряет два 4s-электрона:
![]()
Ион железа акцептирует шесть электронных пар атомов кислорода шести молекул воды на свободные валентные орбитали:
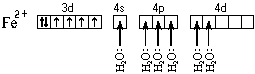
Образуется комплексный катион, химическое строение которого можно выразить одной из следующих формул:
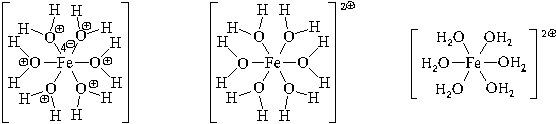
Пространственное строение этой частицы выражается одной из пространственных формул:
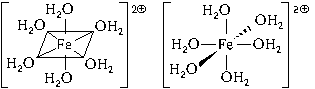
Форма координационного полиэдра – октаэдр. Все связи Fe-O одинаковые. Предполагается sp3d2-гибридизация АО атома железа. Магнитные свойства комплекса указывают на наличие неспаренных электронов.
Если FeCl2 растворять в растворе, содержащем цианид-ионы, то протекает реакция
FeCl2кр + 6CN- = [Fe(CN)6]4- + 2Cl- .
Тот же комплекс получается и при добавлении к раствору FeCl2 раствора цианида калия KCN:
[Fe(H2O)6]2+ + 6CN- = [Fe(CN)6]4- + 6H2O .
Это говорит о том, что цианидный комплекс прочнее аквакомплекса. Кроме того магнитные свойства цианидного комплекса указывают на отсутствие неспаренных электронов у атома железа. Все это связано с несколько иным электронным строением этого комплекса:
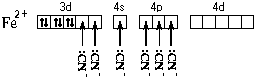
Более " сильные"
лиганды CN![]() образуют более прочные связи с атомом
железа, выигрыша в энергии хватает на
то, чтобы " нарушить" правило Хунда
и освободить 3d-орбитали
для неподеленных пар лигандов.
Пространственное строение цианидного
комплекса такое же, как и аквакомплекса,
но тип гибридизации другой – d2sp3.
образуют более прочные связи с атомом
железа, выигрыша в энергии хватает на
то, чтобы " нарушить" правило Хунда
и освободить 3d-орбитали
для неподеленных пар лигандов.
Пространственное строение цианидного
комплекса такое же, как и аквакомплекса,
но тип гибридизации другой – d2sp3.
" Сила" лиганда зависит прежде всего от электронной плотности облака неподеленной пары электронов, то есть, она увеличивается с уменьшением размера атома, с уменьшением главного квантового числа, зависит от типа гибридизации ЭО и от некоторых других факторов. Важнейшие лиганды можно выстроить в ряд по возрастанию их " силы" (своеобразный " ряд активности" лигандов), этот ряд называется спектрохимическим рядом лигандов. В результате трудов многих ученых ряд транс-влияния лигандов в настоящее время выглядит следующим образом:
CO > CN – > NO2– > ЭДТА > NH3 > SCN– > H2O > OH– > F– > Cl– > SCN– > Br – > I –
Слева находятся лиганды более сильного поля, справа – более слабого.
Ряд транс-влияния лигандов дает возможность делать важные предсказания. В частности, с его помощью можно судить о направлении реакций замещения лигандов во внутренней сфере координационных соединений.
Химические свойства комплексных соединений
Для комплексных соединений, прежде всего, характерны те же свойства, что и для обычных соединений тех же классов (соли, кислоты, основания). Если комплексное соединение кислота, то это сильная кислота, если основание, то и основание сильное.
В водном растворе
комплексные соединения диссоциируют
по типу диссоциации сильного электролита
– на комплексный ион и ионы, составляющие
внешнюю сферу, например: Na3[Co(NO2)6]
![]() 3Na++[Co(NO2)6]3–
.
3Na++[Co(NO2)6]3–
.
Внутренняя сфера типичных комплексных соединений в растворах может диссоциировать на ионы или на ионы и молекулы (по типу диссоциации слабого электролита). Например, [Cu(NH3)4]SO4 = [Cu(NH3)4]2+ + SO42- , K3[Fe(CN)6] = 3 K+ + [Fe(CN)6]3- , [Co(NO2)6]3- Co3+ + 6 NO2- .
Электролитическая
диссоциация комплексных ионов подчиняется
закону действующих масс и количественно
характеризуется константой диссоциации,
которая носит название константы
нестойкости Кн,
и для последнего процесса диссоциации:
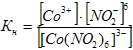 .
.
У типичных комплексных ионов Кн очень мала и является мерой его устойчивости.
Если комплексное соединение кислота, то это сильная кислота, если основание, то и основание сильное. Эти свойства комплексных соединений определяются только наличием ионов H+ или OH-.
Кроме этого комплексные кислоты, основания и соли вступают в обычные реакции обмена, например:
[Cu(NH3)4]SO4
+ BaCl2
= BaSO4![]() +
[Cu(NH3)4]Cl2
FeCl3
+ K4[Fe(CN)6]
= Fe4[Fe(CN)6]3
+
3KCl
+
[Cu(NH3)4]Cl2
FeCl3
+ K4[Fe(CN)6]
= Fe4[Fe(CN)6]3
+
3KCl
Кроме этого в реакцию может вступать и сама комплексная частица, причем, тем активнее, чем она менее устойчива. Обычно это реакции замещения лигандов, протекающие в растворе, например:
[Cu(H2O)4]2+ + 4NH3 = [Cu(NH3)4]2+ + 4H2O,
а также кислотно-основные реакции типа
[Zn(OH)4]2- + 2H3O+ = [Zn(H2O)2(OH)2] + 2H2O [Zn(H2O)4]2+ + 2OH- = [Zn(H2O)2(OH)2] + 2H2O.
Образующийся в этих реакциях комплекс [Zn(H2O)2(OH)2] после выделения и высушивания превращается в гидроксид цинка: [Zn(H2O)2(OH)2] = Zn(OH)2 + 2H2O.
Последняя реакция – простейший пример разложения комплексного соединения. В данном случае она протекает при комнатной температуре. Другие комплексные соединения разлагаются при нагревании, например:
[Cu(NH3)4]SO4.H2O = CuSO4 + 4NH3 + H2O (выше 300 oС), 4K3[Co(NO2)6] = 12KNO2 + 4CoO + 4NO + 8NO2 (выше 200 oС), K2[Zn(OH)4] = K2ZnO2 + 2H2O (выше 100 oС).
Для оценки возможности протекания реакции замещения лигандов можно использовать спектрохимический ряд, руководствуясь тем, что более сильные лиганды вытесняют из внутренней сферы менее сильные.
Образующийся в реакциях взаимодействия раствора щелочи с основанием амфотерного металла комплекс, например, [Zn(H2O)2(OH)2] после выделения и высушивания превращается в гидроксид цинка:
[Zn(H2O)2(OH)2] = Zn(OH)2 + 2H2O
Последняя реакция – простейший пример разложения комплексного соединения. В данном случае она протекает при комнатной температуре. Другие комплексные соединения разлагаются при нагревании, например:
[Cu(NH3)4]SO4.H2O = CuSO4 + 4NH3 + H2O (выше 300 oС); 4K3[Co(NO2)6] = 12KNO2 + 4CoO + 4NO + 8NO2 (выше 200 oС); K2[Zn(OH)4] = K2ZnO2 + 2H2O (выше 100 oС).
Окислительно-восстановительные реакции с участием комплексных соединений. Комплексные соединения могут участвовать в окислительно-восстановительных реакциях. При этом изменяется степень окисления центрального атома. Возможны реакции двух типов:
а) Изменение степени окисления без разрушения комплекса
2K3[Fe3+(CN)6] + 2KI = 2K4[Fe2+CN)6] + I2 ;
б) Изменение степени окисления с разрушением комплекса в результате восстановления центрального иона до металла
Zn + 2K[Au+(CN)2] = 2Auo + K2[Zn(CN)4].
