
Периферические анальгетики
Прохождение болевого сигнала зависит от функционирования прово-дящих путей между поврежденной частью тела и мозгом. Аксон проводит импульс за счет диффузии ионов через мембрану нервного волокна и на конечном этапе путем высвобождения нейромедиатора в синапсе. Знание нейромедиаторов, участвующих в этом процессе, важно для понимания физиологии болевого восприятия и механизма действия обезболивающих средств. Правда, эксперименты такого рода проводятся только на живот-ных, а экстраполяция результатов таких исследований на человеческий организм не всегда оправдана.
Место действия периферических анальгетиков – это вмешательство в процесс возникновения болевого ощущения в поврежденной ткани или на пути прохождения сигнала по сенсорному нерву до спинного мозга. Эти обезболивающие средства наименее опасны: действуя на периферии, они не влияют на работу ЦНС и сводят до минимума такие побочные эффекты общих анестетиков, как остановка дыхания, тошнота и выработка болез-ненного пристрастия.
На начальном этапе повреждение клеток вызывает высвобождение в периферической ткани или в ткани внутренних органов алгогенов. Эта группа химических веществ стимулирует небольшие сенсорные нервы, их действие может быть также опосредовано влиянием на местную сосудис-тую систему. Действие алгогенов, как говорилось выше, усиливается прос-тагландинами, которые делают более чувствительными окончания нерв-ных клеток, предназначенных для передачи болевого сигнала. В соответст-вии с этим исследование периферических анальгетиков сфокусированы на трех областях:
Блокировка эффекта простагландинов
Блокировка эффекта алгогенов
Блокировка передачи между периферическими нервами и нейронами спинного мозга.
Роль простагландинов становится ничтожной если удается заблокиро-вать действие самих алгогенов. Это достаточно сложная задача, так как ал-гогенов много и действуют они на разные рецепторы. В идеальном случае надо иметь набор (коктейль) из нескольких антагонистов. Более всего привлекает внимание в роли алгогена серотонин. Введение этого вещества под кожу вызывает сильнейшее жжение. Предполагается, что он высво-бождает вещество Р и брадикинин – нонапептид Арг-Про-Про-Гли-Фен-Сер-Про-Фен-Арг, рецептор которого не идентифицирован. Модификация структуры брадикинина за счет введения других аминокислот, в частности замена фенилаланина на тиенилаланин (Тие) привела к получению эффек-тивного антагониста брадикинина, который к тому же плохо гидролизу-ется пептидазами: Арг-Про-Про-Гли-Тие-Сер-DФен-Тие-Арг.
Определенную роль в генерировании болевого сигнала играют и эндо-генные опиоиды, например, Мет-энкефалин. При поиске их структурных аналогов был найден пентапептид Тир-DАрг-Гли-Фен(4-NO2)-Про-NН2, который оказался обезболивающим средством, действующим на уровне периферической нервной системы.
Самыми успешными местными анестетиками оказались структурные аналоги алкалоида кокаина, который до сих пор ограниченно применяется в медицинской практике для небольших хирургических вмешательств:
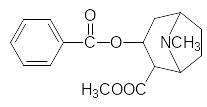
Его действие, судя по всему, основано на блокировке медиаторного эффекта серотонина и катехоламинов. Первыми синтетическими местны-ми анестетиками стали полученные путем упрощения структуры кокаина анестезин (бензокаин) и новокаин:
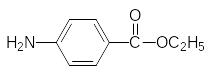
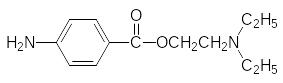
которые полностью лишены наркотического эффекта, присущего кокаину. Затем были получен ряд более эффективных и более длительно дейст-вующих препаратов, примерами которых служат лидокаин и артикаин:
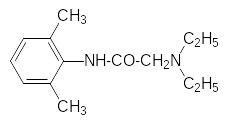
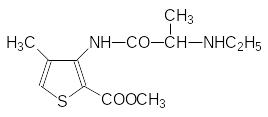
Эти вещества вводят парентерально при небольших хирургических операциях, например, в стоматологии.
