
- •§1. Макрокинетическая система.
- •§2. Основные задачи химической кинетики.
- •§3. Скорость химической реакции.
- •§4. Скорость простых химических превращений.
- •5. Реакции нулевого порядка.
- •§7. Последовательные реакции.
- •§8. Параллельные реакции.
- •§11. Кинетические уравнения обратимого химического проце-сса.Пусть имеем простую реак-цию:
- •§13. Колебательные режимы протекания химических реакций.При описании процесса окисления высших углеводородов используется модельная схема. Схема Вольтера:
- •§14. Элементарные понятия теории цепных реакций.
- •4. Стадия разветвления цепей.
- •§16. Окисление водорода при низком давлении, как пример црр.Рассмотрим одну из наибо-лее интересных реакций: окисле-ние водорода. Это высокоэнерге-тическая реакция.
- •§19. Элементы теории соударений.Данная теория была разработана и нашла широкое применение для газофазных реакций.
§3. Скорость химической реакции.
Определение скорости химиче-ского процесса непосредственно связано со структурой реагирую-щей системы и свойствами по-верхности, отделяющей её от ок-ружающей среды. Исходные, про-межуточные и конечные проду-кты реакции в ходе химического процесса могут находиться в различных фазовых состояниях. Поэтому различают гомогенные, гетерогенные и гомогенно-гетеро-генные реакции, и соответствую-щие им скорости. Химическая ре-акция называется гомогенной, если она протекает в пределах одной фазы. Гетерогенная реак-ция протекает на границе раздела фаз. Гомогенно-гетерогенная ре-акция – это сложный химический процесс, отдельные стадии кото-рого являются гомогенными, а другие гетерогенными реакциями.
Скорость химической
реакции должна характеризовать
количе-ство вещества вступающего в
ре-акцию, или образующегося в ре-зультате
неё. Реагирующая систе-ма состоит из
совокупности Ра-зличных молекул, или
их фра-гментов. Как в механике опери-руют
со скоростью определенного сорта частиц,
также в хим. кине-тике вводится понятие
скорости хим. реакции по конкретному
ко-мпоненту. Скорость химической реакции
по i-му
компоненту опре-деляется пропорционально
скоро-сти изменения массы этого
ком-понента,т.е.
![]() Коэффициент пропорциональности зависит
от того, какая реакция рассматрива-ется
(гетерогенная, гомогенная,
гомогенно-гетерогенная). Ограничимся
случаем гомогенной реакции. Для неё
коэффициент пропорциональности равен:
Коэффициент пропорциональности зависит
от того, какая реакция рассматрива-ется
(гетерогенная, гомогенная,
гомогенно-гетерогенная). Ограничимся
случаем гомогенной реакции. Для неё
коэффициент пропорциональности равен:
![]() ,
где V
– объем
реагирующей системы.
,
где V
– объем
реагирующей системы. ![]() ,
,
![]() (2)
Часто массу
измеряют в молях, тогда
(2)
Часто массу
измеряют в молях, тогда ![]() ,
,![]() (2’)
(2’)
![]() – масса i-го
компонента;
– масса i-го
компонента;
![]() –
количество молей
i-го
компо-нента. Если в ходе химического
процесса объем реагирующей системы не
меняется, т. е. V=const,
то скорость химической реакции
будет:
–
количество молей
i-го
компо-нента. Если в ходе химического
процесса объем реагирующей системы не
меняется, т. е. V=const,
то скорость химической реакции
будет: ![]() , (3)
, (3)
![]() –
концентрация i-го
компоне-нта, т. е. количество i-го
компо-нента в единице объема
–
концентрация i-го
компоне-нта, т. е. количество i-го
компо-нента в единице объема
![]() ,
,
![]() .
.
Молярная концентрация
![]() ,
,![]() .Очень
часто сле-дят за скоростью изменения
ко-нцентрации i-го
компонента.
.Очень
часто сле-дят за скоростью изменения
ко-нцентрации i-го
компонента.
Скорость реакции сложных процессов.
Если i-ый компонент промежу-точный, и участвует в нескольких стадиях сложного химического процесса, то скорость реакции по этому компоненту будет вычи-сляться с учетом всех стадий, в которых он участвует.
![]() (4)
(4)
![]() –
скорость образования,
эта скорость должна учитывать все
стадии, где i-ый
компонент явля-ется продуктом (образуется).
–
скорость образования,
эта скорость должна учитывать все
стадии, где i-ый
компонент явля-ется продуктом (образуется).
![]() –
скорость расхода,
эта скоро-сть должна складываться из
ско-ростей всех стадий, где i-ый
компонент является исходным веществом
(расходуется).
–
скорость расхода,
эта скоро-сть должна складываться из
ско-ростей всех стадий, где i-ый
компонент является исходным веществом
(расходуется).
В частности, если
имеется обра-тимая реакция, при V
=const,
то можно записать
![]() .
.
Протекание реакции в условиях переменного объема.
Переменность объема
вносит свой вклад в скорость изменения
концентрации i-го
компонента. ![]() ,
,
если перейти к
концентрации, и определенной выше
скорости химической реакции, то
![]() (5)
(5)
![]() – относительная
скорость изменения объема.
– относительная
скорость изменения объема.
Таким образом,
изменение конце-нтрации, при переменном
объеме будет определяться скоростью
хи-мического процесса и относите-льной
скоростью изменения объе-ма.![]() (5’)
(5’)
Протекание реакции в движу-щейся среде.
Если реакции
протекают в движу-щейся сплошной среде,
то относи-тельная скорость изменения
объе-ма для i-го
компонента, опреде-ляется вектором
скорости i-го
ко-мпонента, точнее его диверген-цией:![]() , где
, где
![]() –
ско-рость движения i-го
компонента.
–
ско-рость движения i-го
компонента.
Кроме того, если система дви-жется, то производная
![]()
Должна пониматься
в смысле Лаг-ранжа (![]() - изменение ci
вдоль траектории движения).
- изменение ci
вдоль траектории движения).
Используя данные формулы и (5’), можем получить следующие соотношения:
![]()
![]() Таким
образом, получили фор-мулу:
Таким
образом, получили фор-мулу:![]() (6)
(6)
Обычно в механике многокомпо-нентных систем стремятся из-бавиться от рассмотрения ско-ростей каждой компоненты, и перейти к скорости системы в целом:
![]() ,
i=1,…,N
(
,
i=1,…,N
(![]() - скорость движения центра масс).
- скорость движения центра масс).
Это удается сделать
введением в рассмотрение диффузионных
век-торов потока соответствующего
компонента:
![]()
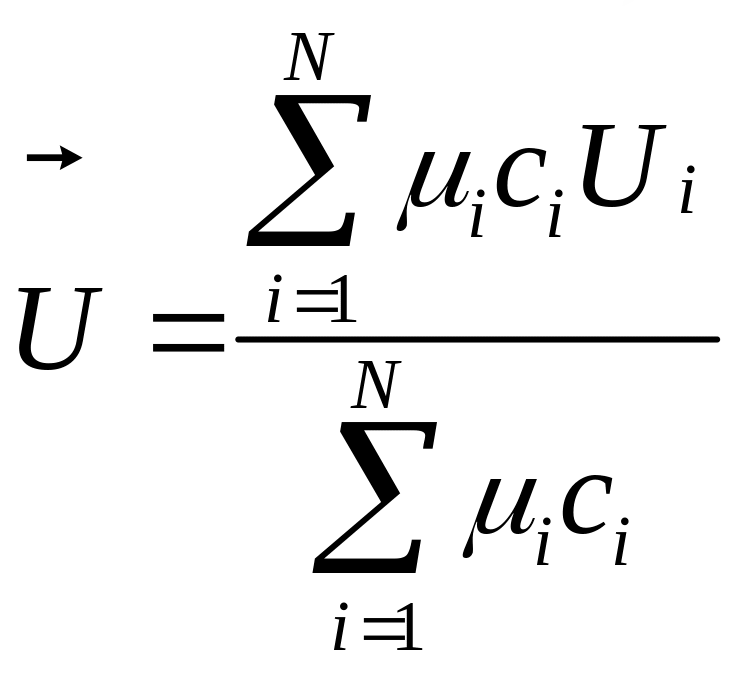 ,
здесь
,
здесь
![]() –
моля-рная масса i-го
компонента.
–
моля-рная масса i-го
компонента.
![]() ,
т. е. скорость i-го
ко-мпонента определяется диффу-зией
i-го
компонента и переносом его движущейся
системой. Заме-тим, что процесс диффузии
может присутствовать, даже если сис-тема
в целом покоится, т. е.
,
т. е. скорость i-го
ко-мпонента определяется диффу-зией
i-го
компонента и переносом его движущейся
системой. Заме-тим, что процесс диффузии
может присутствовать, даже если сис-тема
в целом покоится, т. е.
![]() ,
а
,
а
![]() .
Процесс диффузии отсу-тствует только
если для всех ко-мпонент выполняется
равенство:
.
Процесс диффузии отсу-тствует только
если для всех ко-мпонент выполняется
равенство:
![]() .Таким
образом, если ввести
.Таким
образом, если ввести
![]() ,
то (6) преобразу-ется:
,
то (6) преобразу-ется:![]() (7
(7
Уравнение (7) – закон сохране-ния массы i-го компонента (урав-нение неразрывности в диффе-ренциальной форме). Концентра-ция i-го компонента изменяется за счет химического процесса, за счет дивергенции диффузионного вектора, и за счет дивергенции потока в целом. *(рис.3)
Рассмотрим объем
![]() ,
который ограничен поверхностью
,
который ограничен поверхностью
![]() ,
и проинтегрируем (7) по этому
объему
,
и проинтегрируем (7) по этому
объему![]() Воспользуемся
формулой Остро-градского-Гаусса:
Воспользуемся
формулой Остро-градского-Гаусса:
![]() .
.
![]() ,
,
![]() .
(7’)
.
(7’)
(7’) – закон
сохранения массы i-го
компонента в объеме
(закон сохранения в интегральной фо-рме).
Т. е. изменение массы i-го
компонента происходит за счет химического
процесса, за счет диффузионного потока
через поверхность
,
и за счет потока массы i-го
компонента вместе со всей движущейся
системой (кон-вективный поток). Таким
обра-зом, изучается
![]() ,
,
![]() определяет-ся отдельно. Существуют
феноме-нологические и статистические
методы. Часто используется за-кон
Фика (аналог
закона Фурье для теплопроводности):
определяет-ся отдельно. Существуют
феноме-нологические и статистические
методы. Часто используется за-кон
Фика (аналог
закона Фурье для теплопроводности):
![]() ,
где
,
где
![]() –
коэффи-циент диффузии i-го
компонента.
–
коэффи-циент диффузии i-го
компонента.
