Тема 4 Вуглеводні
Заняття 2. Ненасичені вуглеводні: Алкени, дієни , алкіни.
Мета:сформувати поняття про нові класи органічних сполук – ненасичені вуглеводні: алкени, алкіни, дієни; ознайомитись з природою кратних зв’язків та пов’язані з цим хімічними властивостями, продовжувати формувати вміння складати структурні формули за назвами речовин, називати речовини по міжнародній номенклатурі; розглянути нові види гібридизації атомних орбіта лей, будову ненасичених вуглеводнів та пов’язані з цим фізичні та хімічні властивості даних сполук; удосконалювати вміння складати рівняння хімічних реакцій за участі органічних речовин.
Навчальні питання:
Алкени,алкіни, дієни. Гомологічний ряд , загальна формула.
Будова молекули , фізичні і хімічні властивості. Правило Марковнікова, полімеризація.
Ізомерія та номенклатурні назви.
Добування та застосування
Полімери та полімеризація. Будова полімерного ланцюга.
Застосування та добування полімерів, пластмас.
Навчальна література:
Л-3 с.44-60, 63-64, 66-70
Л-4 с.61-68
ІІІ. Алкени.
Визначення |
Функціо- нальні групи |
Загальна формула |
Номенк- латурна назва |
Види ізомерії |
Будова |
Застосування |
Добування |
Фізичні і Хімічні властивості |
Ненасичені вуглеводні – вулгеводні в молекулах яких атоми карбону зв’язані між собою кратними (подвійними чи потрійними зв’язками) Алкени – це ненасичені вуглеводні з одним подвійним зв’язком. Полімери – речовини молекули яких (макромолекули ) складаються з великої кількості груп атомів ( структурних ланок) зв’язаних між собою хімічними зв’язками. |
С = С
|
CnH2n |
Нумерація починається з того краю де ближче знаходиться подвійний зв'язок ,після кореня пишеться номер карбону з якого починається подвійний зв'язок ,в кінці пишеться закінчення ен |
1.ізомерія карбонового ланцюга 2.ізомерія положення подвійного зв’язку 3. просторова ізомерія 4.міжкласова ізомерія з циклоалканами. |
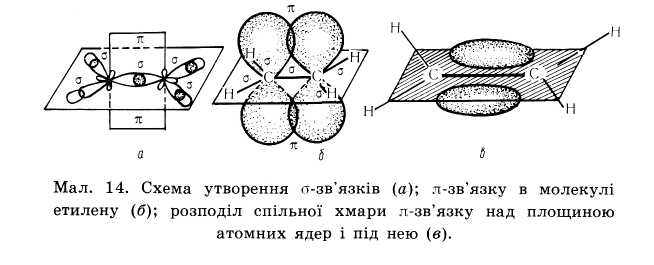
Два атоми Карбону, що приймають участь в утворенні подвійного зв’язку знаходяться в стані sр2 – гібридизації. Тобто із чотирьох існуючих орбіта лей кожного атома вирівнюють ся лише три ( одна s, та дві р орбіта лі), і одна р – орбіталь лишається не гібридизована (має форму гантелі). Три гібридизовані орбіта лі кожного атома карбону розташовуються у вигляді двох рівносторонніх трикутників на площині. Однією вершиною ці трикутники перекриваються утворюючи δ-зв'язок інші орбіта лі утворюють δ- зв’язки з атомами гідрогенів
Не гібридизовані р-орбіталі обох атомів карбонів розташовуються перпендикулярно площині δ-звязків , перекриваються над і під площиною ,утворюючи π – зв'язок. Отже подвійний зв'язок алкенів містить один δ-зв'язок і один π-зв'язок. δ-зв'язок міцніший ніж π-зв'язок.
|
1.етилен використовують для органічного синтезу поліетилену, етанолу, хлор етану, вінілхлориду, стиролу. 2.етилен прискорює дозрівання фруктів. |
1. відщеплення галогенів від галогенопохідних алканів СН3-CHBr-CH2Br +Zn→CH3-CH=CH2+ ZnBr2 2.Відщеплення галогеноводнів CH3-CHCl-CH3+ NaOH →CH2=CH-CH3+ NaCl +H2O 3.відщеплення води (дегідратація) CH3-CHOH-CH2-CH3 → CH2=CH-CH2-CH3 +H2O 4.відщеплення водню від алканів (дегідрогенування) CH3-CH2-CH2-CH3 → CH3-CH=CH-CH3 +H2 5. крекінг алканів C8H18 →C4H10+C4H8 6. часткова гідрогенізація алкінів. CHΞCH+H2→CH2=CH2 |
C2Н4– С5Н10 -гази, С6Н12 – С14Н28 –рідини, С15Н30 і вище –тверді речовини. Вони практично не розчинні у воді і частково розчинні у спиртах. 1.Реакція приєднання – характерна для всіх ненасичених вуглеводнів А) приєднання водню C2H4+H2→C2H6 Б) приєднання галогенів C2H4+Cl2 →C2H4Cl2 В) приєднання води C2H4+H2O →C2H5OH Г) приєднання галоген оводнів правило Марковнікова: Гідроген приєднується до більш гідрогенізованого атома карбону CH3-CH=CH2 +HCl →CH3-CHCl-CH3 2.окиснення: А) повне окиснення (горіння) C2H4+3O2→2 CO2 +2H2O Б) часткове окиснення – знебарвлення розчину марганцівки – якісна реакція на ненасичені вуглеводні. 3C2H4+2KMnO4+4H2O → 2MnO2+3CH2OH-CH2OH +2KOH 3. полімеризація – послідовне сполучення однакових молекул у більші за розміром (полімери) CH2=CH2+ CH2=CH2 +CH2=CH2→ -CH2-CH2-CH2-CH2-CH2-CH2- → (-CH2-CH2-)n ,n – ступінь полімеризації
|
Гомологічний ряд |
||||||||
С2Н4 – етен (етилен) С3Н6 – пропен С4Н8 – бутен С5Н10 – пентен С6Н12 – гексен С7Н14 – гептен С8Н16 – октен С9Н18 – нонен С10Н20 - декен |
||||||||
Будова молекули етилену
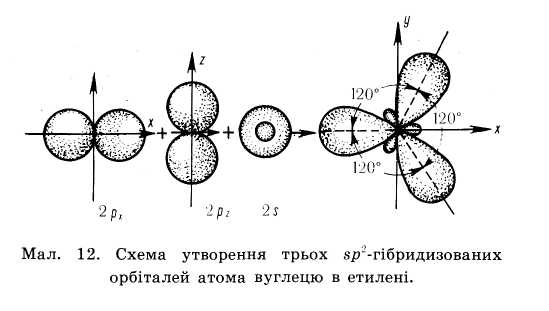
Приклади назв алкенів по міжнародній номенклатурі
СН3
С 6Н3 – С5 – С4Н2 – С3Н = С2Н– С1Н3 С1Н2 = С2Н – С3Н2 – С4Н2 – С5Н – СН3
СН3 С6Н2 – С7Н3
5,5 –диметилгекс-2-ен 5-метилгепт-1-ен.
ІV.Алкіни
Визначення |
Функціо- нальні групи |
Загальна формула |
Номенк- латурна назва |
Види ізомерії |
Будова |
Застосування |
Добування |
Фізичні і Хімічні властивості |
Алкіни – це ненасичені вуглеводні з одним потрійним зв’язком |
С Ξ С |
СnH2n-2 |
Нумерація починається з того краю де ближче знаходиться потрійний зв'язок ,після кореня пишеться номер карбону з якого починається потрійно зв'язок ,в кінці пишеться закінчення ин |
1.ізомерія карбонового ланцюга 2.ізомерія положення потрійного зв’язку 3.міжкласова ізомерія з дієнами |
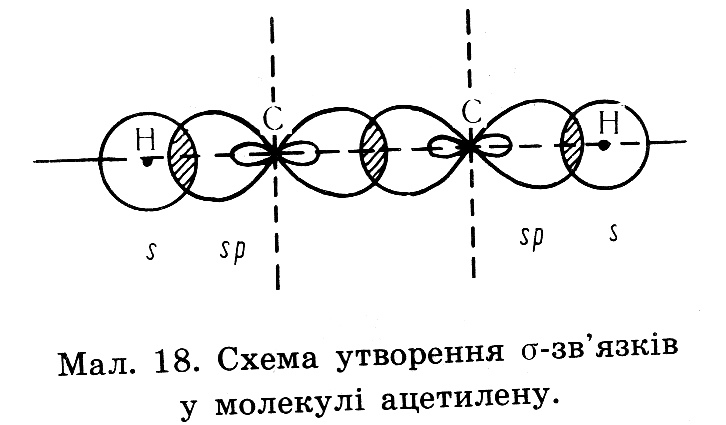
Два атоми Карбону, що приймають участь в утворенні потрійного зв’язку знаходяться в стані sр – гібридизації. Тобто із чотирьох існуючих орбіта лей кожного атома вирівнюють ся лише дві( одна s, та одна р-орбіта лі), і дві р – орбіталі лишаються не гібридизовані (мають форму гантелі). Дві гібридизовані орбіта лі кожного атома карбону розташовуються у вигляді двох прямих ліній на площині. Однією вершиною ці лінії перекриваються утворюючи δ-зв'язок інші орбіта лі утворюють δ- зв’язки з атомами гідрогенів
Не гібридизовані р-орбіталі обох атомів карбонів розташовуються перпендикулярно один одному утворюючи два π – зв'язок на двох взаємоперпендикулярних площинах, на перетині цих площин розташовується δ-звязок Отже потрійний зв'язок алкінів містить один δ-зв'язок і два π-зв'язка. δ-зв'язок міцніший ніж π-зв'язок.
|
1.сировина для синтезу оцтової кислоти, синтетичного каучуку, хлорвінілових і поліхлорвінілових пластмас. 2. виплавляння скла 3.зварювання та різання металів.
|
1. крекінг метану, при температурі 1500 0С 2СН4→С2Н2 +3Н2 2.карбідний метод СаС2 +2Н2О → С2Н2+Са(ОН)2 |
1.Реакція приєднання – характерна для всіх ненасичених вуглеводнів А) приєднання водню C2H2+H2→C2H4 C2H2+2H2→C2H6 Б) приєднання галогенів C2H2+2Cl2 →C2H4Cl4 В) приєднання води. Реакція Кучерова, відбувається в присутності каталізатора – солей ртуті C2H2+H2O →СН3СНО Г) приєднання галогеноводнів правило Марковнікова: Гідроген приєднується до більш гідрогенізованого атома карбону CH3-CΞCH +2HCl →CH3-CCl2-CH3 2.окиснення: А) повне окиснення (горіння) 2C2H2+5O2→4CO2 +2H2O Б) часткове окиснення – знебарвлення розчину марганцівки – якісна реакція на ненасичені вуглеводні. 3C2H2+8KMnO4→ 8MnO2+ 3CОOК-CОOК+2KOH +2Н2О 3.димеризація 2С2Н2→ СН2=СН-СΞСН 4.тримеризація
|
Гомологічний ряд |
||||||||
С2Н2 – етин (ацетилен) С3Н4 – пропин С4Н6– бутин С5Н8 – пентин С6Н10 – гексин С7Н12 – гептин С8Н14 – октин С9Н16 – нонин С10Н18 - декин |
||||||||
Приклади назв по міжнародній номенклатурі алкінів.
С2Н5 СН3
С 1Н Ξ С2 – С3Н2 – С4Н – С5 – С6Н – С7Н2 – С8Н3 С1Н3 – С2 Ξ С3 – С4Н2 – С5Н – С6Н3
СН3 СН3 СН3
5-етил-4,5,6-триметилокт-1-ин 5-метилгекс-2-ин
Будова молекули ацетилену (етину)
V. Дієни.
Визначення |
Функціо- нальні групи |
Загальна формула |
Номенк- латурна назва |
Види ізомерії |
Будова |
Застосування |
Добування |
Фізичні і Хімічні властивості |
Дієни - це ненасичені вуглеводні з двома подвійними зв’язкоми. Полімери – речовини молекули яких (макромолекули ) складаються з великої кількості груп атомів ( структурних ланок) зв’язаних між собою хімічними зв’язками. |
С=С-С=С CnH2n-2 С3Н4 – пропдієн С4Н6– бутдієн С5Н8 – пентдієн С6Н10 – гексдієн С7Н12 – гептдієн С8Н14 – октдієн С9Н16 – нондієн С10Н18 - декдієн |
Нумерація починається з того краю де ближче знаходиться подвійний зв'язок ,після кореня пишеться номери карбонів з яких починаються подвійні зв'язки ,в кінці пишеться закінчення дієн |
1.ізомерія карбонового ланцюга 2.ізомерія положення подвійного зв’язку 3. просторова ізомерія 4.міжкласова ізомерія з алкінами. |
Два атоми Карбону, що приймають участь в утворенні подвійного зв’язку знаходяться в стані sр2 – гібридизації. Тобто із чотирьох існуючих орбіта лей кожного атома вирівнюють ся лише три ( одна s, та дві р орбіта лі), і одна р – орбіталь лишається не гібридизована (має форму гантелі). Три гібридизовані орбіта лі кожного атома карбону розташовуються у вигляді двох рівносторонніх трикутників на площині. Однією вершиною ці трикутники перекриваються утворюючи δ-зв'язок інші орбіта лі утворюють δ- зв’язки з атомами гідрогенів
Не гібридизовані р-орбіталі обох атомів карбонів розташовуються перпендикулярно площині δ-звязків , перекриваються над і під площиною ,утворюючи π – зв'язок. Отже подвійний зв'язок алкенів містить один δ-зв'язок і один π-зв'язок. δ-зв'язок міцніший ніж π-зв'язок.
|
1.дієни використовують для органічного синтезу канчуків , полімерів та пластмас Найважливіші дієни: дивініл ізопрен
|
1. ізопрен – природній каучук ,із соку дерева гівеї. 2. синтетичний каучук(метод Лебедева)
|
1.Реакція приєднання – характерна для всіх ненасичених вуглеводнів А) приєднання водню C4H6+2H2→C4H10 Б) приєднання галогенів C4H6+2Cl2 →C4H6Cl4 В) приєднання води C4H6+H2O →C4H8(OH)2 Г) приєднання галоген оводнів правило Марковнікова: Гідроген приєднується до більш гідрогенізованого атома карбону CH2=СН-CH=CH2 +2HCl → CH3-CHCl-СНCl -CH3 2.окиснення: А) повне окиснення (горіння) 2C4H6+11O2→8CO2 +6H2O Б) часткове окиснення – знебарвлення розчину марганцівки – якісна реакція на ненасичені вуглеводні. 3. полімеризація – послідовне сполучення однакових молекул у більші за розміром (полімери) n CH2=CH-CH=CH2 → (-CH2-CH=CH-CH2-) n → ,n – ступінь полімеризації При полімеризації дієнів утворюються каучуки.
|
|