
- •1 Комплекс авиационного вооружения
- •Краткая история развития авиационных боеприпасов.
- •Системные требования к кав
- •Явение взрыва
- •Классификация взрывчатых веществ
- •Удельная энергия вв
- •2.3 Температура взрыва
- •Удельный объем продуктов взрыва
- •2.5 Давление продуктов взрыва
- •2.6 Чувствительность вв
- •2.6.1 Чувствительность к тепловому импульсу
- •2.6.2 Чувствительнось к удару
- •2.6.3 Критические напряжения
- •2.6.4 Чувствительность к детонационному импульсу
- •2.7 Стойкость вв
- •2.7.1 Методы испытания порохов на стойкость
- •2.8 Скорость детонации
- •2.9 Бризантное действие вв
- •2.10 Фугасное действие вв
- •2.11 Бризантные взрывчатые вещества (бвв)
- •2.11.1 Основные виды бвв Однородные бвв
- •2.12 Инициирующие взрывчатые вещества (ивв)
- •2.13 Метательные взрывчатые вещества
- •2.14. Пиротехнические взрвычатые вещества
- •3 Проникающее действие боеприпасов
- •Удар о поверхность среды;
- •Собственно проникание;
- •Проникание при наличии откола или сквозное пробивание (при среде конечной толщины).
- •3.1 Проникание в сплошные среды
- •В нашем случае ускорением свободного падения можно пренебречь, т.К.
- •Ввиду того, что начальным участком можно пренебречь.
- •3.2 Пробитие многослойных преград
- •4 Бронебойное действие боеприпасов
- •Коэффициент для гомогенной брони составляет 1600…2000, для гетерогенной – 2000…3000.
- •5 Проникание при высоких скоростях удара
- •6 Рикошетирование боеприпасов
- •Отсюда, подставив в зачение , получим
- •Смещение центра тяжести боеприпаса вперед.
- •Притупление головной части или выемка в головной части.
- •Применение тормозных устройств.
- •7 Фугасное действие боеприпасов
- •Подставляя значение в выражение для скорости движения газов, получим
- •7.1 Параметры водушной ударной волны
- •7.2 Удельный импульс ударной волны. Общие принципы разрушающего действия при взрыве в воздухе
- •7.3 Разрушающее действие подводного взрыва
- •7.4 Взрыв заряда в грунте
- •7.5 Воронка в грунте
- •8 Кумулятивное действие боеприпасов
- •8.1 Физическая сущность кумулятивного действия
- •8.2 Гидродинамическая теория кумуляция.
- •8.3 Бронебойное и заброневое действие кумулятивных зарядов
- •8.4 Факторы, влияющие на кумулятивное действие
- •8.5 Особенности формирования и действия кумулятивных дально- бойных зарядов
- •9 Осколочное действие авиационных боеприпасов
- •9.1 Физическая картина взрыва заряда в оболочке
- •9.2 Закон дробления оболочки на осколки
- •9.3 Закон разлета осколков
- •9.4 Начальная скорость осколков
- •9.5 Баллистика осколков
- •9.6 Поражающее действие осколков
- •9.6.1. Пробивное действие осколков
- •10 Система авиационных боеприпасов
- •10.1 Боеприпасы бомбардировочного вооружения
- •10.2 Аэродинамические нагрузки, действующие на авиабомбу в свободном полете
- •10.3 Авиабомбы для бомбометания с малых и предельно малых высот
- •10.4 Авиабомбы на основе топливновоздушной смеси
- •10.5 Управляемые (корректируемые) авиационные бомбы
- •10.5.1. Классификация управляемых авиационных бомб
- •10.5.2. Состояние и тенденции развития уаб (каб)
- •10.5.3 Конструкция и принцип действия типовых образцов
- •10.5.3.1 Уаб с полуактивными лазерными системами наведения
- •Семейство «Пейв Уэй-I»
- •Семейство «Пейв Уэй-II»
- •Семейство «Пейв Уэй-III»
- •10.5.4 Типовые схемы боевого применения уаб с лазерными сн
- •10.6 Уаб с телевизионными (тепловизионными) системами наведения
- •10.6.1 Типовые схемы боевого применения уаб с телевизионными сн в составе уак
- •11 Авиационное контейнерно-кассетное оружие
- •11.1 Несбрасываемые контейнеры
- •11.2 Управляемые кассетные системы.
- •11.3 Разовые бомбовые кассеты
- •12 Артиллерийские боеприпасы
- •12.1 Снаряды к авиационным пушкам.
- •Корпус снаряда, 2 – ведущий поясок
- •12.2 Пули к авиационным пулеметам.
- •13 Неуправляемые авиационные ракеты
- •– Эффективная скорость истечения
- •14 Авиационные взрыватели
- •14.1 Назначение и классификация взрывателей
- •14. 2 Авиационные взрыватели контактного и дистанционного действия
- •14.2.1 Классификация взрывателей контактного действия
- •14.2.2 Принципы устройства и действия основных механизмов контактных взрывателей механического типа
- •14.21. Схема противосъемного устройства
- •14.2.3 Особенности устройства и действия контактных взрывателей электрического типа
- •14.3 Авиационные взрыватели дистанционного действия
- •14.4 Авиационные неконтактные взрыватели
- •14.4.1. Общие сведения о неконтактных взрывателях, их классификация и основные характеристики
- •14.4.2 Неконтактные радиовзрыватели
- •14.4.2.1. Неконтактные рв доплеровского типа
- •14.4.2.2 Принцип действия импульсных рв
- •14.4.2.3 Принцип действия импульсно-доплеровских рв
- •14.4.2.4 Неконтактные оптические взрыватели
- •Библиографический список
2.3 Температура взрыва
Температура
взрыва
![]() -
максимальная
температура, до которой нагреваются
продукты взрыва в результате взрывчатого
превращения ВВ.
-
максимальная
температура, до которой нагреваются
продукты взрыва в результате взрывчатого
превращения ВВ.
Полагая процесс адиабатным, в котором вся энергия расходуется на нагрев продуктов детонации, можно записать
![]() ,
где
,
где
![]() - средняя теплоемкость продуктов взрыва.
- средняя теплоемкость продуктов взрыва.
Так как теплоемкость зависит от температуры, зависимость может быть представлена в виде
![]()
Для практических задач достаточно первых двух членов
Отсюда
![]() (2.3)
(2.3)
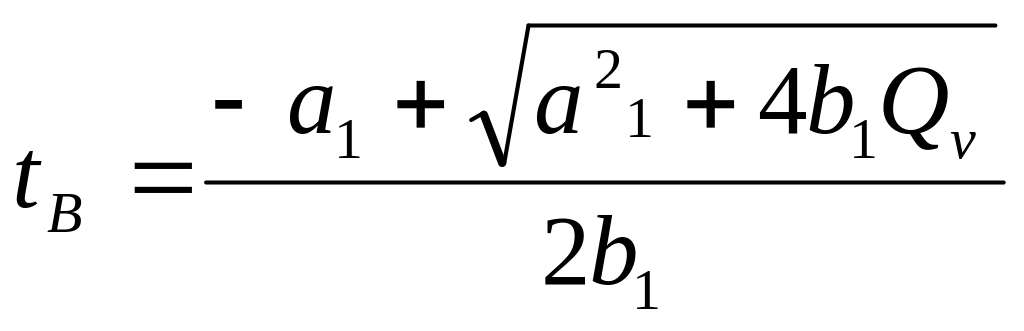 (2.4)
(2.4)
Значения
![]() и
и
![]() приведены в таблице 2.3.
приведены в таблице 2.3.
Таблица 2.3
Продукты взрыва
|
, Дж/моль (оС) |
, Дж/моль (оС)2 |
Четырехатомные газы |
41,86 |
1,8810-3 |
Двухатомные газы |
20,09 |
1,8810-3 |
Пары воды |
16,74 |
9,010-3 |
Углекислый газ |
37,68 |
2,4310-3 |
Пары ртути |
12,56 |
0 |
Твердые вещества |
26,79 |
0 |
Пример
Определить температуру взрыва гексогена
Уравнение превращения имеет вид
![]() (вода
парообразная)
(вода
парообразная)
1. Определим ВВ по таблице 2
![]()
![]()
![]()
![]()
![]()
![]()
2. Определим
![]()
Определим продуктов взрыва
![]()
![]()
![]()
![]()
Определим
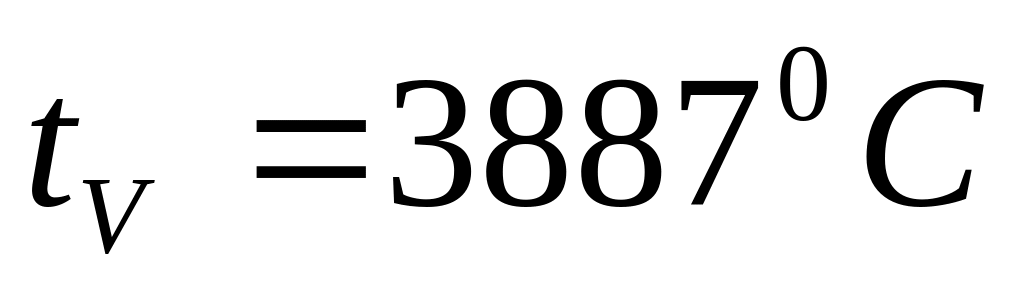
Удельный объем продуктов взрыва
Удельным объемом продуктов взрыва Vo называется объем, который занимают продукты взрыва 1 кг ВВ при нормальных условиях
(Р = 1 атм, t = 0oC).
Уравнение взрывчатого превращения можно записать
![]() ,
(2.5)
,
(2.5)
где
![]() - масса моля ВВ,
- масса моля ВВ,
![]() -
количество молей ВВ,
-
количество молей ВВ,
![]() - масса молей продуктов взрыва,
- масса молей продуктов взрыва,
![]() - количество молей продуктов взрыва.
- количество молей продуктов взрыва.
Зная количество молей газообразных продуктов взрыва можно определить удельный объем продуктов взрыва
![]() (дм/кГ)
(2.6)
(дм/кГ)
(2.6)
22, 4103 – объем, который занимает один моль при t = 0oC и Р = 98,0665 кПа
Для
нитроглицерина
![]()
Удельный объем газов нескольких ВВ приведен в таблице 2.4.
Таблица 2.4
Тип ВВ |
вв, г/м3 |
Vo, л/кг |
Гексоген |
1,8 |
890 |
ТЭН |
1,65 |
790 |
Тротил |
1,5 |
750 |
Гремучая ртуть |
3,77 |
300 |
2.5 Давление продуктов взрыва
В идеальном случае, когда при взрыве все ВВ превращается в газообразные продукты, которые ведут себя как идеальный газ, для описания их состояния применимо уравнение Клайперона-Менделеева.
![]() (2.7)
(2.7)
- число молей газа.
![]() ,
,
где
![]() -
количество молей газообразных продуктов,
образующихся при взрыве 1 кГ ВВ;
-
количество молей газообразных продуктов,
образующихся при взрыве 1 кГ ВВ;
![]() - масса ВВ.
- масса ВВ.
Отсюда
![]() ,
обозначая
,
обозначая
![]() ,
а
,
а
![]() ,
получим
,
получим
![]() ,
где
,
где
![]() - сила ВВ (кДж/кГ),
- сила ВВ (кДж/кГ),
![]() - плотность заряжания.
- плотность заряжания.
Но
при
![]() эта формула дает большие погрешности.
Необходимо в этом случае учитывать
молекулярную структуру газов. Для
больших давлений используется формула
Абеля, которая выводится из уравнения
Ван-дер-Ваальса
эта формула дает большие погрешности.
Необходимо в этом случае учитывать
молекулярную структуру газов. Для
больших давлений используется формула
Абеля, которая выводится из уравнения
Ван-дер-Ваальса
![]() ,
(2.8)
,
(2.8)
где
![]()
![]() - поправка в давлении, учитывающая
притяжение молекул,
- поправка в давлении, учитывающая
притяжение молекул,
![]() -
коволюм - объем, пропорциональный объему
молекул.
-
коволюм - объем, пропорциональный объему
молекул.
По
Ван-дер-Ваальсу коволюм равен учетверенному
объему молекул, или
![]() ,
где
,
где
![]() -
удельный объем продуктов взрыва.
-
удельный объем продуктов взрыва.
Пренебрегая
поправкой
и решая уравнение относительно
![]() получим
получим
![]() (2.9)
(2.9)
Умножая
и деля на 1/![]() получим формулу Абеля, позволяющую
вычислять давление до 6108
Па.
получим формулу Абеля, позволяющую
вычислять давление до 6108
Па.
![]() ,
(2.10)
,
(2.10)
где - плотность заряжания (кГ/дм3), - сила ВВ (кДж/кГ), ,
![]() -
удельный объем продуктов взрыва.
-
удельный объем продуктов взрыва.
Подставляя
в формулу значение
![]()
![]() , где
, где
![]() -
масса заряда;
-
масса заряда;
- объем камеры сгорания и решая относительно получим формулу внутренней баллистики
![]() ,
(2.11)
,
(2.11)
позволяющую рассчитать массу пороха, необходимую для получения давления при постоянном объеме.
