
- •Оглавление
- •Глава 1. Литературный обзор
- •Глава 2. Элементарная теория ударных волн
- •Моделирование ударной волны
- •Уравнение энергии
- •Глава 3. Ударные волны в идеальном газе Энтальпия
- •Адиабата Гюгонио
- •Уравнение Гюгонио
- •Глава 4. Детонация
- •Численное моделирование детонационного процесса
- •Прямая Михельсона
- •Глава 5. Энергетическое использование детонации
- •Электрогенератор на идд
- •Численное моделирование цикла идгтд
- •Глава 6. Приложение идд
- •Список Литературы
Прямая Михельсона
Вспомним
соотношение, выведенное в статье об
ударных волнах:


При
стационарном движении газа оно выполнимо
для любых контрольных поверхностей,
проведённых внутри зоны протекания
реакции, иначе нарушается условие
стационарности процесса. Отсюда скорость
распространения
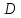 одинакова
для всех контрольных поверхностей. Это
соотношение выведено, как нам известно,
только из законов сохранения массы и
количества движения, а поэтому никак
не зависит ни от энергии реакции, ни
от свойств реагирующих веществ или
продуктов реакции. На (
одинакова
для всех контрольных поверхностей. Это
соотношение выведено, как нам известно,
только из законов сохранения массы и
количества движения, а поэтому никак
не зависит ни от энергии реакции, ни
от свойств реагирующих веществ или
продуктов реакции. На (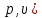 -диаграмме
изобразим процессы, происходящие в
детонационной волне с заданной скоростью
-диаграмме
изобразим процессы, происходящие в
детонационной волне с заданной скоростью
 .
Все
они будут отвечать точкам прямой,
выражаемой уравнением (его не трудно
получить из уравнения скорости
распространения фронта ударной волны,
выведенного в теории ударных волн):
.
Все
они будут отвечать точкам прямой,
выражаемой уравнением (его не трудно
получить из уравнения скорости
распространения фронта ударной волны,
выведенного в теории ударных волн):

Эта
прямая называется прямой Михельсона.
Рассмотрим фиг.13: состояние
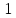 непосредственно позади фронта ударной
волны
достигается из состояния
непосредственно позади фронта ударной
волны
достигается из состояния
 скачкообразно. Этот переход происходит
на длине одного свободного пробега
молекулы газа, но вещество отнюдь не
проходит все состояния, отвечающие
прямой
скачкообразно. Этот переход происходит
на длине одного свободного пробега
молекулы газа, но вещество отнюдь не
проходит все состояния, отвечающие
прямой
 .
Переход из точки
.
Переход из точки
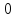 в точку
в точку
 описывается
адиабатой Гюгонио (на фиг.13 это кривая
описывается
адиабатой Гюгонио (на фиг.13 это кривая
 ).
Непосредственно за фронтом ударной
волны, т. е. за контрольной поверхностью
).
Непосредственно за фронтом ударной
волны, т. е. за контрольной поверхностью
 ,
начинается химическая реакция,
где и происходит выделение тепла.
Если построить адиабату Гюгонио,
соответствующую промежуточному
состоянию, то она должна лежать выше
адиабаты
,
начинается химическая реакция,
где и происходит выделение тепла.
Если построить адиабату Гюгонио,
соответствующую промежуточному
состоянию, то она должна лежать выше
адиабаты
 ,
поскольку продукты реакции обладают
повышенным содержанием энергии и на
(
,
поскольку продукты реакции обладают
повышенным содержанием энергии и на
( -диаграмме
этому состоянию должны соответствовать
точки с более высоким значением энтальпии.
Эта адиабата изображена пунктиром.
Однако, необходимо, чтобы состояние
изменялось вдоль прямой
-диаграмме
этому состоянию должны соответствовать
точки с более высоким значением энтальпии.
Эта адиабата изображена пунктиром.
Однако, необходимо, чтобы состояние
изменялось вдоль прямой
 .
Мы
достигаем пунктирной адиабаты,
перемещаясь от точки
.
Мы
достигаем пунктирной адиабаты,
перемещаясь от точки
 вправо; химическая реакция и выделение
тепла за фронтом ударной волны
сопровождаются уменьшением плотности
и давления, т. е. волной разрежения.
вправо; химическая реакция и выделение
тепла за фронтом ударной волны
сопровождаются уменьшением плотности
и давления, т. е. волной разрежения.
Теперь
рассмотрим
адиабату, отвечающую полной энергии
взрывчатого превращения газа
 .
Пусть
детонационная волна распространяется
свободно (без дополнительного сжатия
сзади или искусственного поджигания
впереди фронта), в таком случае ее
адиабата должна
касаться прямой
.
Пусть
детонационная волна распространяется
свободно (без дополнительного сжатия
сзади или искусственного поджигания
впереди фронта), в таком случае ее
адиабата должна
касаться прямой
 .
.
Упростим доказательство этого утверждения, предварительно рассмотрев некоторые его следствия.
На
рис. 4 совместно изображены адиабата
 и адиабата
и адиабата
 ,
которая отвечает
полному выделению тепла.
,
которая отвечает
полному выделению тепла.
Учитывая,
что энтальпия состояния, отвечающего
полному выделению энергии, уже не
столь явно зависит от химической энергии
 ,
получим уравнение адиабаты
,
получим уравнение адиабаты
 .
В
общем виде, выражая эту энтальпию через
.
В
общем виде, выражая эту энтальпию через
 ,
мы
получим:
,
мы
получим:

Это уравнение особенно просто выглядит для газа с теплоёмкостью, не зависящей от температуры, потому что тогда энтальпия выражается следующим образом:


При подстановке этих выражений в выражение общего вида получается уравнение искомой адиабаты.
Это
уравнение справедливо для всех её точек,
но если интересоваться специально теми
точками, которые близки к упомянутой
точке касания, то давлением и температурой
исходного газа
 ,
,
 в выражении общего вида можно пренебречь
по сравнению с теми же величинами для
точки касания; тогда
в выражении общего вида можно пренебречь
по сравнению с теми же величинами для
точки касания; тогда

Выразим
 :
:

Аналогичное
уравнение для адиабаты
 есть
есть

Сравнивая
числители этих выражений, мы видим, что
кривая для полного выделения энергии
лежит гораздо выше кривой
 ,
так как
,
так как
 гораздо
больше начальной энтальпии. Пересечение
кривых *) отвечало бы таким
давлениям,
которые в детонационной волне не
наблюдаются.
гораздо
больше начальной энтальпии. Пересечение
кривых *) отвечало бы таким
давлениям,
которые в детонационной волне не
наблюдаются.
На
фиг.14 видно прежде всего, что скорость,
отвечающая прямой
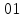 ,
вообще наименьшая из возможных, имеющих
общую точку с адиабатой
,
вообще наименьшая из возможных, имеющих
общую точку с адиабатой
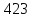 .
Всякая другая прямая
.
Всякая другая прямая
 ,
пересекающая обе адиабаты, имеет больший
наклон и отвечает поэтому большей
скорости*). Между тем, стационарный
процесс, отвечающий расширению по прямой
,
пересекающая обе адиабаты, имеет больший
наклон и отвечает поэтому большей
скорости*). Между тем, стационарный
процесс, отвечающий расширению по прямой
 должен
приводить вещество в состояние, которому
соответствует полное выделение тепла,
просто в силу определения этого последнего
состояния.
должен
приводить вещество в состояние, которому
соответствует полное выделение тепла,
просто в силу определения этого последнего
состояния.
Итак, скорость детонации является минимальной из всех возможных при стационарных режимах распространения химической реакции ударной волной.
Состояние
реагирующей смеси меняется вдоль прямой
 непрерывным образом. Состав смеси в
каждой точке определяется из уравнений
химической кинетики. Так как реакция
протекает необратимо, энтропия всей
реагирующей. смеси возрастает
необратимым образом и достигает максимума
на прямой
непрерывным образом. Состав смеси в
каждой точке определяется из уравнений
химической кинетики. Так как реакция
протекает необратимо, энтропия всей
реагирующей. смеси возрастает
необратимым образом и достигает максимума
на прямой
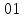 в точке касания
в точке касания
 ,
отвечающей
полному выделению тепла. Существенно,
что настоящий максимум достигается
именно на этой прямой, касающейся верхней
адиабаты, а не пересекающейся с ней,
как, например, в точке
,
отвечающей
полному выделению тепла. Существенно,
что настоящий максимум достигается
именно на этой прямой, касающейся верхней
адиабаты, а не пересекающейся с ней,
как, например, в точке
 прямой
прямой
 (фиг.14).
(фиг.14).
