
- •Оглавление
- •Глава 1. Литературный обзор
- •Глава 2. Элементарная теория ударных волн
- •Моделирование ударной волны
- •Уравнение энергии
- •Глава 3. Ударные волны в идеальном газе Энтальпия
- •Адиабата Гюгонио
- •Уравнение Гюгонио
- •Глава 4. Детонация
- •Численное моделирование детонационного процесса
- •Прямая Михельсона
- •Глава 5. Энергетическое использование детонации
- •Электрогенератор на идд
- •Численное моделирование цикла идгтд
- •Глава 6. Приложение идд
- •Список Литературы
Уравнение энергии
Теперь получим уравнение энергии.
По условию газ не отдаёт и не получает тепла. Тогда, согласно I закону термодинамики:


Пусть:
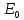 – начальная
внутренняя энергия единицы массы газа
– начальная
внутренняя энергия единицы массы газа
 – внутренняя
энергия единицы массы сжатого газа
– внутренняя
энергия единицы массы сжатого газа
 – кинетическая
энергия единицы массы сжатого газа
– кинетическая
энергия единицы массы сжатого газа
 – вся
масса сжатого газа
– вся
масса сжатого газа
Тогда:
 – полное
изменение энергии газа при сжатии
– полное
изменение энергии газа при сжатии
 – работа
внешней силы, произведённая поршнем
над газом за время t.
– работа
внешней силы, произведённая поршнем
над газом за время t.
Таким образом, уравнение энергии имеет следующий вид:

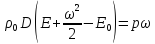



Глава 3. Ударные волны в идеальном газе Энтальпия
Введем
понятие энтальпии. Энтальпия ( )
– это тепловая функция, отражающая
состояние макроскопической системы в
условиях термодинамического равновесия.
В качестве независимых переменных в
ней используются такие термодинамические
характеристики газа, как:
)
– это тепловая функция, отражающая
состояние макроскопической системы в
условиях термодинамического равновесия.
В качестве независимых переменных в
ней используются такие термодинамические
характеристики газа, как:
 – энтропия
(понятие в термодинамике, введенное для
обозначения меры необратимого рассеяния
энергии)
– энтропия
(понятие в термодинамике, введенное для
обозначения меры необратимого рассеяния
энергии)
 – давление
– давление
 – число
частиц (моль) вещества
– число
частиц (моль) вещества
Если упростить, то энтальпия — это энергия, доступная для преобразования в теплоту при определённом постоянном давлении.
Рассмотрим
термомеханическую систему, состоящую
из цилиндра высотой
 ,
наполненного газом, и плотно прилегающего
гладкого поршня площадью
,
наполненного газом, и плотно прилегающего
гладкого поршня площадью
 с грузом весом
с грузом весом
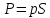 ,
который уравновешивает давление внутри
цилиндра с газом. Энтальпия данной
системы состоит из суммы внутренней
энергии газа
,
который уравновешивает давление внутри
цилиндра с газом. Энтальпия данной
системы состоит из суммы внутренней
энергии газа
 и потенциальной энергии поршня с грузом
и потенциальной энергии поршня с грузом
 ,
где
,
где
 – объем цилиндра:
– объем цилиндра:

То есть, энтальпия представляет собой сумму внутренней энергии тела и работы, которую необходимо над телом совершить, чтобы ввести определенное тело в окружающую среду, имеющую конкретное давление, находящуюся в равновесном состоянии. Являясь одним из термодинамических потенциалов, энтальпия, аналогично внутренней энергии, принимает конкретные значения для каждого определенного состояния, т.е. является функцией состояния. Тогда мы можем говорить, что:

Вычислим изменение энтальпии для единицы массы через уравнение энергии:


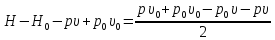


Адиабата Гюгонио
Будем
считать термодинамические свойства
вещества известными. Выразим энергию
 как функцию удельного объема и давления:
как функцию удельного объема и давления:
 .
Подставив данное выражение в уравнение
энергии, получим уравнение некоторой
кривой в плоскости (
.
Подставив данное выражение в уравнение
энергии, получим уравнение некоторой
кривой в плоскости ( ,
для которой начальные давление и объем
являются параметрами. Очевидно, что
кривая проходит через точку
,
для которой начальные давление и объем
являются параметрами. Очевидно, что
кривая проходит через точку
 ,
т.к. при подстановке этой координаты в
уравнение энергии, оно обнуляется.
,
т.к. при подстановке этой координаты в
уравнение энергии, оно обнуляется.
Эта
кривая называется адиабатой Гюгонио и
отражает набор состояний газа, получаемых
путем однократного сжатия из состояния
 при переходе через фронт ударный волны
при переходе через фронт ударный волны
 .
На этой поверхности скачкообразно
изменяются плотность и удельный объем
вещества. Такое сжатие носит название
ударного сжатия.
.
На этой поверхности скачкообразно
изменяются плотность и удельный объем
вещества. Такое сжатие носит название
ударного сжатия.
Сам
процесс сжатия вещества отнюдь не
происходит строго по адиабате Гюгонио.
Наоборот, газ, сжимаемый ударной волной,
заведомо не проходит тот ряд состояний,
который в плоскости ( отвечает набору точек, лежащих на
адиабате Гюгонио. Она лишь отображает
совокупность всех возможных конечных
состояний сжатия
отвечает набору точек, лежащих на
адиабате Гюгонио. Она лишь отображает
совокупность всех возможных конечных
состояний сжатия
 при данных
при данных
 .
.
Разделим
процесс ударного сжатия на два этапа.
Первая волна сжатия со скачком давления
 .
Вторая волна сжатия, идущая по веществу
после первой, со скачком давления
.
Вторая волна сжатия, идущая по веществу
после первой, со скачком давления
 .
Тогда для второй волны начальными
параметрами среды будут
.
Тогда для второй волны начальными
параметрами среды будут
 .
Это значит, что адиабата Гюгонио для
первого скачка уплотнения не будет
совпадать с адиабатой для второго скачка
уплотнения, т.к. начальные состояния
будут разными. Более того, конечный
объем газа после сжатия второй ударной
волной не
равен, а вообще говоря, меньше объема
до которого сожмётся вещество, если по
нему пройдёт однократная волна со
скачком давления
.
Это значит, что адиабата Гюгонио для
первого скачка уплотнения не будет
совпадать с адиабатой для второго скачка
уплотнения, т.к. начальные состояния
будут разными. Более того, конечный
объем газа после сжатия второй ударной
волной не
равен, а вообще говоря, меньше объема
до которого сожмётся вещество, если по
нему пройдёт однократная волна со
скачком давления
 .
.
Таким образом, ударное сжатие имеет существенные отличия от изэнтропического (сжатия при постоянной энтропии). Изэнтропическое сжатие обладает свойством аддитивности, т.е. конечное состояние вещества совершенно не зависит от деления процесса на этапы, наоборот, определяется только начальным состоянием и полным изменением давления. Таким образом, изэнтропическое сжатие обратимо, а ударное – необратимо.
