4.5 Свойства и применения пленок оксида кремния
Оксид кремния
относится к числу наиболее высококачественных
диэлектриков. Он имеет диэлектрическую
проницаемость
![]() 3.9,
3.9,
![]() 1.46,
1.46,
![]() 2
.107
В/см (в слоях
2
.107
В/см (в слоях
![]() 200
нм). У более толстых слоев
200
нм). У более толстых слоев
![]() уменьшается пропрорционально
уменьшается пропрорционально
![]() .
.
Роль, которую выполняет пленка SiO2 определяет возможность использования того или иного метода ее получения.
Для использования в качестве межуровневой изоляции или защитного слоя, наносимого поверх металлизации можно использовать химическое осаждение из газовой фазы. Защитные слои часто наносятся также пиролизом ТЭОС.
Слои, используемые в качестве масок при локальном легировании, обычно получают термическим окислением. На практике нередко используется комбинированный режим окисления, когда начальный этап окисления ведется в атмосфере сухого O2, затем в атмосфере паров воды, после чего опять следует окисление в сухом O2. Длительности этих трех процессов выбираются приблизительно равными. Первый этап окисления задает структуру границы раздела Si–SiO2. Во время второго этапа формируется основная толща пленки. Третий этап является термообработкой, в процессе которой понижается концентрация растворенной в пленке воды, толщина пленки при этом увеличивается незначительно. Такая методика позволяет сравнительно быстро получать слои SiO2, по свойствам приближающиеся к получаемым в атмосфере сухого O2. Для получения маскирующих слоев используют также методы химического осаждения из газовой фазы.
Наиболее высококачественные слои SiO2 для МДП структур получают только термическим окислением в атмосфере сухого O2. Для МДП структур на основе иных полупроводниковых соединений используют методы химического осаждения из газовой фазы или анодирования.
Параметр |
Значение параметра |
Плотность, г/см3 |
2.2 |
Показатель преломления |
1.46 |
Диэлектрическая постоянная |
3.82 |
Ширина запрещенной зоны, эВ |
8.9 |
Удельное сопротивление постоянному току при T = 25 ºС, Ом*см |
1014-1016 |
Скорость травления в буферном растворе HF, нм/мин |
100 |
Линия ИК поглощения, мкм |
9.3 |
Коэффициент теплового расширения, С-1 |
5*10-7 |
Механические напряжения в окисле, дин/см2 |
3*109 |
4.6 Модель процесса
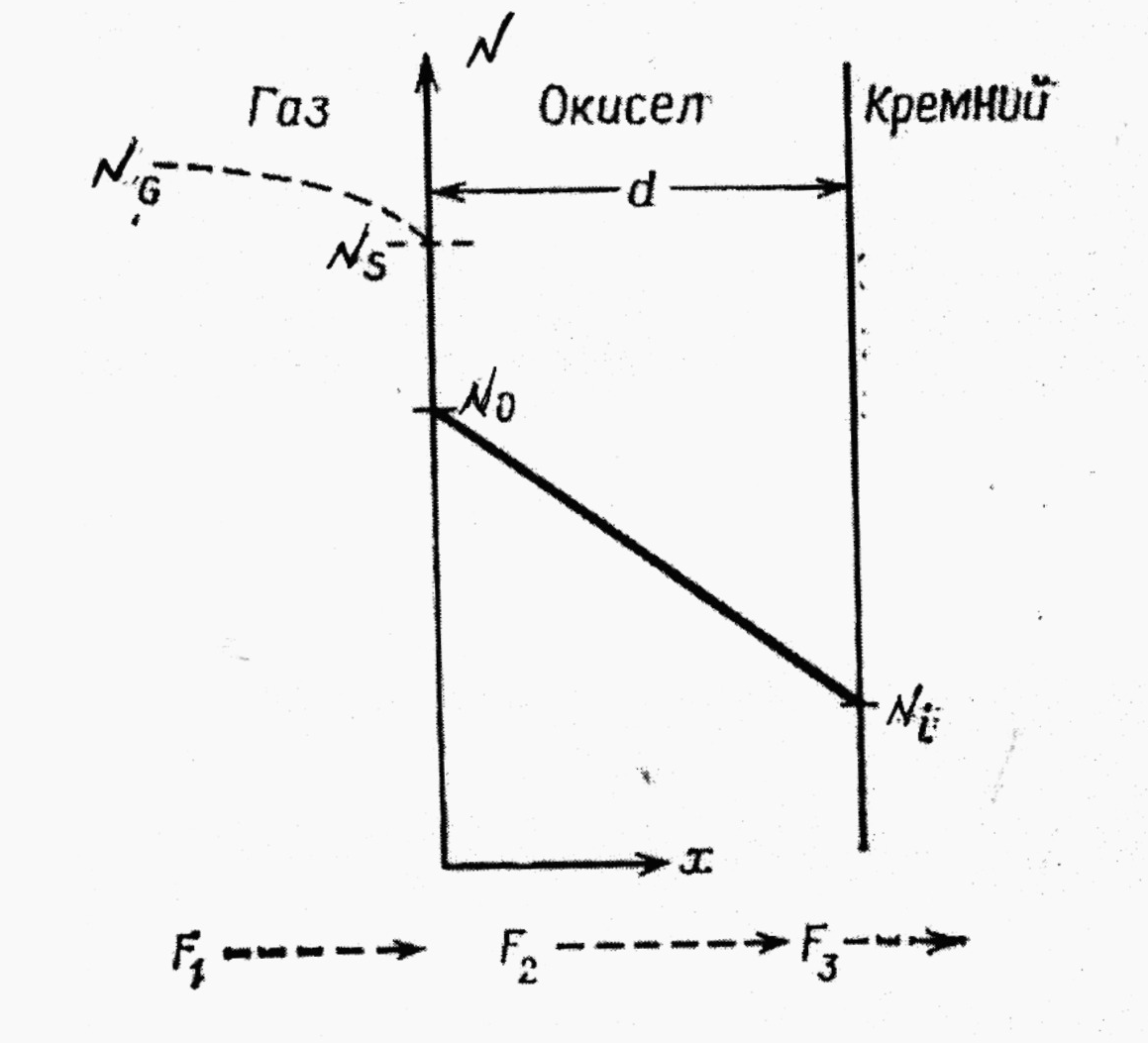
Кинетика процесса окисления Si наиболее точно описывается моделью Дила и Гроува (см. С. Зи Технология СБИС). Она применима для температурного диапазона 700–1300 °С, парциальных давлений O2 (0,2—1,0)∙105 Па и толщины окисных пленок 30–2000 нм в атмосфере, состоящей из кислорода и (или) паров воды. Здесь мы рассмотрим более простую модель. Пусть на поверхности Si уже есть пленка некоторой толщины и примем, что нарастание новых слоев пленки идет на границе раздела пленка – Si (рис. 4.2).
В этом случае окислитель только диффундирует сквозь пленку, не накапливаясь в ней. Иными словами поток атомов окислителя j постоянен по всей ее толще, а градиент концентрации постоянен по толще пленки.
|
Рис. 4.2. Рост Si02 |
Поэтому первое уравнение для расчета толщины пленки (x) записывается в виде:
![]() (4.2)
(4.2)
Здесь
![]() и
и
![]() – концентрации окислителя у внешней
границы SiO2
и у ее границы раздела с Si
соответственно.
– концентрации окислителя у внешней
границы SiO2
и у ее границы раздела с Si
соответственно.
Второе уравнение отражает наличие химической реакции образования SiO2:
![]() (4.3)
(4.3)
Здесь k – постоянная равновесия химической реакции, которая учитывает свойства взаимодействующих сред, а при окислении монокристаллов и их ориентацию.
Третье уравнение
отражает скорость наращивания пленки
и
![]() записывается
в виде:
записывается
в виде:
![]() (4.4)
(4.4)
В этом уравнении
![]() есть
концентрация атомов окислителя,
необходимых для образования единичного
объема пленки.
есть
концентрация атомов окислителя,
необходимых для образования единичного
объема пленки.
Исключив из этих уравнений j и , получим:
![]() (4.5)
(4.5)
После интегрирования получим:
![]() (4.6)
(4.6)
Здесь
![]() – это постоянная интегрирования,
отражающая наличие пленки к моменту
начала окисления.
– это постоянная интегрирования,
отражающая наличие пленки к моменту
начала окисления.
Эта простейшая модель не учитывает некоторых важных моментов.
Полагают, что кислород диффундирует в форме однократно отрицательно заряженных ионов О2-. Процессу перехода кислорода из атмосферы, где он находится в виде молекул О2 в состояние ионов, диффундирующих в оксиде, соответствует химическая реакция
О2 ↔ О2- + e+.
Освобождающиеся при этом электроны или дырки могут захватываться на столь глубокие уровни, что оказываются менее подвижными, чем ионы. При этом в пленке образуется электрическое поле, тормозящее диффузию ионов.
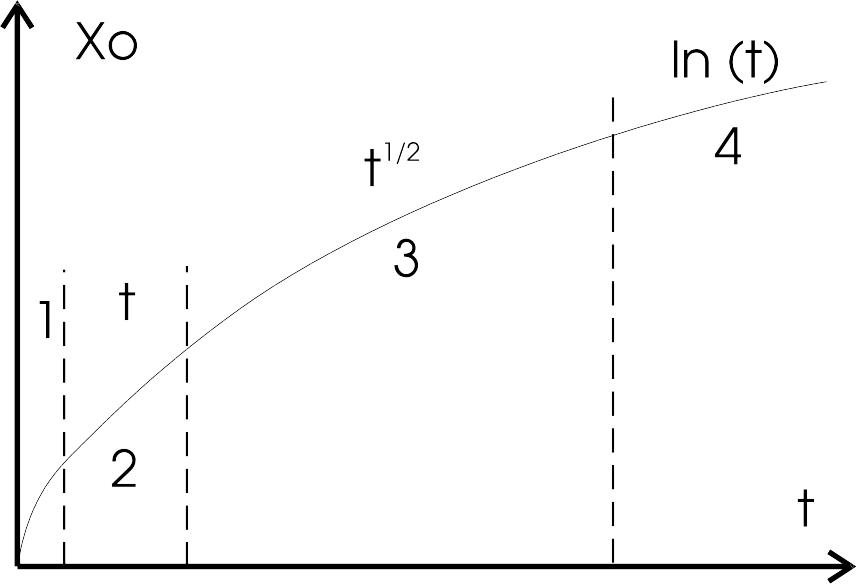
На начальных этапах окисления (см. участок 1, рис. 4.3), когда пленка еще слишком тонкая (мал член с x2), возможно и непосредственное взаимодействие окисляемого материала с окислителем, находящимся в состоянии, характерном для окружающей среды, затем линейный участок (2), плавно переходящий в параболический (3), толщина пленки растет пропорционально времени окисления, скорость роста лимитируется химической реакцией. Далее закон роста может перейти в логарифмическую зависимость, где сказывается действие тормозящего электрического поля. При температурах порядка 400- 500оС электроны и дырки в оксиде кремния становятся достаточно подвижными и не формируют электрического поля, оказывающего заметное влияние на перенос ионов окислителя. Поэтому участок логарифмической зависимости толщины пленки от времени перестает наблюдаться.
Рост толстой пленки лимитируется процессами диффузии, толщина пленки возрастает как t1/2. Все эти процессы сильно зависят от температуры.
|
Рис. 4.3. Рост Si02 |