
- •1. Гармонический осциллятор, его закон движения, скорость, ускорение, возвращающая сила, энергия.
- •2. Маятники пружинный, математический, физический.
- •3. Сложение одинаково направленных гармонических колебаний с одинаковыми частотами. Метод векторной диаграммы. Биения.
- •4. Сложение взаимно-перпендикулярных колебаний. Фигуры Лиссажу.
- •5. Свободные затухающие колебания. Логарифмический декремент. Апериодический процесс.
- •6. Вынужденные колебания. Резонанс
- •7. Волна, уравнение гармонической волны.
- •8. Перенос волной энергии, вектор Умова.
- •9. Электромагнитное поле. Уравнения Максвелла. Плоская электромагнитная волна.
- •Уравнения Максвелла для электромагнитного поля
- •Интерференция волн
- •Интерференция света
- •11. Интерференция света в тонких пленках, примеры ее наблюдения и применения.
- •Кольца Ньютона
- •Полосы равного наклона (интерференция от плоскопараллельной пластинки)
- •Применение интерференции света
- •12. Дифракция, условие её наблюдения. Принцип Гюйгенса-Френеля. Метод зон Френеля и его применение для расчета дифракции света на узкой щели.
- •13. Дифракционная решетка, ее применение в качестве спектрального прибора.
- •14. Физические принципы голографии.
- •15. Поляризация света. Поляризатор и анализатор. Закон Малюса. Примеры получения и применения поляризованного света.
- •16. Тепловое излучение, его характеристики: энергетическая светимость, испускательная и поглощательная способности. Цвет несамосветящегося тела. Абсолютно черное и серое тела. Закон Кирхгофа
- •17. Законы излучения абсолютно черного тела: Закон Стефана-Больцмана, закон Вина. Трудности классической физики при объяснении распределения энергии в спектре черного тела. Квантовая гипотеза Планка.
- •1. Закон Стефана-Больцмана:
- •2. Закон Вина:
- •18. Фотоэффект, красная граница, работа выхода электрона из металла, задерживающее напряжение. Квантовый механизм фотоэффекта, уравнение Эйнштейна.
- •19. Эффект Комптона, его квантовый механизм.
- •20. Корпускулярно-волновой дуализм излучения. Фотоны. Взаимосвязь волновых и корпускулярных характеристик фотонов. Связь между корпускулярной и волновой картинами.
- •21. Волна де Бройля. Дифракция электронов. Статистический смысл волн де Бройля. Электронный микроскоп как пример практического использования электронных волн.
- •22. Соотношения неопределенностей как выражение корпускулярно-волнового дуализма и границ применения классической физики.
- •23. Состояние и уравнение движения квантовой частицы. Волновая функция, ее статистический смысл. Уравнение Шредингера.
- •24. Примеры применения уравнения Шредингера: частица в бесконечно глубокой потенциальной яме; гармонический осциллятор.
- •25. Развитие представлений о строении атома. Модель атома Резерфорда, ее недостатки.
- •26. Спектры испускания и поглощения атомов как источник информации об их строении и свойствах. Спектр атома водорода. Формула Бальмера.
- •27. Модель атома Бора, ее недостатки. Постулаты Бора. Энергетические уровни атома водорода и его спектр по модели Резерфорда – Бора.
- •28. Волновая модель атома водорода. Квантовые числа, их проявления в опыте. Периодическая таблица элементов Менделеева как отражение квантовых состояний электронов.
- •29. Спонтанное и вынужденное излучение. Лазер.
- •30. Ядро атома: состав, размеры, плотность. Энергия связи ядра атома, удельная энергия связи.
- •31. Радиоактивность. Закон радиоактивного распада. Период полураспада. Виды радиоактивного распада. Экологические аспекты радиоактивности.
- •32. Ядерная реакция. Законы сохранения. Энергетический эффект. Реакция деления тяжелых ядер, термоядерная реакция, их применение в энергетике, экологические аспекты.
28. Волновая модель атома водорода. Квантовые числа, их проявления в опыте. Периодическая таблица элементов Менделеева как отражение квантовых состояний электронов.
Атом Н
![]()


Δ – оператор Лапласа
![]()
U – сферически-симметричная функция
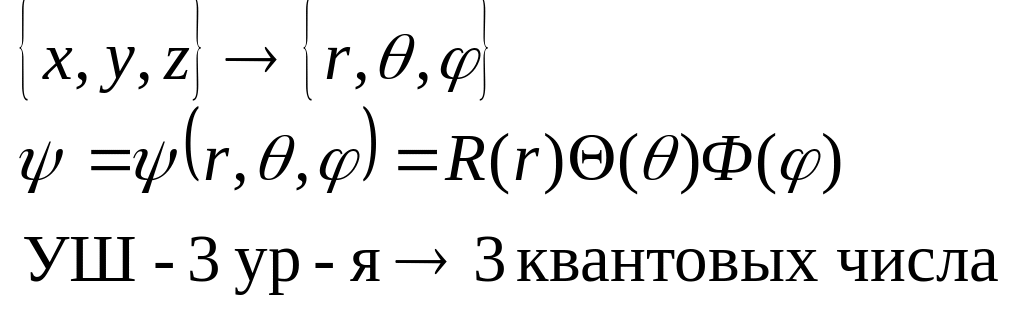
![]()
n – главное квантовое число, n = 1,2,3,…,∞ - уровни энергии (квантование энергии)
![]() (как в модели Бора)
(как в модели Бора)
l – азимутальное (орбитальное) квантовое число; l = 0,1,…, (n-1)
n=1 → l=0
n=2 → l=1,2 и т.д.
Квантование момента импульса:
![]() - на одном и том же
уровне энергии могут быть электроны с
различными моментами импульса.
- на одном и том же
уровне энергии могут быть электроны с
различными моментами импульса.
m – магнитное квантовое число, связано орбитальным.
m = -l,-(l-1),…, -1, 0, 1,…, l – всего (2l+1) значение.
Орбитальный момент электрона связан его магнитным моментом (электрон образует круговой ток).
Во внешнем магнитном поле магнитная стрелка стремится повернуть вдоль поля.
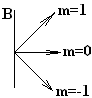 m
– проекция
Lz,
z
– ось, заданная внешним полем, например
m
– проекция
Lz,
z
– ось, заданная внешним полем, например
![]() .
.
Lz = hm.
Из УШ следует квантование энергии момента импульса и проекции момента импульса, что подтверждается в опыте, т.е. в спектре излучения атома. Квантование энергии – спектр линейчатый; квантование момента импульса и его проекции проявляются в том, что под действием внешнего магнитного поля спектральные линии расщепляются на m-близких линий.
Опыт показал, что даже в отсутствии поля спектральные линии являются дублетами (двойными), что свидетельствует еще об одном квантовом числе S. S = ±1/2 (2 значения). S – спиновое квантовое число.
Электрон обладает собственным механическим и магнитным моментами. Собственный механический момент называется спин.
Классическая аналогия:
![]()
Состояние электрона в атоме: (n, l, m, S).
Периодическая система Менделеева отображает периодичность свойств разных элементов. Объяснение тому дает квантовая механика. Электроны подчиняются принципу Паули.
1. Паули: n, l, m, S – только один электрон.
2. Принцип минимума Е
В многоэлектронных атомах заполнение электронных оболочек идет снизу вверх.
n=1, l=0, m=0, S=±1/2 2 состояния (H, He);
![]()
Квантовая механика – основа химии.
29. Спонтанное и вынужденное излучение. Лазер.
Рассмотрим совокупность невзаимодействующих атомов в основном состоянии:
![]()
![]()
Метастабильный уровень ~ 10-3 с.
![]()
Излучение когерентное – падающий и испущенный фотоны согласованы по частоте и фазе.
Между поглощением и испусканием существует равновесие.
В обычных материалах:
![]()
N ~ e-E/kT
N2 < N1
Инверсная (обратная) среда N2 > N1 (есть метастабильный уровень).
![]()
Усиление (генерация) излучения.
Неравновесные (инверсные) среды усиливают излучение, т.е. генерируют его за счет вынужденного излучения. При этом вынужденное излучение когерентное, т.е. все фотоны движутся «ухо в ухо». Вынужденное излучение используется в лазерах.
Лазер – источник когерентного излучения в видимом диапазоне, полученный искусственным путем. В его принципе действия реализуется вынужденное (индуцированное) излучение, обладающее монохроматичностью и когерентностью, в отличие от естественного (спонтанного) излучения.
Принципиальна схема (блок-схема):
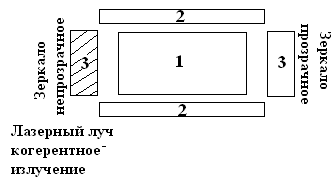
1 – активная среда, допускающая инверсную (обратную) заселенность уровней (добавка примесей: рубин, He-Ne);
![]()
2 - Система накачки (возбуждения), источник энергии;
3 – Резонатор.
Свойства и применение лазерного излучения:
1. Монохроматичность λ ± Δλ, Δλ – мала по сравнению с естественной шириной;
2. Когерентность:
![]()
3. Высокая плотность мощности в пучке (в технике, в медицине, в науке).
