
- •71. Реакция монобромирования бутана в условиях радикального механизма
- •72. Сравнение свойств альдегидов и кетонов в условиях реакции нуклеофильного присоединения
- •73. Двухосновные карбоновые кислоты
- •74. Реакции полимеризации пропена
- •75. Методы получения аминов восстановлением нитросоединений и из галогеноуглеводородов
- •76. Реакции нуклеофильного присоединения у кетонов
- •77. Реакция полимеризации 1,3 – бутадиена
- •78. Получение диазосоединений
- •79. Реакция полимеризации этилена. Укажите элементарное звено, степень полимеризации
- •80. Расположение в ряд по возрастанию кислотных свойств спиртов (этанол, пропанол, 2- хлорэтанол)
73. Двухосновные карбоновые кислоты
Двухосновные карбоновые кислоты — это карбоновые кислоты, содержащие две карбоксильные группы —COOH, с общей формулой HOOC—R—COOH, где R — любой двухвалентный органический радикал.
Химические свойства
Дикарбоновые кислоты проявляют те же химические свойства, что и монокарбоновые — эти свойства обусловлены наличием карбоксильной группы:
- диссоциация в водных растворах
- образование солей: в отличие от монокарбоновых кислот, дикарбоновые способны образовывать кислые соли;
- образование галогенангидридов.
В то же время есть существенные различия, обусловленные наличием второй карбоксильной группой :
склонность к образованию хелатов;
образование некоторыми кислотами циклических ангидридов;
способность образовывать полимеры в реакции с другими полифункциональными соединениями.
Примеры
Щавелевая кислота Этандиовая кислота HOOC—COOH
Малоновая кислота Пропандиовая кислота НООС—СН2—СООН
Янтарная кислота Бутандиовая кислота НООС—(СН2)2—СООН
Фталевая
кислота Бензол-1,2-дикарбонавя кислота 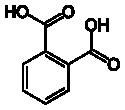
74. Реакции полимеризации пропена
Пропен (пропилен) СН2=СН-СН3 — непредельный (ненасыщенный) углеводород ряда этена, горючий газ, относится к углеводородам ряда этена (алкены или олефины).
- Полимеризация
Условия реакции: нагревание, присутствие Катализаторов. Соединение молекул происходит путем расщепления внутримолекулярных π-cвязей и образования новых межмолекулярных σ-cвязей

В присутствии Катализаторов Циглера - Натты (в массе, в растворе или псевдоожиженном слое) пропен полимеризуется до полипропилена; в присутствии металлоорганических комплексных Катализаторов образуются этен-пропиленовые сополимеры, обладающие свойствами натуральных каучуков; при полимеризации на кислотных Катализаторах (А1С13, HF, Н3РО4) - три- и тетрамеры пропена, на щелочных Катализаторах-4-метил-1-пентен, полимеры которого обладают уникальными теплофизическими свойствами, в присутствии А1k3А1-2-метил-1-пентен, деметилированием которого получают изопрен:
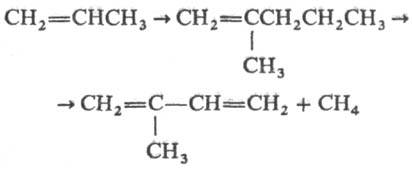
75. Методы получения аминов восстановлением нитросоединений и из галогеноуглеводородов
При действии восстановителей нитрогруппа превращается в первичную аминогруппу:
R-NO2 а R-NH2
Эта реакция проходит с соединениями как жирного, так и ароматического ряда. Особенно большое практическое значение этот метод имеет в ароматическом ряду, так как сами ароматические нитропроизводные получаются очень легко и являются поэтому вполне доступными продуктами.
В качестве восстановителей в большинстве случаев пользуются металлами: оловом, цинком или железом в присутствии соляной кислоты.
Наиболее быстро и полно восстановление происходит при действии олова:
2R-NO2 + 3Sn + 14HCl а 2[R-NH3]Cl + 3SnCl4 + 4H2O
В технике для восстановления нитросоединений пользуются железом, которое значительно дешевле олова:
R-NO2 + 3Fe + 7HCl а [R-NH3]Cl + 3FeCl2 + 2H2O
Опытным путем было установлено, что для проведения этой реакции можно взять в 40 раз меньше кислоты, чем это требуется приведенным уравнением, что объясняется окислением двухвалентного железа в трехвалентное.
В качестве восстановителей могут быть также использованы сернистый аммоний или сернистый натрий:
R - NO2 + 3(NH4)2S а R - NH2 + 6NH3 + 3S + 2H2O
Применяя сернистый аммоний, возможно провести частичное восстановление полинитросоединений, например получить нитроанилин из динитробензола.
Восстановление нитросоединений может быть произведено и в газовой фазе водородом в присутствии металлической меди как катализатора.
