
- •71. Реакция монобромирования бутана в условиях радикального механизма
- •72. Сравнение свойств альдегидов и кетонов в условиях реакции нуклеофильного присоединения
- •73. Двухосновные карбоновые кислоты
- •74. Реакции полимеризации пропена
- •75. Методы получения аминов восстановлением нитросоединений и из галогеноуглеводородов
- •76. Реакции нуклеофильного присоединения у кетонов
- •77. Реакция полимеризации 1,3 – бутадиена
- •78. Получение диазосоединений
- •79. Реакция полимеризации этилена. Укажите элементарное звено, степень полимеризации
- •80. Расположение в ряд по возрастанию кислотных свойств спиртов (этанол, пропанол, 2- хлорэтанол)
71. Реакция монобромирования бутана в условиях радикального механизма
Реакции радикального присоединения— реакции присоединения, в которых атаку осуществляют свободные радикалы — частицы, содержащие один или несколько неспаренных электронов. При этом радикалы могут атаковать как другие радикалы, так и нейтральные частицы.
Реакции радикального присоединения обозначают AdR.
Реакции свободнорадикального присоединения характерны для алкенов, которые часто вступают в них вместо реакций электрофильного присоединения в присутствии источника свободных радикалов
Механизм реакции радикального присоединения включает в себя следующие стадии:
1. Первая стадия — инициирование цепи. Она может начаться спонтанно, фотохимически, электрохимически, посредством нагревания или путем химического иницирования[2].
2. Вторая стадия — развитие цепи. На этой стадии радикалы реагируют с молекулами, образуя продукты реакции и новые радикалы.
3. Третья стадия — обрыв цепи или рекомбинация свободных радикалов.
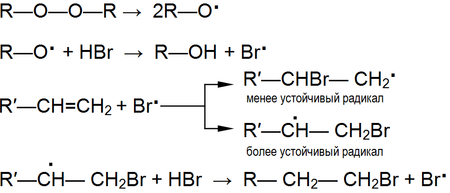
Реакции радикального замещения ускоряются в условиях генерирования свободных радикалов и замедляются в присутствии веществ, улавливающих свободные радикалы.
Радикальное присоединение идет против правила Марковникова (эффект Хараша). Вызвано это повышенной стабильностью третичных, аллильных и некоторых других радикалов, образующихся при присоединении атакующего радикала в определённую позицию в молекуле.
72. Сравнение свойств альдегидов и кетонов в условиях реакции нуклеофильного присоединения
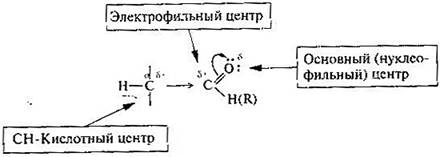
Наличие в молекуле альдегида или кетона электрофильного центра — атома углерода карбонильной группы — предопределяет возможность нуклеофильной атаки. Местом электрофильной атаки служит основный (нуклеофильный) центр — атом кислорода карбонильной группы. Кроме того, в альдегидах и кетонах имеется слабый СН-кислотный центр, атом водорода которого обладает с определенной протонной подвижностью и может, в частности, подвергаться атаке основанием. Легкость нуклеофильной атаки по атому углерода карбонильной группы альдегида или кетона зависит от величины эффективного положительного заряда на атоме углерода, его пространственной доступности и кислотно-основных свойств среды. С учетом электронных эффектов групп, связанных с карбонильным атомом углерода, величина дельта+ на нем в альдегидах и кетонах убывает в следующем ряду.
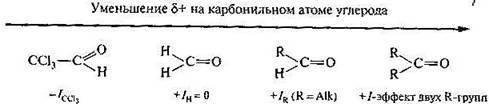
Пространственная доступность карбонильного атома углерода уменьшается при замене водорода на более объемистые органические радикалы. Поэтому альдегиды более реакционноспособны, чем кетоны.Альдегиды содержат в молекуле карбонильную группу, связанную с атомом водорода, т. е. альдегидную группу —СН=O. Кетоны содержат карбонильную группу, связанную с двумя углеводородными радикалами, т. е. кетонную группу.В зависимости от строения углеводородных радикалов альдегиды и кетоны бывают алифатическими, алициклическими и ароматическими.Изомерия альдегидов связана только со строением радикалов.Изомерия кетонов связана со строением радикалов и с положением карбонильной группы в углеродной цепи.
