- •Процессы обратимые и необратимые. Равновесные и неравновесные
- •Энтальпия. Физические свойства
- •Теплоёмкость рабочего тела
- •Изохорный процесс газа
- •Изобарный процесс газа.
- •Изотермический процесс газа.
- •Адиабатный процесс газа.
- •Цикл Карно и его свойства.
- •Цикл газотурбинной установки с регенерацией
Адиабатный процесс газа.
Процесс протекающий без подвода и отвода теплоты, т.е. при отсутствии теплообмена с окружающей средой, называют адиабатным, а кривая этого процесса –адиабатой. Условия процесса: dq=0 , q=0.
Т.к.
dq=0
,
то согласно первому закону термодинамики:
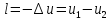
и
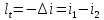
Таким образом совершаемая рабочим телом механическая работа в адиабатном термодинамическом процессе равна уменьшению внутренней энергии тела, техническая работа при этом пропорциональна изменению (уменьшению) энтальпии. В обратимом диабатном процессе энтропия термодинамического тела не меняется: S=Const.
Уравнение
адиабаты в системе координат pv
–диаграммы
при постоянной теплоёмкости (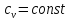 )
для идеального газа:
)
для идеального газа:
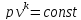 где
где
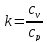 -
показатель адиабаты
-
показатель адиабаты
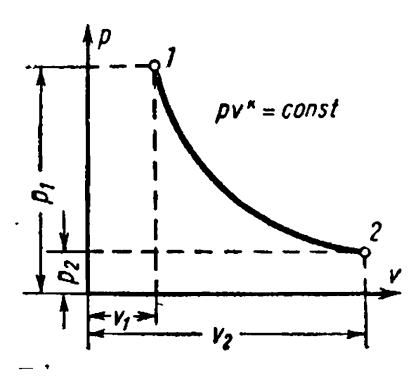
Зависимости
между начальными и конечными
параметрами процесса: между р
и v
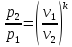 ,
,
между
T
и v
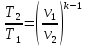
между
р
и T 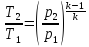
Работу 1 кг газа находят по следующим формулам
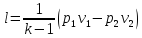
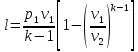
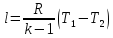
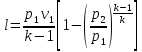
Изменение
внутренней энергии газа и работа
адиабатного процесса равны по величине
и противоположны по знаку.
. 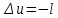
Изменение
внутренней энергии идеального газа
в адиабатном процессе может быть
также выражено уравнением
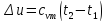
Второй закон термодинамики
Второй закон термодинамики устанавливает направление протекания самопроизвольных тепловых процессов в природе и определяет условия превращения теплоты в работу. Закон утверждает, что теплота в природе самопроизвольно переходит только от тел более нагретых к менее нагретым.
В соответствии со вторым законом термодинамики для превращения теплоты в работу в любом тепловом двигателе необходимо иметь два тела с различными температурами. Более нагретое тело будет источником теплоты для получения работы, менее нагретое – теплоприемником. При этом к. п. д. теплового двигателя всегда будет меньше единицы.
Второй закон динамики математически может быть выражен:
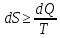
Где dS –бесконечно малое приращении энтропии системы;
dQ – бесконечно малое количество теплоты, полученной системой от источника теплоты;
T - абсолютная температура источника теплоты.
Знак неравенства соответствует необратимым процессам, а равенства - обратимым. Следовательно, аналитическое выражение второго закона термодинамики для бесконечно малого обратимого процесса примет вид
dQ=TdS
а т.к. согласно первому закону термодинамики
dQ=dU+pdV
то
TdS=dU+pdV.
Цикл Карно и его свойства.
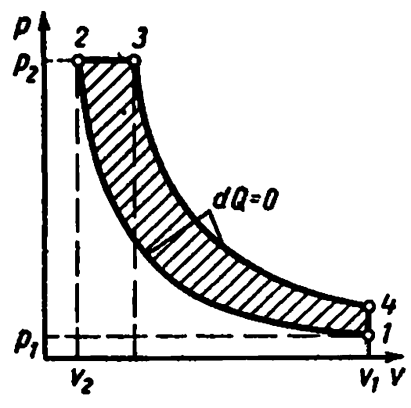
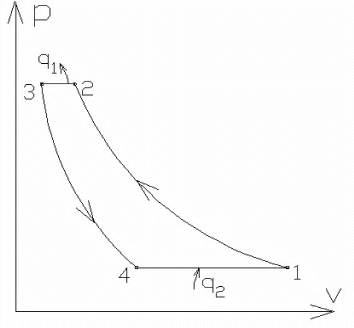
Цикл Карно. Состоит из двух изотерм и двух адиабат. Этот цикл представляет собой замкнутый процесс , совершаемый рабочим телом в идеальной тепловой машине при наличии двух источников теплоты: нагревателя и холодильника.
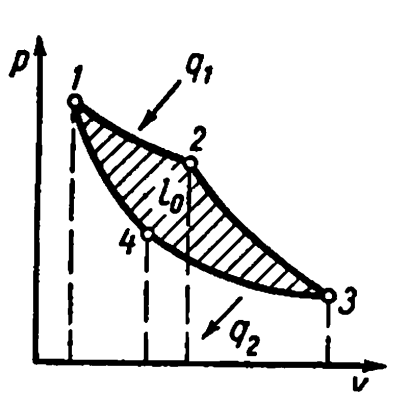
Цикл Карно в pv-диаграмме
Процессы 1—2 и 3—4 являются изотермическими, а 2—3 и 4—1 — адиабатными. Начальная температура рабочего тела в цикле принимается равной температуре нагревателя T1. При изотермическом расширении от состояния 1 до состояния 2 рабочее тело получает от нагревателя количество теплоты q1 при температуре T1. На участке 2—3 рабочее тело адиабатно расширяется. При этом температура рабочего тела понижается отT1 до T2, а давление падает от p2 до p3. При сжатии по изотерме 3—4 от рабочего тела отводится к холодильнику количество теплоты q2 при температуре T2. Дальнейшее сжатие по адиабате 4—1 приводит к повышению температуры рабочего тела от T2 до T1, а рабочее тело возвращается в первоначальное состояние.
Суммарная работа цикла lц графически изображается площадью 12341.
Термический
к. п. д. цикла: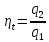
Количество подведённой теплоты:
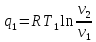
Количество отведённой теплоты:
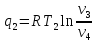
Работа цикла Карно
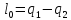
Термический к.п.д. цикла:
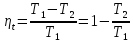
Цикл с подводом теплоты при постоянном объёме состоит из двух адиабат и двух изохор
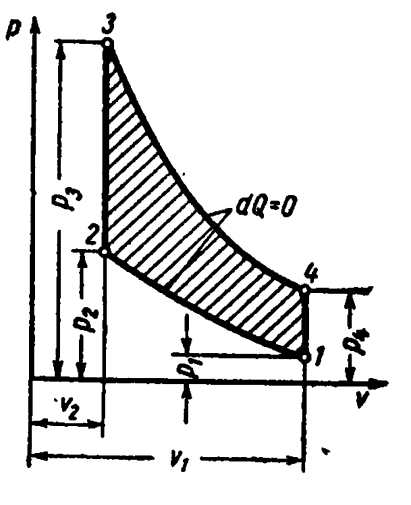
Характеристики цикла:
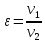 -степень
сжатия
-степень
сжатия
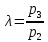 степень
повышения давления
степень
повышения давления
Количество подведённой теплоты :
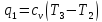
Количество отведённой теплоты:
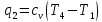
Работа
цикла
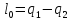
Термический к.п.д. цикла:
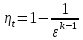
Цикл с подводом теплоты при постоянном давлении состоит из двух адиабат, одной изобары и одной изохоры.
Характеристики цикла:
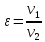 -степень
сжатия
-степень
сжатия
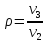 степень
предварительного расширения.
степень
предварительного расширения.
Количество подведённой теплоты :
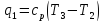
Количество отведённой теплоты:
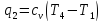
Работа
цикла
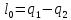
Термический к.п.д. цикла:
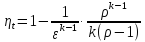
Цикл с комбинированным подводом теплоты состоит из двух адиабат, двух изохор и одной изобары
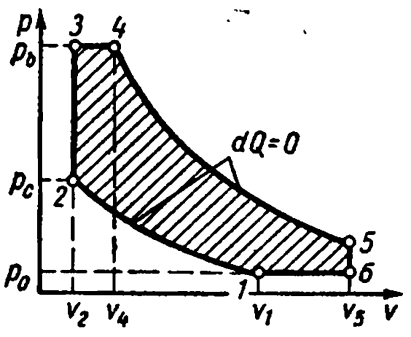
Характеристики цикла
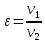 ;
;
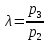 ;
;
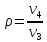
Количество подведённой теплоты
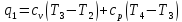
Количество отведённой теплоты
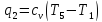
Термический к.п.д. цикла
Таблицы водяного пара.
Перегретый пар или насыщенный пар по своим свойствам значительно отличаются от идеальных газов. Уравнения для состояния паров весьма сложны и в расчётной практике не применяются. Для практических целей используют таблицы и диаграммы, составленные на основании опытных и теоретических данных. Таблицы составлены с высокой степенью точности для перегретых и насыщенных паров до температуры 10000С и давления 98,0 Мпа.
В таблицах для насыщенного пара приведены температуры насыщения, давления, значения удельных объёмов, энтальпия и энтропия жидкости и сухого пара, теплота парообразования. В таблицах перегретого пара приведены для различных давлений и температур величины основных параметров: удельный объём, энтальпия и энтропия.
i – S диаграмма водяного пара.
Большим
достоинством is
диаграммы
является то, что техническая работа и
количество теплоты, участвующие в
процессах, изображаются отрезками
линий, а не площадями. При построении
is-
диаграммы по
оси ординат откладывается удельная
энтальпия пара, а по оси абсцисс –
удельная энтропия. За начало координат
принято состояние воды в тройной
точке, где
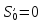 ,
,
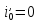 .
.
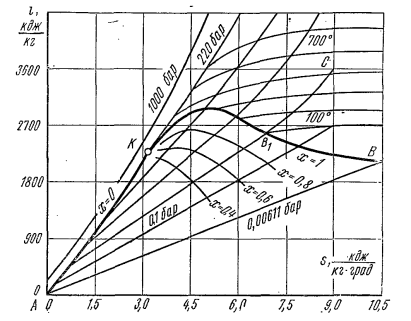
Пользуясь данными таблиц водяного пара , на диаграмму наносят пограничные кривые жидкости и пара, сходящиеся в критической точке К. Пограничная кривая жидкости выходит из начала координат, т.к. в этой точке энтропию и энтальпию принимают равной нулю. Состояние воды отмечают точками на соответствующих изобарах. Линии изобар в области влажного пара являются прямыми наклонными линиями расходящимися веером от пограничной кривой жидкости. В изобарном процессе:
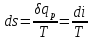 или
или
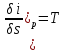
Угловой коэффициент наклона изобары к оси абсцисс в каждой точке диаграммы числено равен абсолютной температуре данного состояния. Т.к. в области влажного пара изобара совпадает с изотермой, то согласно последнему уравнению изобары влажного пара являются прямыми линиями:
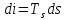 ,
а это и есть уравнение прямой линии.
В области перегретого пара изобары
имеют кривизну с выпуклостью,
обращённой вниз. В области влажного
пара наносится сетка линий постоянной
сухости пара (x=const)
которые сходятся в критической точке
К.
,
а это и есть уравнение прямой линии.
В области перегретого пара изобары
имеют кривизну с выпуклостью,
обращённой вниз. В области влажного
пара наносится сетка линий постоянной
сухости пара (x=const)
которые сходятся в критической точке
К.
Изотермы в области влажного пара совпадают с изобарами. В области перегретого пара они расходятся: изобары поднимаются вверх, а изотермы представляют собой кривые линии, обращённые выпуклостью вверх. На диаграмму наносят сетку изохор, которые имеют вид кривых, поднимающихся более круто вверх по сравнению с изобарами. Обратимый адиабатный процесс изображается вертикальной прямой. Область лежащая ниже изобары тройной точки изображает состояния смеси пар + лёд.
Адиабатический процесс водяного пара. Изображение процесса в p – V , i – S и T –S диаграммах.
Адиабатный процесс совершается без подвода и отвода теплоты, и энтропия рабочего тела при обратимом процессе остаётся постоянной величиной: s=const. Поэтому на is и Ts-диаграммах адиабаты изображаются вертикальными прямыми: рис. а и б
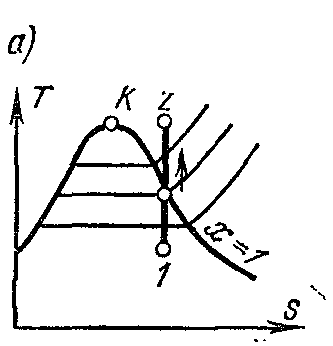
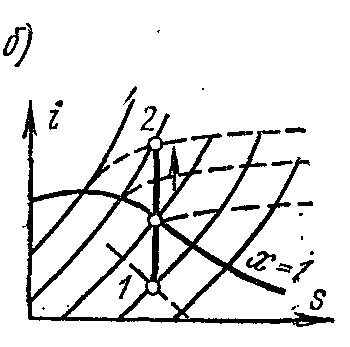
При адиабатном расширении давление и температура пара уменьшаются; перегретый пар переходит в сухой, а затем во влажный пар. Из условий постоянства энтропии возможны определение конечных параметров пара, если известны параметры начального и один параметр конечного состояний.
На pv- диаграмме обратимый адиабатный процесс изображается некоторой кривой (рис. в)
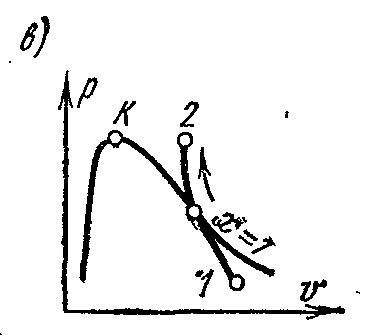
Удельная работа в адиабатном процессе определяется из уравнения:
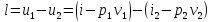 .
.
Изменение удельной внутренней энергии:
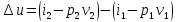
Многоступенчатое сжатие в компрессоре.
Для получения газа высокого давления применяют многоступенчатые компрессоры
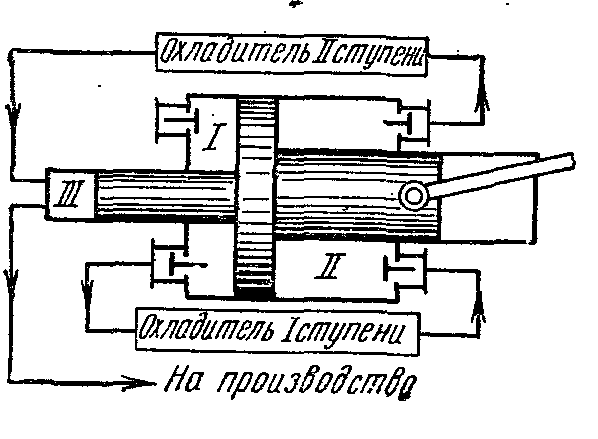
в которых сжатие газа осуществляется политропно в нескольких последовательно соединённых цилиндрах с промежуточным его охлаждением после каждого сжатия.
Применение сжатия газа в нескольких цилиндрах понижает отношение давлений в каждом из них и повышает объёмный к.п.д. компрессора. Кроме того, промежуточное охлаждение газа после каждой ступени улучшает условия смазки поршня в цилиндре и уменьшает расход энергии на привод компрессора.
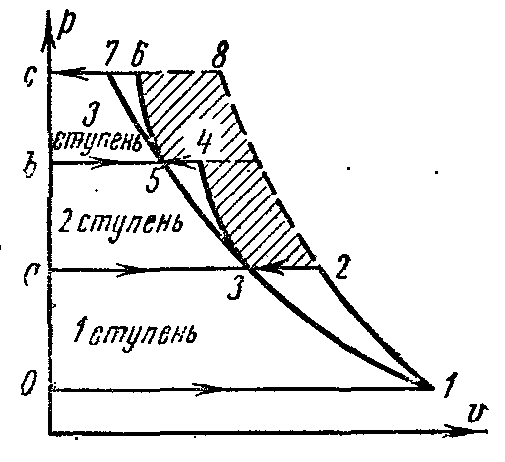
идеальная индикаторная диаграмма трёхступенчатого компрессора, где 0-1 – линия всасывания в первую ступень;
1-2 – политропный процесс сжатия в первой ступени; 2-а – линия нагнетания из первой ступени в первый охладитель; а-3 – линия всасывания во вторую ступень; 3-4 – политропный процесс сжатия во второй ступени; 4-в – линия нагнетания из второй ступени во второй охладитель; в-5 – линия всасывания в третью ступень; 5-6 - политропный процесс сжатия в третьей ступени; 6-с – линия нагнетания из третьей ступени в резервуар или на производство. Отрезки 2-3, 4-5 изображают уменьшение объёма газа в процессе при постоянном давлении от охлаждения в первом и втором охладителях. Охлаждение рабочего тела во всех охладителях производится до одной и той же температуры, равной начальной Т1, поэтому температуры газа в точках 1, 3 и 5 одинаковые и лежат на изотерме 1 – 7.
Отношение давлений во всех ступенях обычно берётся одинаковым:
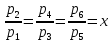
При одинаковых отношениях давлений во всех ступенях, равенстве начальных температур и равенстве показателей политропы равны между собой и конечные температуры газа в отдельных ступенях компрессора:
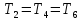
Степень
увеличения давления в каждой ступени
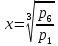 или при
z
ступеней
или при
z
ступеней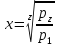
Степень
увеличения давления в каждой ступени
равна корню z-й
степени из отношений конечного давления
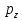
к
начальному
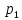
При равенстве температур газа у входа в каждую ступень и равенстве отношений давлений во всех цилиндрах получаем равенство затраченных работ во всех ступенях компрессора:
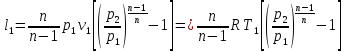
Во второй ступени
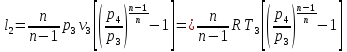
Работа в третьей ступени
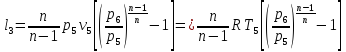
Откуда l1=l2=l3
Полная удельная работа в джоулях, расходуемая на сжатие газа в трёх ступенях компрессора: lк=3l1
При одинаковых условиях сжатия газа количества теплоты , отводимые от газа в отдельных ступенях, равны между собой:
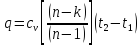
Теплоту отводимую от газа в любом охладителе при изобарном процессе охлаждения, находим по формуле:
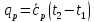
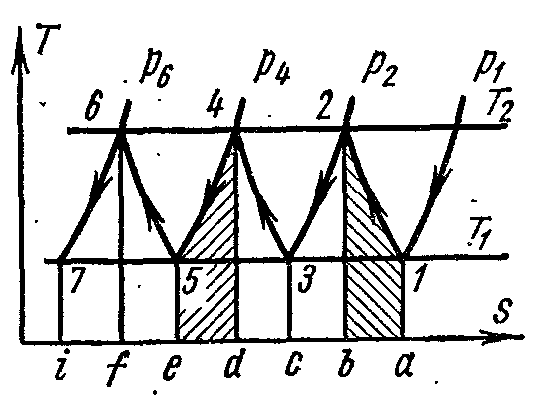
В Ts-диаграммах процессы адиабатного сжатия изображены прямыми 1-2, 3-4, 5-6, а процессы охлаждения кривыми 2-3, 4-5, 6-7.
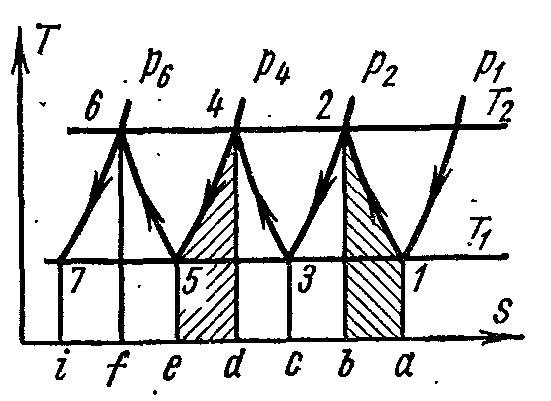
Процессы политропного сжатия изображены кривыми 1-2, 3-4, 5-6, а процессы охлаждения в охладителях - линиями 2-3, 4-5, 6-7.
Цикл ДВС со сгоранием при V=const
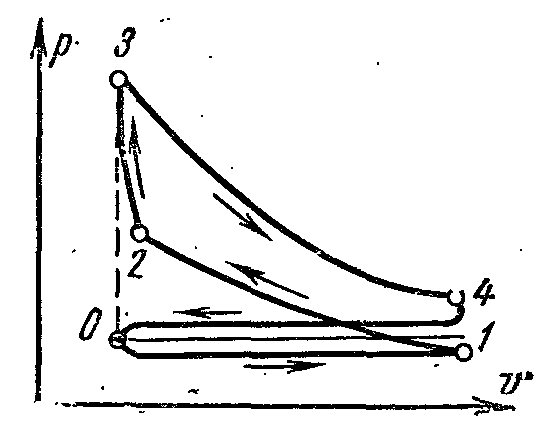
На рисунке изображена индикаторная диаграмма двигателя, работающего с быстрым сгоранием топлива при постоянном объёме. В качестве горючего используется бензин, светильный или генераторный газ, спирты и др.
При ходе поршня из левого мёртвого положения в крайнее правое через всасывающий клапан засасывается горючая смесь. Этот процесс изображён кривой 0-1, называется линией всасывания, она не является термодинамическим процессом , т.к. в нём основные параметры не изменяются, а изменяются только масса и объём смеси в цилиндре. При обратном движении поршня всасывающий клапан закрывается, происходит сжатие горючей смеси. Изображается кривой 1-2, называется линией сжатия. В точке 2 происходит воспламенение горючей смеси от электрической искры. Сгорание горючей смеси происходит почти мгновенно, т.е. практически при постоянном объёме. Этот процесс изображён кривой 2-3. В результате сгорания топлива температура газа резко возрастает и давление увеличивается (точка 3). Затем продукты горения расширяются. Поршень перемещается в правое мёртвое положение, и газы совершают полезную работу. На индикаторной диаграмме процесс расширения изображается кривой 3-4, называемой линией расширения. В точке 4 открывается выхлопной клапан, и давление в цилиндре падает почти до наружного давления. При дальнейшем движении поршня справа на лево из цилиндра удаляются продукты сгорания через выхлопной клапан при давлении, несколько превышающим атмосферное давление. Изображается кривой 4-0 и называется линией выхлопа. Такой рабочий процесс совершается за четыре хода поршня или за два оборота вала. Такие двигатели называются четырёхтактными.
Цикл с подводом теплоты при постоянном объёме состоит из двух адиабат и двух изохор
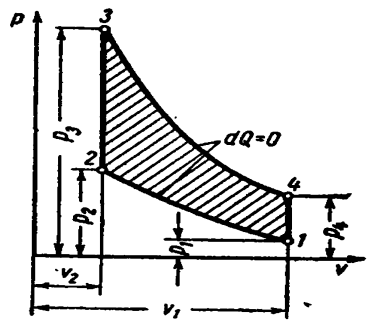
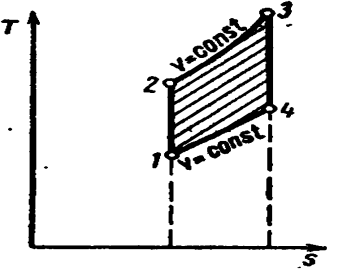
Характеристиками цикла являются:
 – степень
сжатия
– степень
сжатия
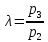 – степень
повышения давления
– степень
повышения давления
Количество подведённой теплоты :
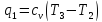
Количество отведённой теплоты:
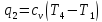
Работа
цикла
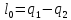
Термический к.п.д. цикла:
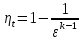
Цикл ДВС со сгоранием при p=const
Изучение циклов с подводом количества теплоты при постоянном объёме показало, что для повышения экономичности двигателя , работающего по этому циклу, необходимо применять высокие степени сжатия. Воздух при большом сжатии имеет настолько высокую температуру что подаваемое в цилиндр топливо самовоспламеняется без запальных приспособлений. Раздельное сжатие воздуха и топлива позволяет использовать любое жидкое тяжёлое и дешёвое топливо – нефть, мазут, смолы, каменноугольные масла.
Таким достоинством обладают двигатели, работающие с постепенным сгоранием топлива при постоянном давлении. В них воздух сжимается в цилиндре двигателя, а жидкое топливо распыляется сжатым воздухом от компрессора.
Идеальный цикл двигателя с постепенным сгоранием топлива при постоянном давлении, т.е. цикл с подводом количества теплоты при постоянном давлении осуществляется следующим образом.
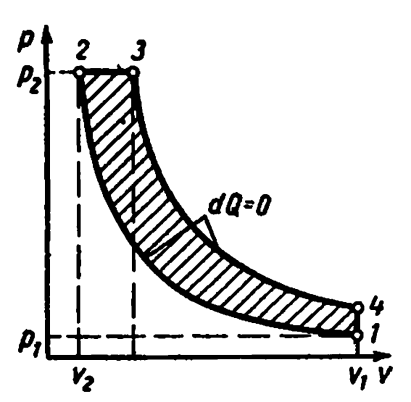
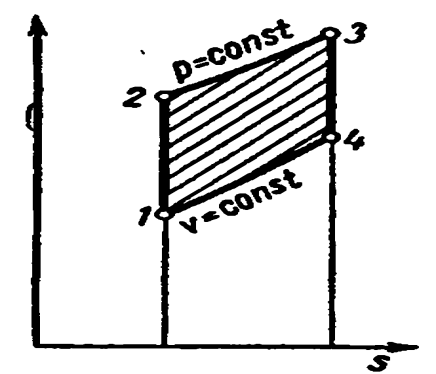
Газообразное рабочее тело с начальными параметрами p1 , v1 , T1 сжимается по адиабате 1-2; затем телу по изобаре 2-3 сообщается некоторое количество теплоты q1. От точки 3 рабочее тело расширяется по адиабате 3-4. По изохоре 4-1 рабочее тело возвращается в первоначальное состояние, при этом в теплоприёмник отводится теплота q2.
Характеристики цикла:
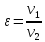 -степень
сжатия
-степень
сжатия
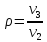 степень
предварительного расширения.
степень
предварительного расширения.
Количество подведённой теплоты :
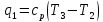
Количество отведённой теплоты:
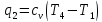
Работа
цикла
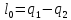
Термический к.п.д. цикла:
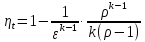
Цикл ДВС с подводом тепла при V и p =const
В бескомпрессорном двигателе высокого сжатия со смешанным подводом количества теплоты жидкое топливо топливным насосом подаётся через топливную форсунку в головку цилиндра в виде мельчайших капелек. Попадая в нагретый воздух, топливо самовоспламеняется и горит в течении всего периода, пока открыта форсунка: вначале при постоянном объёме, а затем при постоянном давлении.
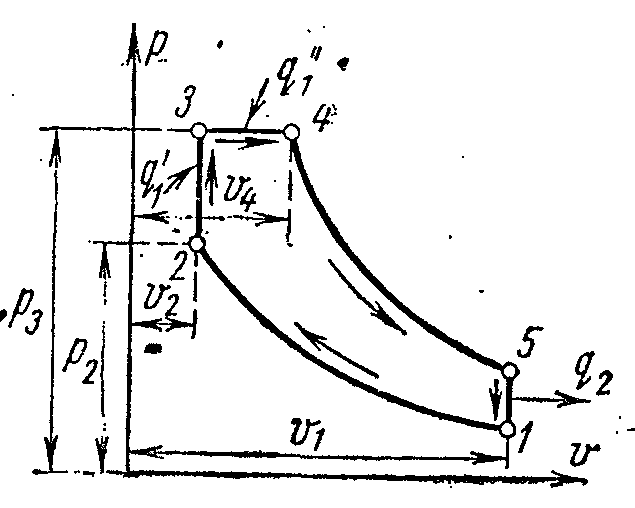
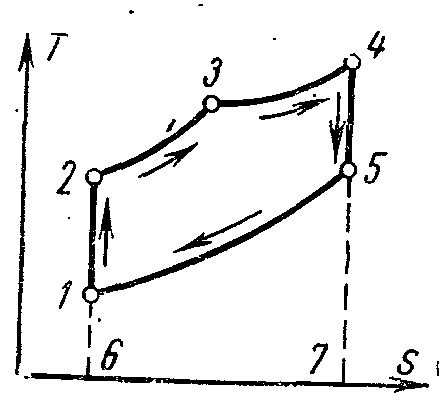
Идеальный цикл двигателя со смешанным подводом количества теплоты изображён в pv – и Ts – диаграммах.
рабочее
тело с начальными параметрами p1
, v1
, T1
сжимается по адиабате 1-2 до точки 2. По
изохоре 2-3 к рабочему телу подводится
первая доля теплоты
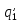 .
По изобаре 3-4 подводится вторая доля
теплоты
.
По изобаре 3-4 подводится вторая доля
теплоты
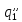 .
От
точки 4 рабочее тело расширяется по
адиабате 4-5. По изохоре 5-1 рабочее тело
возвращается в первоначальное состояние
– в точку 1, при этом отводится теплота
.
От
точки 4 рабочее тело расширяется по
адиабате 4-5. По изохоре 5-1 рабочее тело
возвращается в первоначальное состояние
– в точку 1, при этом отводится теплота
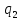 в
теплоприёмник.
в
теплоприёмник.
Характеристики цикла являются:
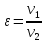 -степень
сжатия
-степень
сжатия
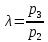 – степень
повышения давления
– степень
повышения давления
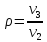 -
степень
предварительного расширения .
-
степень
предварительного расширения .
Определим термический КПД цикла при условии что теплоёмкости cp , cv и показатель адиабаты k= cp / cv постоянны:
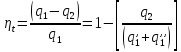
Первая доля подведённой теплоты:
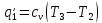
Вторая доля подведённого количества теплоты:
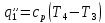
Количество отведённой теплоты:
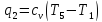
Термический КПД цикла
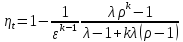
Цикл газотурбинной установки
Рабочим телом в газотурбинных установках являются продукты сгорания жидкого или газообразного топлива.
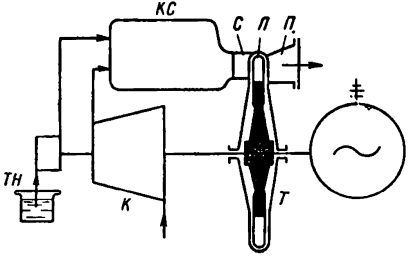
На рисунке представлена схема наиболее распространённого типа газотурбинной установки со сгоранием топлива при постоянном давлении.
Компрессор К, расположенный на одном валу с газовой турбиной Т, всасывает воздух из атмосферы и сжимает его до заданного давления. Сжатый в компрессоре воздух поступает в камеру сгорания КС; туда же топливным насосом ТН подаётся жидкое горючее. Сгорание происходит при постоянном давлении. Из камеры сгорания газы поступают в сопла С, из которых они с большой скоростью поступают на рабочие лопатки Л турбины и приводят во вращение её ротор. Отработавшие газы через выпускной патрубок П выпускаются в атмосферу.
Цикл ГТУ с подводом количества теплоты в процессе p=const.
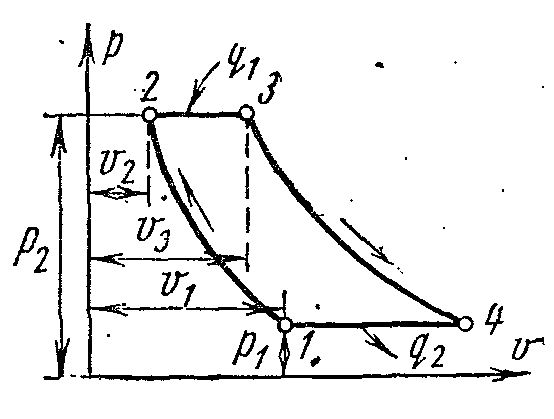
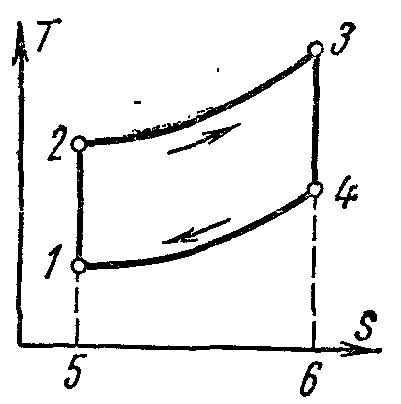
Идеальный цикл газотурбинной установки на pv – и Ts – диаграммах с подводом теплоты при p=const. Цикл состоит из двух адиабат и двух изобар.
Отвод теплоты от рабочего тела производится не по изохоре, как в ДВС, а по изобаре. Рабочее тело с начальными параметрами p1 , v1 , T1 сжимается по адиабате 1-2 до точки 2. От точки2 к рабочему телу подводится некоторое удельное количество теплоты q1 по изобаре 2-3. Затем рабочее тело расширяется по адиабате 3-4 до начального давления и возвращается по изобаре 4-1 в первоначальное состояние, при этом отводится удельное количество теплоты q2.
Характеристиками
цикла является степень повышения
давления в компрессоре
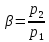 и степень изобарного расширения
и степень изобарного расширения
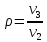 .
.
Количество подводимой теплоты:
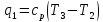
Количество отводимой теплоты:
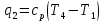
Термический КПД цикла
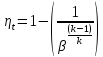
Цикл паросиловой установки. Цикл Ренкина.
За основной цикл в паротурбинной установке принят идеальный цикл Ренкина. В этом цикле осуществляется полная конденсация рабочего тела в конденсаторе, вследствие чего вместо громоздкого малоэффективного компрессора для подачи воды в котёл применяют питательный водяной насос, который имеет малые габариты и высокий КПД.

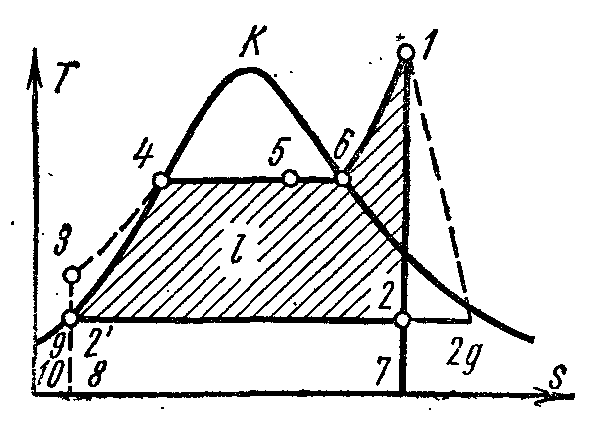
На
pv-
диаграмме
точка 4 характеризует состояние
кипящей воды в котле при давлении p1.
Линия
4-5 изображает процесс парообразования
в котле; затем пар подсушивается в
перегревателе при давлении p1.
Полученный пар по адиабате 1-2 расширяется
в цилиндре парового двигателя до
давления p2
в конденсаторе. В процессе 2 –
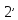 пар полностью конденсируется до
состояния кипящей жидкости при
давлении p2
,
отдавая теплоту парообразования
охлаждающей воде. Процесс сжатия воды
пар полностью конденсируется до
состояния кипящей жидкости при
давлении p2
,
отдавая теплоту парообразования
охлаждающей воде. Процесс сжатия воды
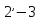 осуществляется в насосе; получающееся
при этом повышение температуры воды
ничтожно мало, и им в исследованиях
при давлениях до 3,0 – 4,0 МПа пренебрегают.
Линия 3-4 изображает изменение объёма
воды при нагревании от температуры
в конденсаторе до температуры кипения.
Работа насоса изображается заштрихованной
пл. 03
осуществляется в насосе; получающееся
при этом повышение температуры воды
ничтожно мало, и им в исследованиях
при давлениях до 3,0 – 4,0 МПа пренебрегают.
Линия 3-4 изображает изменение объёма
воды при нагревании от температуры
в конденсаторе до температуры кипения.
Работа насоса изображается заштрихованной
пл. 03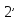 7. Энтальпия пара при выходе из
перегревателя в точке 1 равна i1
и
на Ts
–диаграмме
изображается пл. 9
7. Энтальпия пара при выходе из
перегревателя в точке 1 равна i1
и
на Ts
–диаграмме
изображается пл. 9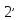 34617109. Энтальпия пара при входе в
конденсатор в точке 2 равна i2
и на Ts
–диаграмме
изображается пл. 9
34617109. Энтальпия пара при входе в
конденсатор в точке 2 равна i2
и на Ts
–диаграмме
изображается пл. 9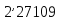 . Энтальпия воды при выходе из
конденсатора в точке
. Энтальпия воды при выходе из
конденсатора в точке
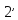 равна i1
и
на Ts
–диаграмме
изображается пл. 9
равна i1
и
на Ts
–диаграмме
изображается пл. 9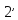 8109. Полезная работа пара в цикле Ренкина
l
изображается на pv-
диаграмме
пл.
8109. Полезная работа пара в цикле Ренкина
l
изображается на pv-
диаграмме
пл.
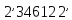 .
.
Если
в цикле Ренкина учитывать работу насоса,
то процесс адиабатного сжатия воды в
нём представится на Ts-
диаграмме
адиабатой
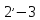 ,
а изобара 3-4 соответствует нагреванию
воды в котле при давлении p1
до соответствующей температуры кипения.
,
а изобара 3-4 соответствует нагреванию
воды в котле при давлении p1
до соответствующей температуры кипения.
Термический КПД цикла Ренкина определяется по формуле:
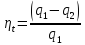
Удельное
количество теплоты
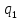 в цикле подводится при p=const
в процессах 3-4 (подогрев воды до
температуры кипения), 4-6 (парообразование)
и 6-1(перегрев пара) и равно разности
энтальпий начальной и конечной точек
процесса:
в цикле подводится при p=const
в процессах 3-4 (подогрев воды до
температуры кипения), 4-6 (парообразование)
и 6-1(перегрев пара) и равно разности
энтальпий начальной и конечной точек
процесса:
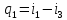
Это
удельное количество теплоты изображается
на Ts
–диаграмме
пл. 8
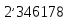 .
Отвод удельного количества теплоты
q2
осуществляется
в конденсаторе по изобаре 2-
.
Отвод удельного количества теплоты
q2
осуществляется
в конденсаторе по изобаре 2-
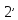 ,
следовательно
,
следовательно
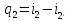
Отводимая
теплота
изображается
на Ts
–диаграмме
пл.
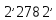
Термический КПД цикла Ренкина :
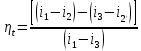
Цикл воздушной компрессорной холодильной установки

На рисунке изображена схема воздушной холодильной установки, где в качестве рабочего тела применяют воздух, являющийся наиболее удобным, безвредным и доступным рабочим телом. Воздушная холодильная установка работает следующим образом.
Воздух, охлаждающий помещение 1, сжимается в компрессоре 2, в результате чего температура его увеличивается. Сжатый воздух при постоянном давлении нагнетается в теплообменник 3, в котором охлаждается водой до температуры окружающей среды. После этого сжатый воздух поступает в расширительный цилиндр, или детандер 4, где расширяется до начального давления. При расширении температура воздуха падает до -60 или -700С и холодильный воздух направляется для охлаждения помещения, где, нагреваясь, опять поступает в компрессор.
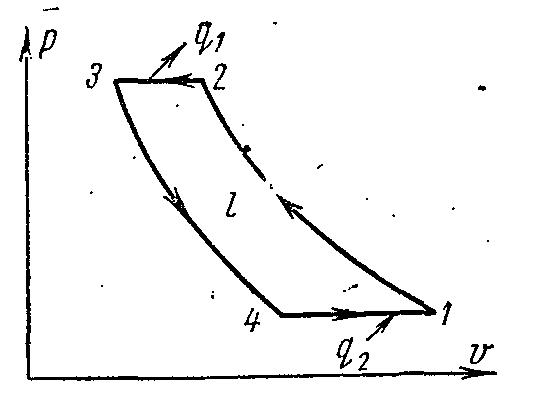
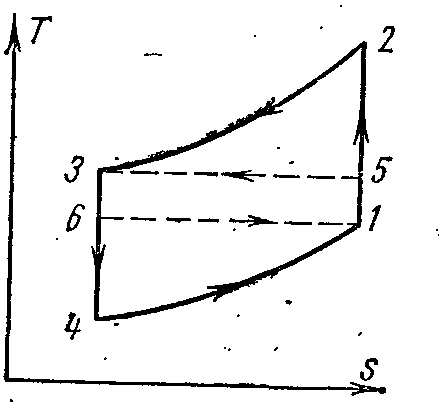
в pv – и Ts – диаграммах:
воздух в процессе 1-2 адиабатно сжимается от давления p1 до p2. В изобарном процессе 2-3 от воздуха отводится удельное количество теплоты внешнему источнику и температура его понижается от T2 до Т3. При адиабатном расширении в процессе 3-4 воздух дополнительно охлаждается от температуры Т3 до Т4. Далее в изобарном процессе 4-1 происходит отвод теплоты от охлаждаемого помещения (теплоотдатчика), в результате чего воздух нагревается от Т4 до Т1.
Работа затрачиваемая на осуществление цикла, равна разности удельных количеств теплоты q1 и q2. Считая теплоёмкость постоянной имеем:
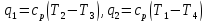
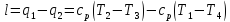
Тогда холодильный коэффициент цикла:
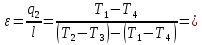
=
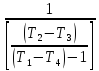
Из адиабатных процессов 1-2 и 3-4
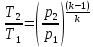 и
и
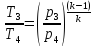
Но
p2=p3,
а p1=p4
тогда
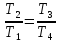
Окончательно имеем
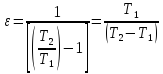
Где Т1 – температура охлаждаемого помещения или температура воздуха, засасываемого в компрессор.
Т2 – температура сжатого воздуха.
Цикл паровой компрессорной холодильной установки
Наибольшее распространение для охлаждения тел до температуры -200С получили холодильные установки, в которых холодильным агентом являются легкокипящие жидкости - аммиак, фреоны, сернистый ангидрид и другие при невысоких давлениях (желательно близких к атмосферному).
На рисунке схема компрессорной установки, работающей на парах аммиака NH3.
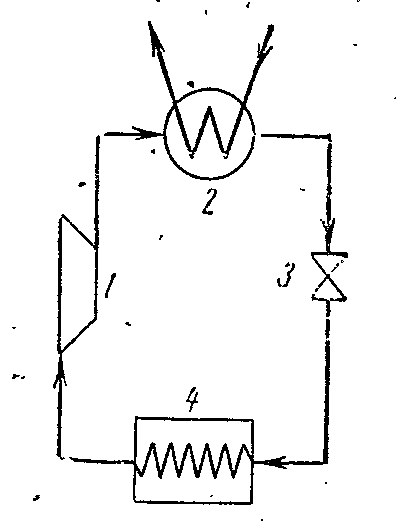
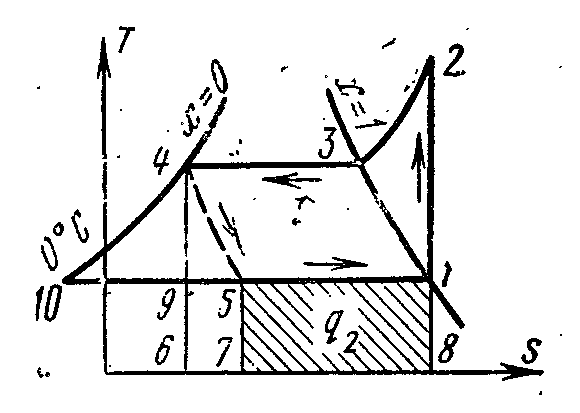
1- компрессор; 2- конденсатор; 3- дроссельный вентиль; 4 – охлаждаемое помещение (испаритель)
В компрессоре сжимается аммиачный сухой насыщенный пар или влажный пар с большой степенью сухости по адиабате 1-2 до состояния перегретого пара в точке 2. Из компрессора пар нагнетается в конденсатор, где полностью превращается в жидкость (процесс 2-3-4). Из конденсатора жидкий аммиак проходит через дроссельный вентиль, в котором дросселируется, что сопровождается понижением температуры и давления. Затем жидкий аммиак с низкой температурой поступает в охладитель, где, получая количество теплоты (в процессе 5-1) испаряется и охлаждает рассол, который циркулирует в охлаждаемых камерах. Процесс дросселирования как необратимый процесс изображается на диаграмме условной кривой 4-5.
В паровой компрессорной установке не применяется расширительный цилиндр (детандер), а рабочее тело дросселируется в регулировочном вентиле. Замена расширительного цилиндра дросселем сопровождается возрастанием энтропии, что вызывает некоторую потерю холодопроизводительности, но эта замена значительно упрощает установку и даёт возможность легко регулировать давление пара и получать необратимую температуру в охладителе .
Удельная
работа затраченная на совершение
цикла:
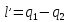 =
=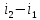
Холодильный
коэффициент компрессорной аммиачной
установки:
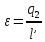
Где
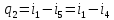 - удельное
количество теплоты, воспринимаемое
аммиачным паром в охладителе.
- удельное
количество теплоты, воспринимаемое
аммиачным паром в охладителе.
Холодильный коэффициент установки
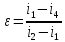
Значения энтальпий в уравнении определяют по is-диаграмме или по таблице аммиака.
Паровые холодильные установки имеют большое преимущество перед воздушными. Они компактны, дёшевы и имеют более высокий холодильный коэффициент.
Процесс парообразования в p – V диаграмме
Фазовая pv – диаграмма системы, состоящей из жидкости и пара, представляет собой график зависимости удельных объёмов воды и пара от давления.
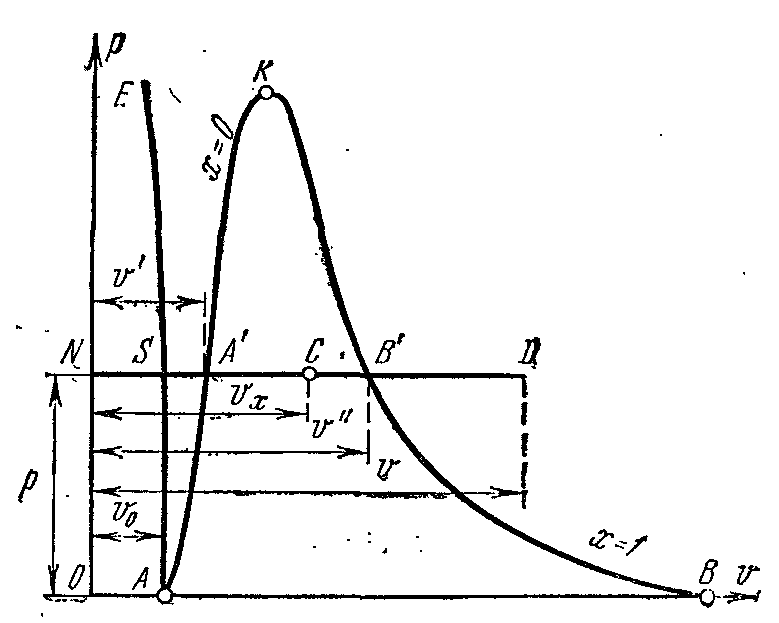
Пусть вода при температуре 00С и некотором давлении ρ занимает удельный объём v0 (отрезок NS) . Вся кривая АЕ выражает зависимость удельного объёма воды от давления при температуре 00С . Т.к. вода вещество почти несжимаемое то кривая АЕ почти параллельна оси ординат. Если при постоянном давлении сообщать воде теплоту, то её температура будет повышаться и удельный объём увеличиваться. При некоторой температуре ts вода закипает, а её удельный объём v’ в точке А’ достигнет при данном давлении максимального значения. С увеличением давления растёт температура кипящей жидкости ts и объём v’ также увеличивается. График зависимости v’ от давления представлен кривой АК которая называется пограничной кривой жидкости. Характеристикой кривой является степень сухости x=0. В случае дальнейшего подвода теплоты при постоянном давлении начнётся процесс парообразования. При этом количество воды уменьшается, количество пара увеличивается. В момент окончания парообразования в точке В’ пар будет сухим насыщенным. Удельный объём сухого насыщенного пара обозначается v’’.
Если процесс парообразования протекает при постоянном давлении то температура его не изменяется и процесс A’B’ является одновременно изобарным и изотермическим. В точках A’ и B’ вещество находится в однофазном состоянии. В промежуточных точках вещество состоит из смеси воды и пара. Такую смесь тел называют двухфазной системой.
График зависимости удельного объёма v’’ от давления представлен кривой КВ, которая называется пограничной кривой пара.
Если к сухому насыщенному пару подводить теплоту при постоянном давлении, то температура и объём его будут увеличиваться и пар из сухого насыщенного перейдёт в перегретый (точка D). Обе кривые АК и КВ делят диаграмму на три части. Влево от пограничной кривой жидкости АК до нулевой изотермы располагается область жидкости. Между кривыми АК и КВ располагается двухфазная система, состоящая из смеси воды и сухого пара. Вправо от КВ и вверх от точки К располагается область перегретого пара или газообразного состояния тела. Обе кривые АК и КВ сходятся в одной точке К, называемой критической точкой.
Критическая точка является конечной точкой фазового перехода жидкость – пар, начинающегося в тройной точке. Выше критической точки существование вещества в двухфазном состоянии невозможно. Никаким давлением нельзя перевести газ в жидкое состояние притемпературах выше критической.
Параметры критической точки для воды:
tк=374,120С ; vк=0,003147 м3/кг;
ρк=22,115 МПа; iк=2095,2 кДж/кг
sк=4,424 кДж/(кг·К).
Процесс p =const водяного пара. Изображение процесса в p – V , i – S и T –S диаграммах.
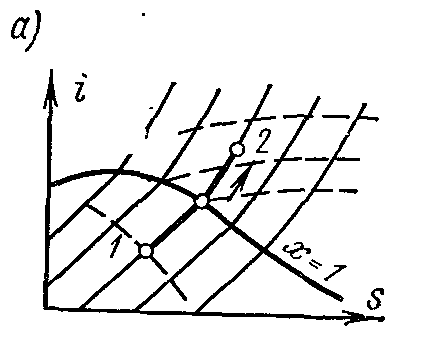
На is – диаграмме изобара в области насыщенного пара представляется прямой линией, пересекающей пограничные кривые жидкости пара. При подводе теплоты к влажному пару степень сухости его увеличивается и он (при постоянной температуре) переходит в сухой, а при дальнейшем подводе теплоты – в перегретый пар. Изобара в области перегретого пара представляет собой кривую, направленную выпуклостью вниз.
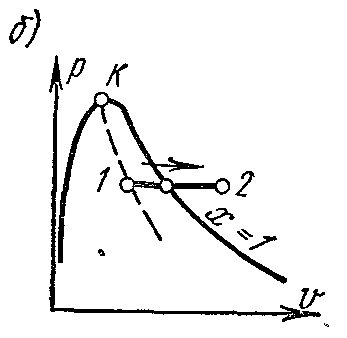
На pv – диаграмме изобарный процесс изображается отрезком горизонтальной прямой, который в области влажного пара изображает и изотермический процесс одновременно.
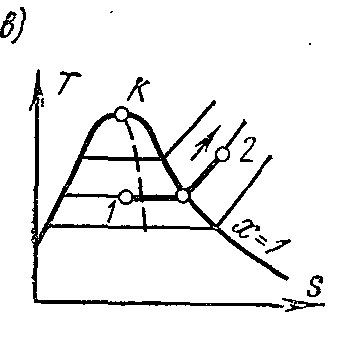
На Ts – диаграмме в области влажного пара изобара изображается прямой горизонтальной линией, а в области перегретого пара – кривой, обращённой выпуклостью вниз. Значения всех необходимых величин для расчёта берутся из таблиц насыщенных и перегретых паров.
Изменение удельной внутренней энергии пара:
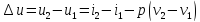
Внешняя работа:
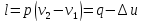
Подведённое
удельное количество теплоты:
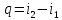
В том случае, когда q задано и требуется найти параметры второй точки, лежащей в области двухфазных состояний, применяется формула для энтальпии влажного пара:
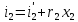
Процесс T=const водяного пара. Изображение процесса в p – V , i – S и T –S диаграммах.
Изотермический процесс.
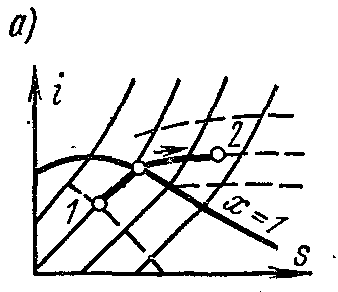
На is – диаграмме в области влажного пара изотерма совпадает с изобарой и является прямой наклонной линией. В области перегретого пара изотерма изображается кривой с выпуклостью вверх.
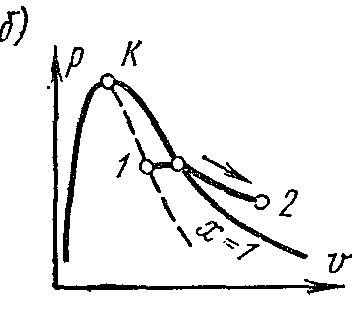
На pv – диаграмме в области влажного пара изотермический процесс изображается горизонтальной прямой. Для насыщенного пара этот процесс совпадает с изобарным. В области перегрева давление пара понижается, а процесс изображается кривой с выпуклостью к оси абцисс.
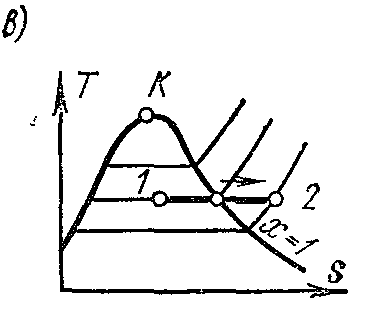
На Ts – диаграмме изотермный процесс изображается отрезком горизонтали.
Удельная внутренняя энергия водяного пара в отличие от внутренней энергии идеального газа изменяется в следствии изменения потенциальной составляющей, поэтому при T=const
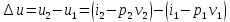
Подведённое удельное количество теплоты в процессе:
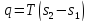
Внешняя работа определяется из первого закона термодинамики:
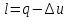
Формула Майера.
Особое
значение в термодинамике имеют
теплоемкости газа при постоянном
давлении, т.е. в изобарном процессе –
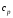 и при постоянном объеме, т.е. в
изохорном процессе –
и при постоянном объеме, т.е. в
изохорном процессе –
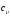 .
Эти теплоемкости связываются формулой
Майера
.
Эти теплоемкости связываются формулой
Майера
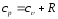
Отношение теплоемкостей
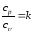
где k – показатель адиабаты.
Понятие «Холодильный коэффициент»
Холодильный коэффициент безразмерная величина (обычно больше единицы), характеризующая энергетическую эффективность работы холодильной машины; равна отношению холодопроизводительности к количеству энергии (работе), затраченной в единицу времени на осуществление холодильного цикла. Определяется типом холодильного цикла, по котором у работает машина, совершенством её основных элементов и для одной и той же машины зависит от температурных условий её работы.
Холодильный коэффициент идеальной холодильной машины, работающей по обратному циклу Карно:
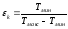
где Tмин и Tмакс – соответственно низшая и высшая температуры в цикле.
Холодильный
коэффициент воздушной холодильной
машины (рисунок)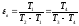 ,
,
где T1 и T2 – соответственно температуры начала и конца адиабатного сжатия;
T3 и T4 – температуры начала и конца адиабатного расширения в детандере.
Уравнение состояния рабочего тела.
Уравнение состояния тела устанавливается зависимость между параметрами состояния. Для идеального газа уравнение состояния выражается законом Клапейрона:
а) для 1 кг газа
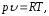
где R – газовая постоянная;
б) для m кг газа
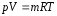 .
.
Для моля идеального газа уравнение состояния предложено Менделеевым:
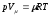 ,
,
где
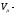 объем моля газа;
объем моля газа;
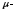 молекулярная
масса.
молекулярная
масса.
При
нормальных физических условиях
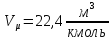 .
.
Универсальная газовая постоянная
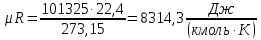
Газовая постоянная
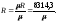
Объем газа V, находящегося при произвольных физических условиях (р и Т), может быть приведен к нормальным физическим условиям (pн и Tн)
по формуле