
- •Введение
- •Понятие о хтп.
- •Тема 1. Иерархическая организация процессов в химическом производстве.
- •Тема 7. Промышленный катализ
- •Типовые технологические операторы хтс.
- •Виды технологических связей между операторами.
- •Тема 12. Сырьевая и энергетическая подсистема хтс.
- •Тема 12. Сырьевая и энергетическая подсистема хтс.
Понятие о хтп.
ХТП представляет собой совокупность операций, позволяющих получить целевой продукт из исходного сырья. Все эти операции входят в состав трех основных стадий, характерных практически для каждого химико-технологического процесса: 1) подготовка исходных реагентов к проведению химической реакции (исходное сырье подвергают очистке от посторонних примесей, пользуясь разными методами); 2) химическое взаимодействие; 3) разделение смеси продуктов, отходов, побочных продуктов, непрореагировавших веществ.
На всех этапах, а особенно на заключительных, проводят также рекуперацию вторичных материальных и энергетических ресурсов. Потоки газообразных и жидких веществ, попадающих в окружающую среду, подвергают очистке и обезвреживанию от опасных примесей. Твердые отходы либо направляют на дальнейшую переработку, либо размещают для хранения в безопасных для окружающей среды условиях.
Таким образом, ХТП в целом – это сложная система, состоящая из единичных связанных между собой процессов (элементов) и взаимодействующая с окружающей средой.
Элементами ХТП являются перечисленные выше процессы тепло- и массообмена, гидромеханические, химические и т. д. Их рассматривают как единичные процессы химической технологии.
Важной подсистемой сложного ХТП является химический процесс.
Химический процесс представляет собой одну или несколько химических реакций, сопровождаемых явлениями переноса теплоты, массы и импульса, оказывающих влияние как друг на друга, так и на протекание химической реакции.
Единичные процессы протекают в различных аппаратах – химических реакторах, абсорбционных и ректификационных колоннах, теплообменниках и т. д. Отдельные аппараты соединены в технологическую схему процесса.
Классификация ХТП. сам/ст
Схожа с классификацией реакторов. Признаки классификации:
по характеру процесса, протекающего в аппарате, реакторе (обратимый, необратимый, равновесный, неравновесный);
по фазовому составу реагентов (гомоген, гет/ген и какие фазы Г, Ж, Т);
по тепловому эффекту (экзо-, эндотермические);
по температуре (низко-, средне-, высокотемпературные);
по давлению (атмосферное, вакуум, повышенное, высокое);
по степени перемешивания (ИВ, ИС);
по температурному режиму (адиабатический, изотермический, политермический). Если ИС – изотермический, если ИВ – адиабатический.
по способу организации процесса (непрерывный и периодический, полунепрерывный).
Кроме того, можно классифицировать по способу организации теплообмена (с внешним, внутренним, комбинированным т/обм.);
Уровни анализа, описания и расчета ХТП.
Анализ и описание ХТП проводят последовательно с учетом уровня протекания процесса. В ОХТ рассматриваются 6 уровней протекания процесса.
-
Молекулярный уровень (микрокинетика).
Здесь рассматривается химическая реакция с позиции формальной кинетики с помощью известных кинетических зависимостей. (гомоген)
-
Уровень малого объема.
Например, зерно катализатора, пузырек газа, капля жидкости и др. (гет/ген проц). Здесь пользуются законами макрокинетики.
-
Уровень потока.
Совокупность частиц (капель, зерен).
-
Уровень реактора.
Здесь учитываются конструктивные особенности реакционных зон, их число, взаимное расположение.
-
Уровень ХТС.
Учитываются взаимные связи между реакторами, аппаратами, машинами.
-
Уровень предприятия, отрасли или министерства.
Рекомендуемая литература.
-
Бесков В. С. Общая химическая технология: Учебник для вузов. – М.: ИКЦ "Академкнига", 2005. – 452 с.
-
Кутепов А. М., Бондарева Т. И., Беренгартен М. Г. Общая химическая технология: Учеб. для вузов. - М.: ИКЦ "Академкнига", 2005. - 528 с.
-
Общая химическая технология/ Под ред. А. Г. Амелина, 1977
-
Общая химическая технология. в 2-х т / Под ред. И. П. Мухленова. – М.: Высш. шк., 1984. – 256 с.
-
Расчеты химико–технологических процессов / Под ред. И. П. Мухленова, 1982
-
Лаптев М. Я. Общая химическая технология: Примеры материальных и тепловых расчетов, 1969, 1975.
-
Игнатенков В.И., Бесков В.С. Примеры и задачи по общей химической технологии: Учеб. пособие для вузов. – М.: ИКЦ “Академкнига”, 2005 г. – 198 с.
-
Галанов М.Э. Практические занятия по дисциплине “Общая химическая технология”. (для студентов заочной формы обучения). – Череповец: ЧГУ, 2005 г. – 64 с. № 7200.
-
Котенко В.А., Докунина Е.В., Розанова О.А. Лабораторный практикум по дисциплине “Общая химическая технология”. Учеб.-метод. пособие. – Череповец: ЧГУ, 2001 г. – 33 с. № . 5341.
-
Лабораторный практикум по ОХТ/ Под ред. И. П. Мухленова, 1979.
Уравнение адиабаты. Графики, характеризующие адиабатический режим протекания ХТП
Рассмотрим реакцию
![]()
Разность температур в адиабатическом реакторе:
![]() , (10.3)
, (10.3)
уравнение выведено из уравнения теплового баланса (см. выше).
![]() , (10.4)
, (10.4)
![]() , (10.5)
, (10.5)
где
х – степень превращения, СА0
– исход концентрация целевого компонента
А, СD
– концентрация D;
qР
– тепловой эффект реакции;
![]() - сред теплоемокость;
- сред теплоемокость;
![]() - поправочный коэффициент, выражающий
отношение масс целевого продукта (напр,
D)
к массе основного исходного вещества
(напр, А).
- поправочный коэффициент, выражающий
отношение масс целевого продукта (напр,
D)
к массе основного исходного вещества
(напр, А).
![]() - теплота, которая выделилась или
поглатилась бы при полном превращении
основного вещества в продукт (при х=1);
G
– масса продукционной смеси;
- коэффициент адиабатического изменения
температуры.
- теплота, которая выделилась или
поглатилась бы при полном превращении
основного вещества в продукт (при х=1);
G
– масса продукционной смеси;
- коэффициент адиабатического изменения
температуры.
Графическое выражение уравнения адиабаты представлено на рис. 10.1.
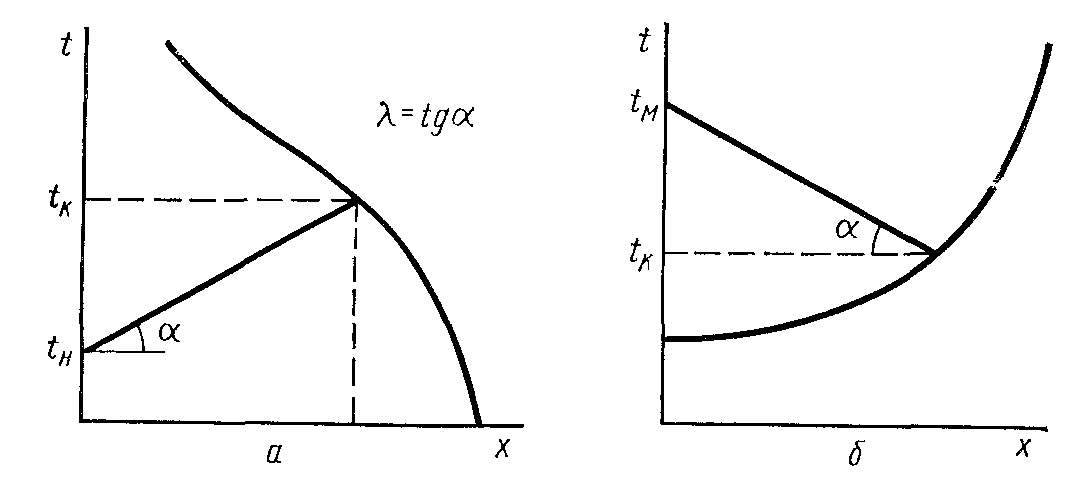
Рис. 10.1. Уравнение адиабаты: а – экзотермическая реакция, б – эндотермическая.
Самостоятельное изучение.
