
- •1. Отличительные особенности поведения полимеров
- •2. Строение полимеров
- •3. Классификация полимеров
- •1. Природные, искусственные и синтетические полимеры
- •2. Органические и неорганические полимеры
- •3. Термопласты и реактопласты
- •4. Пластики, эластомеры, волокна и смолы
- •4. Химия полимеризации
- •4.1. Цепная полимеризация
- •4.1.1. Свободнорадиакальная полимеризация
- •4.1.2. Ионная полимеризация
- •4.1.3. Координационная полимеризация
- •4.2. Ступенчатая полимеризация
- •4.2.1. Поликонденсация
- •4.2.2. Полиприсоединение
- •4.2.3. Полимеризация с раскрытием цикла
- •4.3. Особые типы полимеризационных реакций
- •4.3.1. Электрохимическая полимеризация
- •4.3.2. Полимеризация по механизму метатезиса
- •5. Способы проведения процессов полимеризации
- •6. Средняя молекулярная масса полимеров
- •6.1. Полидисперсность и кривые
- •7. Выделение и очистка полимеров
- •8. Фракционирование полимеров
- •9. Определение молекулярных масс полимеров
- •9.1. Криоскопия
- •9.2. Эбуллиоскопия
- •9.3. Мембранная осмометрия
- •9.4. Парофазная осмометрия
- •9.5. Вискозиметрия
- •9.6. Ультрацентрифугирование
- •9.7. Светорассеяние
- •10. Структура полимерных молекул
- •10.1. Микроструктуры, связанные с химическим строением полимеров
- •10.1.1. Гомоцепные и гетероцепные полимеры.
- •10.1.2. Гомополимеры и сополимеры.
- •10.2. Микроструктуры, связанные с геометрическим
- •10.3. Стереорегулярные полимеры
- •10.4. Геометрическая изомерия
- •11. Стеклообразное состояние полимеров
- •11.1 Агрегатные состояния веществ
- •11.2. Фазовые состояния веществ
- •11.3. Факторы, влияющие на температуру стеклования
- •11.4 Температура стеклования и молекулярная масса полимеров
- •11.5. Влияние пластификаторов на температуру стеклования
- •11.6. Значение температуры стеклования
- •12. Кристаллические полимеры
- •12.1. Полимерные монокристаллы
- •12.2. Влияние степени кристалличности на свойства полимеров
- •13. Химические превращения полимеров
- •14. Деструкция полимеров
- •14.1. Термическая деструкция
- •14.2. Механическая деструкция
- •14.3. Фотодеструкция
- •14.4. Радиационная деструкция
- •14.5. Окислительная деструкция
- •15. Переработка полимеров
4.1.2. Ионная полимеризация
Ионная полимеризация также протекает по цепному механизму и также включает атаку на -электронную пару мономера. Однако в этом случае на нее воздействует не свободный радикал с неспаренным электроном, а положительный или отрицательный ион.
Катионная полимеризация
Представим реакционную систему, в которую вводится протон:

Протон как электрофильная частица вытягивает на себя -электроны двойной связи и образует простую -связь с атомом углерода в голове молекулы, а положительный заряд перемещается к хвосту. Происходит инициирование цепи с образованием катиона карбония. Этот карбкатион атакует электроны -связи второй молекулы мономера, оттягивает их на себя и образует -связь, а положительный заряд смещается к хвосту второй молекулы.

И далее по такому же механизму продолжается рост цепи. В этой цепной реакции в отличие от радикальной полимеризации происходит не разделение -электронной пары мономера, а ее совместное перемещение с образованием карбкатиона.
Для инициирования роста цепи используют кислоты Льюиса, такие как трехфтористый бор. Применительно к ионной полимеризации их называют катализаторами. В присутствии небольших количеств воды или спиртов (называемых сокатализаторами) катализаторы образуют гидраты, существующие в виде ионных пар:

Здесь Н+ – инициирующий полимеризацию активный центр, а [F3BOH]- – противоион. В процессе полимеризации протон атакует -электроны мономера, начиная рост цепи, а анион [F3BOH]- сопровождает растущую цепь, постоянно следуя за карбкатионом.
Обрыв цепи при катионной полимеризации происходит в результате присоединения противоиона к карбкатиону растущей цепи и далее по схеме:
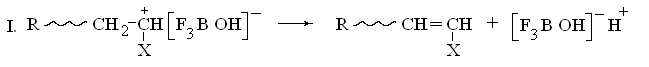
Эту реакцию переноса протона с регенерацией гидрата трехфтористого бора называют «осаждением ионной пары». Возможен и другой путь:

В обоих случаях происходит регенерация исходного катализатора.
В качестве катализаторов катионной полимеризации, кроме ВF3, используют также AlCl3, SnCl4, TiCl4. Примеры мономеров для катионной полимеризации: изобутилен, стирол, метилстирол, многие простые виниловые эфиры.
Анионная полимеризация
Известен другой тип ионной полимеризации, когда атаку -связи мономера осуществляет анион. Отрицательный заряд аниона отталкивает -электроны двойной связи по возможности дальше – на самый конец присоединяющейся молекулы мономера. Одновременно атакующий анион образует -связь с молекулой мономера, а смещаемые -электроны образуют карбанион.
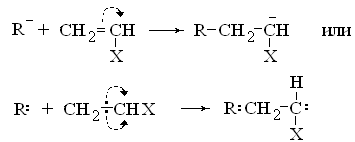
Образовавшийся карбанион атакует новую молекулу мономера, отталкивая ее -электроны к одному концу и присоединяя другим концом и т.д.
Таким образом, если в катионной полимеризации -электроны смещаются в сторону, противоположную росту цепи, то здесь – в направлении роста. Конечно, в анионной полимеризации тоже существует противоион (катион), постоянно следующий за растущей цепью.
В качестве катализатора анионной полимеризации используют металлоорганические соединения: бутиллитий, трифенилметилкалий, этилат натрия, амиды. Мономеры, полимеризуемые по анионному механизму: бутадиен, изопрен, стирол, акрилонитрил.
Интересно, что обрыв цепи здесь не обязателен. Если мономер и катализатор достаточно чисты, то реакция идет на 100%, и карбанионы на концах цепей остаются активными. Если к синтезированному полимеру добавить свежий мономер, то реакцию можно возобновить даже через несколько недель.
