
- •12 Дисперсные системы. Коллоидные растворы
- •12.1 Общие понятия о дисперсных системах
- •12.2 Коллоидные растворы
- •12.3 Методы получения коллоидных растворов
- •12.4 Оптические свойства коллоидных растворов
- •12.5 Кинетические свойства коллоидных растворов
- •12.6 Электрические свойства коллоидных растворов
- •12.7 Кинетическая и агрегативная устойчивость коллоидных систем
- •Золь Гель Твердый коллоид
- •Противоины в коллоидной частице Противоины в среде (а) Вода в коллоидной частице Вода в среде (б)
- •12.8 Коллоидные растворы в природе и технике
- •12.9 Вопросы для самоконтроля
- •Заключение по модулю 2 Химическая термодинамика. Растворы
12 Дисперсные системы. Коллоидные растворы
Истинные растворы содержат молекулы или атомы, размеры которых обычно не превышают 5∙10-9м (5 нм). При увеличении размеров частиц система становиться гетерогенной, состоящей из двух или более фаз с сильно развитой поверхностью раздела. Такие системы получили название дисперсных систем.
12.1 Общие понятия о дисперсных системах
Все дисперсные системы состоят из сплошной фазы, называемой дисперсионной средой, и прерывистой фазы (частиц), называемой дисперсной фазой. В зависимости от размера частиц дисперсные системы подразделяют на группы:
а) взвеси (суспензии, эмульсии), у которых частицы имеют размер 1000нм (10 -'6 м) и более;
б) коллоидные системы, размер частиц которых лежит в пределах от 1 до 500 нм (10 -9 м … 5 ∙ 10 - 7 м).
Дисперсные системы также классифицируются по агрегатным состояниям дисперсной фазы и дисперсионной среды.
Таблица 12.1 - Типы дисперсных систем
|
Тип дискретной системы |
Фазовое состояние |
Примеры |
|
|
Дисперсионной среды |
Дисперсной фазы |
||
|
Аэрозоль |
Газ |
Жидкая |
Туман, облака |
|
Аэрозоль |
Газ |
Твердая |
Дым, пыль |
|
Пена |
Жидкая |
Газ |
Взбитые сливки, мыльная пыль |
|
Эмульсия |
Жидкая |
Жидкая |
Молоко, Майонез |
|
Золь |
Жидкая |
Твердая |
Краски |
|
Твердая эмульсия |
Твердая |
Жидкая |
Масло |
|
Гель |
Твердая |
Жидкая |
Железо, Агар-агар |
12.2 Коллоидные растворы
Коллоидное состояние характерно для многих веществ, если их частицы имеют размер от 1 до 500 нм. Легко показать, что суммарная поверхность этих частиц огромна. Если предположить, что частицы имеют форму шара с диаметром 10 нм, то при общем объеме этих частиц 1 см3 они будут иметь площадь поверхности порядка 102 м2. Как указывалось ранее, поверхностный слой характеризуется поверхностной энергией и способностью адсорбировать те или иные частицы, в том числе ионы из раствора. Характерной особенностью коллоидных частиц является наличие на их поверхности заряда, обусловленного избирательной адсорбцией ионов. Коллоидная частица имеет сложное строение. Она включает в себя ядро, адсорбированные ионы, противоионы и растворитель. Существуют лиофильные (гидрофильные) коллоиды, в которых растворитель взаимодействует с ядрами частиц, и лиофобные (гидрофобные) коллоиды, в которых растворитель не взаимодействует с ядром частиц. Растворитель входит в состав гидрофобных частиц лишь как сольватная оболочка адсорбированных ионов или при наличии стабилизаторов (ПАВ), имеющих лиофобную и лиофильные части.
Несколько примеров коллоидных частиц:
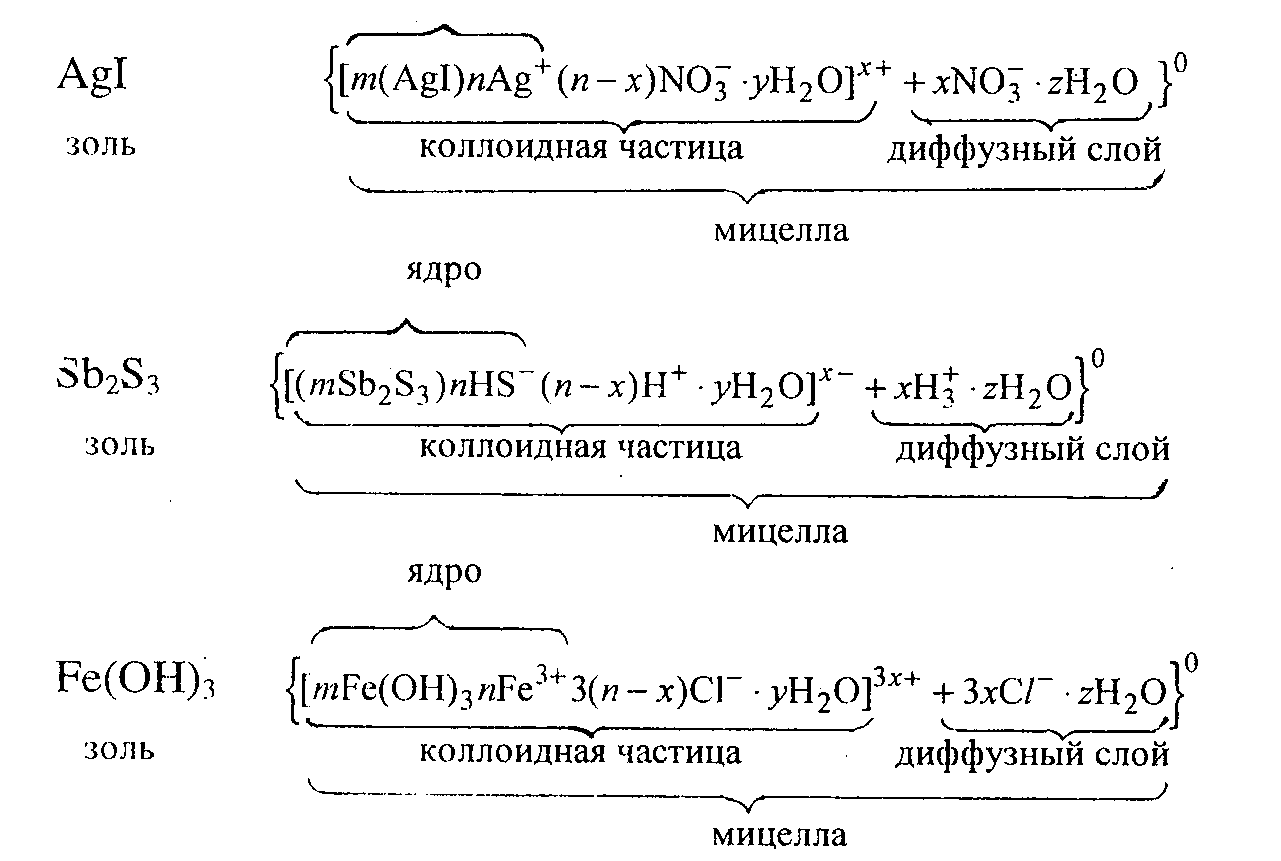
Как видно, ядро состоит из электронейтрального агрегата частиц с адсорбированными ионами элементов, входящих в состав ядра (в данных примерах ионами Ag+, HS", Fe3+). Коллоидная частица кроме ядра имеет противоионы и молекулы растворителя. Адсорбированные ионы и противоионы с растворителем образуют адсорбированный слой. Суммарно заряд частицы равен разности зарядов адсорбированных ионов и противоионов. Вокруг частиц находится диффузный слой ионов, заряд которых равен заряду коллоидной частицы. Коллоидная частица и диффузный слой образуют электронейтральную мицеллу.
