
- •Методичні вказівки до виконання практичних робіт з дисципліни «Теорія процесів окускування»
- •Практическая работа №1 Изучение прессуемости сыпучих материалов
- •1. Методы определения уплотняемости
- •2. Универсальная характеристика прессуемости
- •Практическая работа №2 Изучение диаграмм состояния физико-химических систем, существующих в окусковываемых железорудных шихтах
- •1. Теоретические предпосылки
- •2. Изучение диаграммы состояния Fe3o4–2FeO·SiO2 (основная система для спекания неофлюсованной шихты)
- •3. Изучение диаграммы состояния системы CaO–Fe2o3 (основная система для спекания офлюсованной шихты)
- •Практическая работа №3 Определение смачивания реальных твердых тел
- •Краткие теоретические сведения
- •Изучение форм гистерезиса смачивания
- •Практическая работа №4 Изучение методики расчета газодинамического сопротивления агломерационного слоя
- •Практическая работа №5 Изучение основных технологических параметров работы эксгаустера
- •1. Общие сведения
2. Изучение диаграммы состояния Fe3o4–2FeO·SiO2 (основная система для спекания неофлюсованной шихты)
После плавления фаялита в расплаве магнетита шихты температура плавления железистого силикатного расплава постепенно повышается (рис. 2.3 от точки С к точке А по стрелке). Окончательный состав расплава после растворения в нем больших количеств Fe3O4 показан на рис. 2.3 заштрихованной областью (соответствует концентрации компонентов перед началом кристаллизации – для аглошихты при ее спекании).
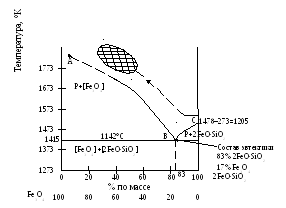
Рис. 2.3. Диаграмма состояния системы Fe3O4-2FeO·SiO2 (по Н.А. Островскому и Я.И. Ольшанскому)
3. Изучение диаграммы состояния системы CaO–Fe2o3 (основная система для спекания офлюсованной шихты)
Из диаграммы состояния системы (рис. 2.4) следует, что после плавления ферритов кальция и последующего растворения в расплаве Fe2O3 температура его (т.е. расплава) плавления снижается (на рис. 2.4 показано стрелкой).
Это же положение относится и к системе 2Fe2O3–2CaO·SiO2, в которой насыщение фаялита известью длительное время сопровождается понижением температуры плавления образующегося при этом известково-железистого оливина.

Рис. 2.4. Диаграмма состояния системы СаО–Fe2O3 (по Б. Филипсу и А. Муэну)
Выводы
Железистый силикатный расплав на основе фаялита, растворяя в себе магнетит, делается все более тугоплавким. Это позволяет твердой шихте перед растворением в расплаве нагреваться до весьма высоких температур. Теплота плавления затрачивается в этом случае при высоких температурах. Наоборот, плавясь, ферриты кальция образуют легкоплавкий расплав, температура плавления которого еще более понижается (при растворении в нем Fe2O3). Теплота плавления затрачивается здесь при низких температурах, что не позволяет нагреться шихте. Следовательно, форма линий ликвидуса в известной мере предопределяет температуру в зоне плавления.
Контрольные вопросы
1. Что такое диаграмма состояния системы?
2. Правило фаз (формулы, расшифровка значений).
3. Вид уравнения правила фаз при Р=const. Названия систем в зависимости от числа степеней свободы.
4. Диаграмма состояния однокомпонентной системы в координатах Р–Т (Н2О): ее вид – кривые плавления, кипения, сублимации; тройная точка (Р=0,61 кПа); критическая точка (t=374,2ºС; р=22,12 МПа) – исчезает различие между жидким и парообразным состоянием (конец кривой кипения).
5. Типичные двухкомпонентные диаграммы: а) эвтектического типа; б) с устойчивым химическим соединением; в) с неограниченной растворимостью компонентов в жидком и твердом состоянии.
6. Диаграмма состояния Fe3O4–2FeO·SiO2: (эвтектика 17% Fe3O4) после плавления фаялита по мере растворения в расплаве магнетита температура плавления расплава повышается, он становится более тугоплавким, шихта нагревается перед расплавлением.
7. Диаграмма состояния CaO–Fe2O3 (Филипс и Муэн) и аналогичная ей 2FeO·SiO2–2CaO·SiO2.
8. Каков общий вывод из изучения диаграмм состояния 2FeO·SiO2–Fe3O4 и CaO–Fe2O3?
Практическая работа №3 Определение смачивания реальных твердых тел
