
- •Тема: «Корабельные электрические аккумуляторы».
- •1. Назначение, принцип действия и основные технические характеристики химических источников тока
- •2. Устройство, электрохимические процессы, свойства и основные правила эксплуатации кислотных аккумуляторов.
- •3. Устройство, электрохимические процессы, свойства и основные правила эксплуатации щелочных аккумуляторов.
2. Устройство, электрохимические процессы, свойства и основные правила эксплуатации кислотных аккумуляторов.
Химические источники тока многократного действия, в которых в качестве электролита используют раствор кислоты Н2SO4 называются кислотными аккумуляторами.
Электрохимическая система такого аккумулятора имеет вид:
(-) Pb | H2SO4 | PbO2 (+) (1.1)
Поскольку электронды кислотных аккумуляторов в своем составе содержат свинец Pb, то они называются свингцово-кислотными аккумуляторами (СКА). Это наиболее распространенные в настоящее время ХИТ в мире.
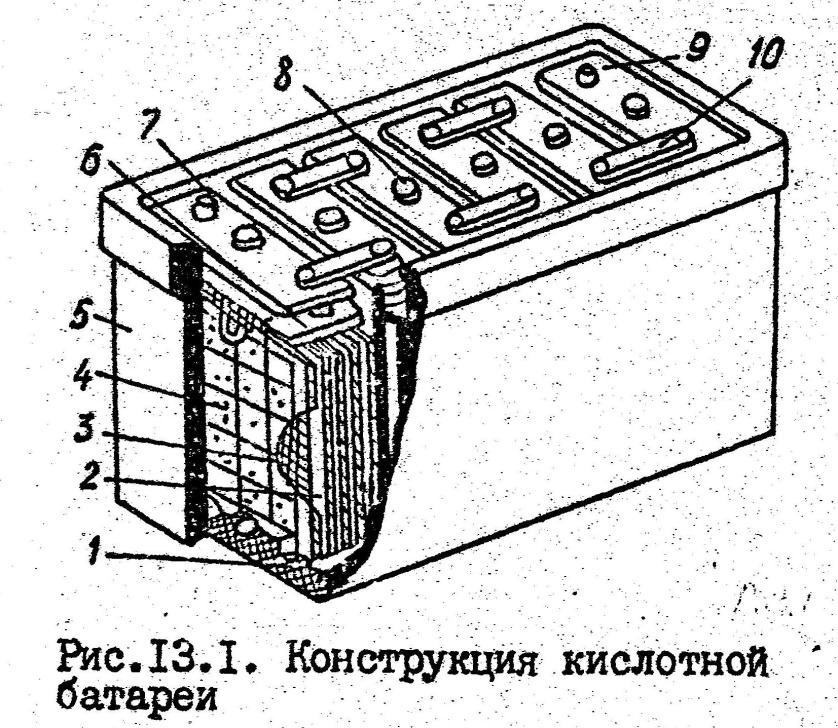
Устройство. Корабельные СКА имеют моноблочную конструкцию (рис.1.2), В едином корпусе (баке) размещают 6 аккумуляторов, соединенных последовательно. Бак выполняют из эбонита или стеклопластика и размещают в нем блоки положительных и отрицательных пластин, которые привариваются к баретке 6, имеющей вертикальный штырь - борн 9. Пластины электродов представляют собой решетку из сплавов свинца и сурьмы. В ячейки решетки запрессовывается активная масса, приготовленная в виде пасты из свинцового порошка в растворе кислоты с добавлением других материалов. За счет специальной технологии на положительных пластинах получают перекись свинца PbO2 темно-коричневого цвета, а на отрицательных - чистый губчатый свиней Pb - светло-серого цвета. Отрицательных пластин на одну больше, чем положительных, и они располагаются крайними, так как обладают большей механической прочностью по сравнению с положительными. Между отрицательными пластинами 2 и положительными пластинами 4 устанавливается сепаратор 3, который предохраняет пластины от замыкания между собой и способствует удержанию активной массы в решетках. В качестве сепараторов используют микропористые эбонитовые листы, а также пластмассы.
Пластины имеют в нижней части "ножки", которые опираются на специальные выступы на дне бака - донные призмы 5, благодаря которым на дне бака образуется так называемое шламовое пространство, в котором накапливается осадок. Установленные в баке блоки пластин закрывают крышками 7. В каждой крышке блока имеются два отверстия для борнов и одно отверстие для заливки электролита. Последнее закрывается вентиляционной пробкой 10. Пробка имеет отверстие для выхода газов. Аккумуляторы в батарее соединяются свинцовыми перемычками (межэлементными соединениями) 8. Все токоведущие детали изготавливают из свинца или свинцовых сплавов. Электролитом служит раствор серной кислоты в воде. Стандартом предусматривается специальная классификация серной кислоты - "аккумуляторная".
Корабельные аккумуляторы обозначаются следующим образом: первая цифра указывает число аккумуляторов в батарее, буквенные обозначения определяют назначение и режим использования, цифры после букв - емкость. Например, 6 СТК-180 М означает: 6 - количество аккумуляторов в моноблоке батарей; СТ - стартерная; К - катерная; 180 - емкость 180 А·ч; М- мипластовая сепарация.
Единичный моноблок батареи не всегда обеспечивает необходимое напряжение, силу тока, емкость и энергию для питания корабельных потребителей. Поэтому единичные моноблоки соединяют в аккумуляторные батареи (АБ). АБ состоят из аккумуляторов с одинаковыми характеристиками.

Для увеличения напряжения АБ применяется последовательное соединение п аккумуляторов (элементов) в батарею (рис.1.3,а), при котором UАБ=n·UЭЛ; IАБ=IЭЛ; CАБ=CЭЛ.
Для увеличения силы тока и емкости производится параллельное соединение n аккумуляторов (элементов) (рис. 1.3,б), при котором UАБ= UЭЛ; IАБ= n·IЭЛ; CАБ= n·CЭЛ.
При смешанном соединении аккумуляторы делят на т равных групп. В группе элементы соединяют последовательно, а сами группы между собой - параллельно (рис.1.3,в). Из схемы соединений следует, что UАБ= n·UЭЛ; IАБ= m·IЭЛ; CАБ= m·CЭЛ.
Мощность и энергия батареи из п элементов не зависят от схемы соединения. Корабельные АБ имеют удельную энергию 8-30 Вт·ч/кг и удельную емкость 6-12 А·ч/кг.
Срок службы корабельных кислотных АБ при правильной эксплуатации составляет не менее 3-х, а срок хранения - 5 лет.
Электрохимические протесы в кислотном аккумуляторе излагаются ниже по теории "двойной сульфатации". Суть этой теории заключается в том, что во время разряда аккумулятора сульфат свинца образуется как на положительном, так и на отрицательном электроде. В исходном состоянии серная кислота в электролите диссоциирует на ионы H+ и HSO-4.

Разряд (рис.1.4,а). При растворении на отрицательном электроде свинец выделяет ионы Pb2+ в раствор. При замкнутой внешней цепи два электрона 2е с отрицательного электрода перемещаются к положительному. На самом электроде ионы свинца Pb2+ вступают в реакцию с ионами HSO-4 и образуют сульфат свинца PbSO4 и ионы водорода H+. Сульфат свинца, поскольку он практически нерастворим в электролите, покрывает поверхность отрицательного электрода.
На положительном электроде двуокись свинца PbSO4 переходит в раствор в ограниченном количестве, так как при обычных условиях она нерастворима в воде. Малые количества двуокиси в соединении с водой ионизируются в четырехвалентные ионы свинца Pb4+ и одновалентные ионы OH- согласно уравнению
PbO2+2H2O → Pb4++4OH- (1.2)
Четырехвалентный свинец восстанавливается поступающими из внешней цепи электронами до двухвалентного. Двухвалентный свинец вступает в реакцию с ионами HSO-4 образуя сульфат свинца PbSO4 и ион водорода Н+. Сульфат свинца оседает на положительном электроде.
Из рисунка видно, что на каждые две молекулы серной кислоты образуется четыре молекулы воды, но две из них расходуются у положительного электрода. В итоге изменение электролита сводится к образованию двух молекул воды. При этом наблюдается расход кислоты. Практически это означает, что плотность электролита уменьшается при разряде и служит мерой разряженности аккумулятора.
3аряд (рис. 1.4,б). Под действием электрического поля источника питания (генератора постоянного тока G или выпрямительного агрегата для заряда) сульфат свинца у обоих электродов ионизируется на границе с электролитом.
На отрицательном электроде двухвалентные ионы свинца получают электроны из внешней цепи и восстанавливаются до чистого свинца. Ионы SO2-4 с ионами Н+ образуют серную кислоту H2SO4.
На положительном электроде двухвалентные ионы свинца отдают два электрона во внешнюю цепь, превращаясь в четырехвалентные. Затем каждый из этих ионов через промежуточные реакции соединяется с двумя ионами кислорода, образуя двуокись свинца. Ионы SO2-4 соединяясь с ионами Н+, образуют серную кислоту H2SO4.. При заряде кислота восстанавливается, и плотность электролита увеличивается.
Токообразующие реакции при заряде и разряде имеют вид:
- на отрицательном электроде
(-)
Pb+HSO-4-2е
 PbSO4+H+
(1.3)
PbSO4+H+
(1.3)
- на положительном электроде
(-)
PbO2+3Н++HSO-4+2е
 PbSO4+2H2O
(1.4)
PbSO4+2H2O
(1.4)
При этом ионы водорода H+ с отрицательной пластины переходят через электролит на положительную пластину. Одновременно два электрона 2е по внешней цепи аккумулятора переходят с отрицательной пластины на положительную, т.е. по внешней цепи протекает электрический ток.
Результирующая реакция:
(+)
PbO2+2H2SO-4+(-)Pb
 2PbSO4+2H2O
(1.4)
2PbSO4+2H2O
(1.4)
Кроме основных токообразующих реакций в аккумуляторе протекает и ряд других реакций. Двуокись свинца химически взаимодействует со свинцовой решеткой. Оба электрода в бездействии могут взаимодействовать с электролитом с выделением водорода на отрицательном электроде и кислорода - на положительном. Эти процессы газовыделения усиливаются во время заряда. К концу заряда, когда активные вещества будут полностью восстановлены, газовыделение резко возрастает, так как подводимая энергия расходуется на разложение воды.
Свойства и правила эксплуатации. Емкость аккумулятора в процессе эксплуатации зависит от степени использования активных материалов электродов. При разряде на обоих электродах образуется сульфат свинца с низкой электропроводностью. При этом пористость электродов уменьшается, поскольку удельный объем сульфата свинца больше удельных объемов свинца и двуокиси свинца. Это приводит к ограничению доступа электролита вглубь пластин и увеличивает внутреннее сопротивление аккумулятора. Так, при разряде малыми токами (8-10-ти часового режима) активная масса используется на 40-50%, а при разряде большими токами - лишь на 5-10%. Это обусловлено прежде всего экранированием активной массы пластин сульфатом свинца (пассивацией пластин), а также концентрационной поляризацией (резким снижением концентрации серной кислоты в порах электродов).
Потери емкости аккумулятора достигают, например, 2-3% в месяц при температуре 10 С. Однако саморазряд возрастает при увеличении срока службы аккумулятора, концентрации и температуры его электролита и может составлять 1% в сутки.
Изменяется величина емкости С и со сроком службы. Вначале она увеличивается за счет переработки пасты в активные вещества (рис.1.5,а). В дальнейшем емкость С постепенно уменьшается, поскольку с увеличением срока службы активная месса отрицательных пластин уплотняется, а положительных, наоборот, разрыхляется. При этом происходит сдавливание электродов, а объем кислоты между ними уменьшается. Из-за изменения объема нарушается контакт между остовом пластин (решеткой) и активной массой. Это приводит к выпаданию активной массы и преждевременному износу аккумулятора.

Емкость аккумулятора при разряде можно определить приближенно с помощью выражения:
C= (1.6)
(1.6)
где d - измеренная и приведенная к температуре +15° С плотность электролита;
dном- номинальная плотность (1.280±0.005 г/см2);
dкон- допустимая конечная плотность электролита (1.130-1.140 г/см2).
Свойства при разряде СКА. Характер изменения ЭДС при разряде (рис.1.5,б) в значительной степени определяется характером изменения плотности электролита. Зависимость ЭДС Е от плотности d определяется приближенным выражением:
E=d+0.84 (1.7)
В первый момент разряда электролит в порах пластин быстро расходуется, и его плотность d резко снижайся. Одновременно снижаются величины ЭДС Е и напряжения U . Вследствие диффузии электролита из бака в поры пластин значения d , E и U несколько возрастают. В момент времени t1 наступает равновесное состояние. С момента t1 и до конца разряда в момент tкон скорость поступления электролита, в поры снижается, поскольку сульфат свинца постепенно закупоривает устья пор активных масс пластин. При этом сопротивление аккумулятора R0 возрастает, и падение напряжения увеличивается. С момента времени tкон (конечное время разряда) поступление электролита в поры практически прекращается, и ЭДС Е резко уменьшается.
После размыкания внешней цепи плотность электролита d в порах и баке выравнивается, и ЭДС Е несколько возрастает.
Конец разряда определяется конечным напряжением. Величина Uкон зависит от режима разряда. Так, при разряде токов одночасового режима в токообразующей реакции используется в основном верхняя часть активной массы пластин, поэтому допускается конечное напряжение Uкон= 1,6 В. При разряде силой тока длительных режимов, например, десятичасового или двадцатичасового, допускается разряд до конечного напряжения Uкон= 1,7 В и Uкон= 1,75 В соответственно.
Свойства при разряде СКА. Изменение ЭДС при заряде (рис.1.5,в) определяется изменением плотности электролита аккумулятора. Вначале в порах активных масс электродов идет интенсивно выделение серной кислоты, и плотность электролита d в них становится выше, чем плотность электролита в остальном объеме бака. Затем, вследствие диффузии электролита из бака (с меньшей плотностью d ) в поры (с большей плотностью d ) происходит снижение плотности электролита в порах, и в момент t1 наступает равновесие.
В промежутке времени t1-t2 плотность электролита растет как в порах, так и в баке, и соответственно увеличивается ЭДС. В момент времени t2 начинается интенсивное газовыделение. Затем ЭДС газовой поляризации увеличивает общую ЭДС аккумулятора и делает ее практически независимой от плотности электролита.
В процессе заряда измерение плотности электролита ведется в верхних слоях аккумуляторного бака, гае величина d значительно меньше, чем в нижних слоях. Выравнивание плотности по всему объему бака происходит только с началом интенсивного газовыделения, когда пузырьки газа перемешивают электролит. К моменту времени t3 процессы восстановления активных веществ завершаются. Продолжение заряда имеет целью разрыхлить активную массу на электродах и перемешать электролит по всему объему бака. В коние заряда ЭДС и плотность электролита становятся постоянными :Е=const , d=const. После прекращения заряда (момент времени t4) действие газовой поляризации прекращается, и ЭДС понижается до установившегося значения Екон.
Конец заряда определяется по постоянству напряжения и плотности электролита (не менее 1,280 + 0,005 г/см3) в течение двух часов у большинства элементов батареи, а также по обильному газовыделению.
Обильное газовыделение в конце зарядки происходит в результате электролиза воды:
2Н2О→2Н2↑+О2↑ (1.8)
Основные правила эксплуатации СКА. В процессе эксплуатации СКА производятся зарядки и контрольно-тренировочныe циклы аккумуляторных батарей.
На надводных кораблях производят чаще всего двухступенчатое (полные) зарядки АБ, которые включают в себя:
-
зарядку аккумуляторов при плотности электролита менее.1,230 г/см3 током 1 ступени (величина которого равна ориентировочно 1/8 - 1/10 емкости аккумулятора);
-
переход на 2 ступень зарядки (величина тока которой равна половине тока 1 ступени) при достижении напряжения заряда Uзар=2,4 В у большинства аккумуляторов батареи;
- окончание зарядки АБ при постоянстве напряжения и плотности электролита d в течение 2-х часов.
При плотности электролита, равной или большей 1,230 г/см3, допускаются одноступенчатые (неполные) зарядки АБ сразу током 2 ступени, но окончание зарядки производят аналогично полной зарядке.
Контрольно – тренировочный цикл АБ включает в себя:
-
зарядку батареи током 2 ступени первого заряда до постоянства плотности электролита и напряжения в течение 3-х часов;
-
обмер плотности электролита всех аккумуляторов и при необходимости корректировка плотности до нормальной (либо дистиллированной водой, либо электролитом с плотностью 1,400 г/см3);
- разрядку батарей током 10-часового режима (величина определяется по паспорту АБ) с замером каждый час (в конце разряда - каждые 30 минут) напряжения у всех аккумуляторов до снижения напряжения хотя бы у одного из них до 1,7 В. По достижении этого конечного напряжения разрядку батареи следует прекратить;
- подсчет емкости АБ, приведенной к температуре+30° С, по формуле
Спр= (1.9)
(1.9)
где Спр - емкость, приведенная к температуре 30° C, А·ч;
Сф – фактическая - емкость, полученная при разряде, А·ч;
Т - средняя температура электролита во время разряда, ° C;
- зарядку батареи полным двухступенчатым режимом.
В процессе эксплуатации емкость АБ должна быть не менее 80%. Если емкость АБ после контрольно-тренировочного цикла будет ниже 80% Сном, следует повторить цикл заряд-разряд (для АБ в консервации емкость не должна быть ниже 90% Сном).
Для увеличения срока эксплуатации СКА необходимо:
-
производить в течение месяца не менее одной полной двухступенчатой зарядки;
-
проводить один раз в 6 месяцев контрольно-тренировочный цикл;
- не допускать разряда ниже 1,7 В на аккумуляторе.
Для приготовления СКА к зарядке следует:
-
включить в работу вытяжную вентиляцию и не останавливать ее до конца зарядки;
-
произвести осмотр № 1 согласно руководящим документам;
-
проверить напряжение на клеммах каждого аккумулятора;
-
открыть вентиляционные пробки;
-
проверить плотность и уровень электролита (неменее 10-15 мм), при необходимости их откорректировать.
Во время зарядки СКА необходимо:
-
следить за постоянством величины зарядного тока и работой вытяжной вентиляции;
-
через каждый час измерять напряжение и температуру электролита (не допуская ее увеличения выше 45 С) у трех контрольных элементов батареи;
-
при достижении напряжения 2,4 В у большинства элементов батареи перейти на 2 ступень, снизив наполовину величину зарядного тока.
По окончании зарядки СКА требуется:
-
отключить батарею от источника;
- протереть аккумуляторы ветошью с 5 %-м раствором соды, а затем сухой ветошью;
-
закрыть вентиляционные пробки;
-
проверить крепление контактов, смазать межэлементные соединения и шины вазелином.
Основные неисправности СКА:
1. Повышенный саморазряд. Для улучшения механических характеристик в свинец решеток пластин АБ добавляется сурьма (3-12%). При работе батареи решетка положительного электрода подвергается коррозии и сурьма переходит в раствор. Оседая на отрицательном электроде, сурьма способствует выделению водорода и увеличивает скорость коррозии, что приводит к увеличению саморазряда СКА. Причиной» повышенного саморазряда является также попадание в электролит примесей (солей железа, морской воды и др.).
2. Сульфатация. Возникает при хранении батареи в разряженном состоянии, систематических недозарядках и чрезмерно глубоких разрядах, а также при чрезмерно высокой плотности электролита. При разряде и заряде АБ с большими токами пластины покрываются сульфатом свинца PbSO4, который не разлагается при обычных зарядах. Для восстановления емкости батареи с сульфатированными электродами электролит заменяют дистиллированной водой (или разбавляют) и заряжают малыми токами. В разбавленном электролите растворимость сульфата свинца выше, чем в нормальном.
3. Короткие замыкания. Причинами коротких замыканий могут быть накопления высокого слоя шлама, коробление электродов, разбухание пластин, приводящее к образованию "мостиков" между электродами. При зарядах сульфат свинца переходит в рыхлую модификацию двуокиси свинца и осыпается, что также способствует коротким замыканиям батарей с большим сроком служб.
Недостатки СКА: повышенная чувствительность к чистоте электролита, перерывам в зароде, недозарядам, интенсивному газовыделению; наличие саморазряда, увеличивающегося со сроком службы: выделение в атмосферу аэрозолей серной кислоты, сурьмы и пр. При попадании внутрь аккумулятора морской воды наряду с другими газами выделяется хлор, представляющий опасность для личного состава корабля.
