
- •Контрольное тестирование по физике
- •Де n1. Механика.
- •1. Кинематика поступательного и вращательного движения
- •2. Динамика поступательного движения
- •3. Динамика вращательного движения
- •4. Работа. Энергия
- •5. Законы сохранения в механике
- •6. Элементы специальной теории относительности
- •Де n2. Молекулярная (статистическая) физика и термодинамика.
- •7. Средняя энергия молекул
- •8. Распределения Максвелла и Больцмана
- •9. Первое начало термодинамики. Работа при изопроцессах
- •10. Второе начало термодинамики. Энтропия
- •Де n3. Электричество и магнетизм.
- •11. Электростатическое поле в вакууме
- •12. Законы постоянного тока
- •13. Магнитостатика
- •14. Электрические и магнитные свойства вещества
- •15. Явление электромагнитной индукции
- •16. Уравнения Максвелла
- •Де n4. Механические и электромагнитные колебания и волны.
- •17. Свободные и вынужденные колебания
- •18. Сложение гармонических колебаний
- •19. Волны. Уравнение волны
- •20. Энергия волны. Перенос энергии волной
- •Де n5. Волновая и квантовая оптика.
- •21. Интерференция и дифракция света
- •22. Поляризация и дисперсия света
- •23. Эффект Комптона. Световое давление
- •24. Тепловое излучение. Фотоэффект
- •Де n6. Квантовая физика и физика атома.
- •25. Дуализм свойств микрочастиц. Соотношение неопределенностей Гейзенберга
- •26. Спектр атома водорода. Правило отбора
- •27. Уравнение Шредингера (общие свойства)
- •28. Уравнение Шредингера (конкретные ситуации)
- •Де n7. Элементы ядерной физики и физики элементарных частиц.
- •29. Фундаментальные взаимодействия
- •30. Ядро. Элементарные частицы
- •31. Ядерные реакции.
- •32.Законы сохранения в ядерных реакциях
Де n2. Молекулярная (статистическая) физика и термодинамика.
7. Средняя энергия молекул
Средняя кинетическая
энергия молекул газа при температуре
![]() зависит
от их конфигурации и структуры, что
связано с возможностью различных видов
движения атомов в молекуле и самой
молекулы. При условии, что имеет место
поступательное, вращательное движение
молекулы как целого и колебательное
движение атомов в молекуле, средняя
кинетическая энергия молекулы кислорода
(
зависит
от их конфигурации и структуры, что
связано с возможностью различных видов
движения атомов в молекуле и самой
молекулы. При условии, что имеет место
поступательное, вращательное движение
молекулы как целого и колебательное
движение атомов в молекуле, средняя
кинетическая энергия молекулы кислорода
(![]() )
равна …
)
равна …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение:
Для
статистической системы в состоянии
термодинамического равновесия на каждую
поступательную и вращательную степени
свободы приходится в среднем кинетическая
энергия, равная
![]() ,
а на каждую колебательную степень –
,
а на каждую колебательную степень –
![]() Средняя
кинетическая энергия молекулы равна:
Средняя
кинетическая энергия молекулы равна:
![]() .
Здесь
.
Здесь
![]() –
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы:
–
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы:
![]() ,
где
,
где
![]() –
число степеней свободы поступательного
движения, равное 3;
–
число степеней свободы поступательного
движения, равное 3;
![]() –
число степеней свободы вращательного
движения, которое может быть равно 0, 2,
3;
–
число степеней свободы вращательного
движения, которое может быть равно 0, 2,
3;
![]() –
число степеней свободы колебательного
движения, минимальное количество которых
равно 1.
Для молекулярного кислорода
(двухатомной молекулы)
–
число степеней свободы колебательного
движения, минимальное количество которых
равно 1.
Для молекулярного кислорода
(двухатомной молекулы)
![]() ,
,
![]() и
и
![]() .
Следовательно,
.
Следовательно,
![]() .
Тогда средняя энергия молекулы кислорода
(
.
Тогда средняя энергия молекулы кислорода
(![]() )
равна:
)
равна:
![]() .
.
Если не учитывать колебательные движения в молекуле водорода при температуре 200 К, то кинетическая энергия в (Дж) всех молекул в 4 г водорода равна …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение:
Средняя
кинетическая энергия одной молекулы
равна:
![]() ,
где
,
где
![]() –
постоянная Больцмана,
–
постоянная Больцмана,
![]() –
термодинамическая температура;
–
термодинамическая температура;
![]() –
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы
–
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы
![]() .
Молекула водорода
.
Молекула водорода
![]() имеет
3 поступательные и 2 вращательные степени
свободы, следовательно,
имеет
3 поступательные и 2 вращательные степени
свободы, следовательно,
![]() В
4 г водорода содержится
В
4 г водорода содержится
![]() молекул,
где
молекул,
где
![]() масса
газа,
масса
газа,
![]() молярная
масса водорода,
молярная
масса водорода,
![]() число
Авогадро. Кинетическая энергия всех
молекул будет равна:
число
Авогадро. Кинетическая энергия всех
молекул будет равна:
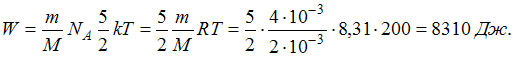
Если не учитывать колебательные движения в молекуле углекислого газа, то средняя кинетическая энергия молекулы равна …
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение:
Средняя
кинетическая энергия молекулы равна:
![]() ,
где
,
где
![]() –
постоянная Больцмана,
–
постоянная Больцмана,
![]() –
термодинамическая температура;
–
термодинамическая температура;
![]() –
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
–
сумма числа поступательных, вращательных
и удвоенного числа колебательных
степеней свободы молекулы:
![]() .
Для молекулы углекислого газа
.
Для молекулы углекислого газа
![]() число
степеней свободы поступательного
движения
число
степеней свободы поступательного
движения
![]() ,
вращательного –
,
вращательного –
![]() ,
колебательного –
,
колебательного –
![]() ,
поэтому
,
поэтому
![]() Следовательно,
средняя кинетическая энергия молекулы
Следовательно,
средняя кинетическая энергия молекулы
![]() равна:
равна:
![]() .
.
1. Кинетическая энергия всех
молекул в 2 г неона при температуре 300 К
в
![]() равна …
равна …
|
|
|
|
|
|
|
|
|
Решение: Средняя
кинетическая энергия одной молекулы
равна
![]() , где
, где
![]() – постоянная Больцмана,
– постоянная Больцмана,
![]() – термодинамическая температура,
– термодинамическая температура,
![]() – сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы
– сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы
![]() . Молекула неона
. Молекула неона![]() имеет 3 поступательные степени свободы,
следовательно,
имеет 3 поступательные степени свободы,
следовательно,
![]() . В 2 г неона содержится
. В 2 г неона содержится
![]() молекул, где
молекул, где
![]() масса газа,
масса газа,
![]() молярная масса неона,
молярная масса неона,
![]() число Авогадро. Кинетическая энергия
всех молекул будет равна:
число Авогадро. Кинетическая энергия
всех молекул будет равна:
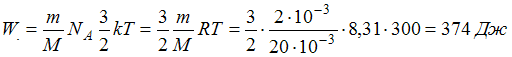 .
.
2. При комнатной температуре
отношение молярных теплоемкостей при
постоянном давлении и постоянном объеме
![]() равно
равно
![]() для
газа …
для
газа …
|
|
гелия |
|
водяного пара |
|
воздуха |
|
кислорода |
Решение:
Из отношения
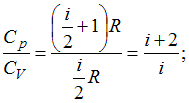
![]() найдем
найдем
![]() ,
,
![]() .
Только 3 поступательные степени свободы
имеют одноатомные газы, следовательно,
это газ гелий.
.
Только 3 поступательные степени свободы
имеют одноатомные газы, следовательно,
это газ гелий.
3. В соответствии с законом равномерного
распределения энергии по степеням
свободы средняя кинетическая энергия
молекулы идеального газа при температуре
T равна:
![]() .
Здесь
.
Здесь
![]() ,
где
,
где
![]() ,
,
![]() и
и
![]() –
число степеней свободы поступательного,
вращательного и колебательного движений
молекулы соответственно. Для гелия (
–
число степеней свободы поступательного,
вращательного и колебательного движений
молекулы соответственно. Для гелия (![]() )
число i равно …
)
число i равно …
|
|
3 |
|
5 |
|
7 |
|
6 |
Решение: Для статистической
системы в состоянии термодинамического
равновесия на каждую поступательную и
вращательную степени свободы приходится
в среднем кинетическая энергия, равная
![]() ,
а на каждую колебательную степень –
,
а на каждую колебательную степень –
![]() .
Средняя кинетическая энергия молекулы
равна:
.
Средняя кинетическая энергия молекулы
равна:
![]() .
Здесь
.
Здесь
![]() –
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы:
–
сумма числа поступательных, числа
вращательных и удвоенного числа
колебательных степеней свободы молекулы:
![]() ,
где
,
где
![]() –
число степеней свободы поступательного
движения, равное 3;
–
число степеней свободы поступательного
движения, равное 3;
![]() –
число степеней свободы вращательного
движения, которое может быть равно 0, 2,
3;
–
число степеней свободы вращательного
движения, которое может быть равно 0, 2,
3;
![]() –
число степеней свободы колебательного
движения, минимальное количество которых
равно 1.
Для гелия (
–
число степеней свободы колебательного
движения, минимальное количество которых
равно 1.
Для гелия (![]() )
(одноатомной молекулы)
)
(одноатомной молекулы)
![]() ,
,
![]() и
и
![]() .
Следовательно,
.
Следовательно,
![]() .
.
