
- •Кислотно-основное титрование
- •Контрольные вопросы
- •Лабораторная работа № 1. Приготовление рабочего раствора соляной кислоты
- •Посуда и реактивы
- •Ход работы
- •Методика определения плотности с помощью пикнометра
- •Методика определения плотности с помощью ареометра
- •Лабораторная работа № 2 Приготовление стандартного раствора тетрабората натрия
- •Посуда и реактивы
- •Ход работы
- •Взятие навески методом присыпания
- •Взятие навески методом отсыпания
- •Ход работы Установление титра и молярной концентрации раствора соляной кислоты методом пипетирования.
- •Установление титра и молярной концентрации раствора соляной кислоты методом отдельных навесок
- •Ход работы
- •Лабораторная работа №5 Определение содержания NaOh и Na2co3 в растворе при их совместном присутствии
- •Посуда и реактивы
- •Ход работы
- •Комплексонометрическое титрование
- •Контрольные вопросы
- •Лабораторная работа №6 Установление титра и молярной концентрации эквивалента рабочего раствора комплексона III
- •Посуда и реактивы
- •Ход работы
- •Лабораторная работа №7 Определение общей жесткости воды методом комплексонометрического титрования
- •Посуда и реактивы
- •Ход работы
- •Лабораторная работа №8 Определение содержания ионов кальция и магния при их совместном присутствии в растворе
- •Посуда и реактивы
- •Ход работы
- •Окислительно-восстановительное (редоксиметрическое) титрование
- •Контрольные вопросы
- •Лабораторная работа №10
- •Установка титра методом отдельных навесок
- •Лабораторная работа №11
- •Перманганатометрическим методом.
- •Посуда и реактивы
- •Лабораторная работа №12 Определение содержания пероксида водорода в растворе
- •Посуда и реактивы
- •Лабораторная работа №13
- •Бихроматометрическим методом
- •Посуда и реактивы
- •Приготовление стандартного раствора бихромата калия
- •Приготовление контрольного раствора соли Мора
- •Литература.
- •Методические указания
- •Ротапринт ТюмГнгу, 625036, Тюмень, Володарского 38
Ход работы
В мерной колбе готовят раствор смеси солей Na2CO3 и NaHCO3. Для приготовления 100,0 мл раствора на аналитических весах берут точные навески Na2CO3 в пределах 0,53 г и NaHCO3 в пределах 0,84 г. Навески количественно переносят в мерную колбу, растворяют в дистиллированной воде; доводят объем до кольцевой отметки и тщательно перемешивают.
Пипеткой Мора отбирают аликвотную часть приготовленного раствора; переносят в колбу для титрования; добавляют 1–2 капли фенолфталеина. Раствор при этом окрашивается в малиновый цвет.
Бюретку для титрования промывают и заполняют 0,1М раствором HCl. Уровень жидкости в бюретке устанавливают на нулевом делении шкалы по нижнему мениску на уровне глаз, а капилляр бюретки опускают в колбу для титрования таким образом, чтобы он не касался поверхности титруемого раствора.
Титрование контрольного раствора смеси Na2CO3 и NaHCO3 проводят до его обесцвечивания от одной избыточной капли титранта. Фиксируют объем HCl (V1), израсходованный на титрование с фенолфталеином. Затем в колбу прибавляют 1–2 капли метилового оранжевого и, не доливая кислоту в бюретку, продолжают титровать до появления оранжевой окраски. Фиксируют общий объем HCl (V2), израсходованный на титрование с двумя индикаторами: фенолфталеином и метиловым оранжевым.
Титрование проводят несколько раз до получения трех сходящихся результатов.
Содержание Na2CO3 и NaHCO3 в контрольном растворе смеси рассчитывают по формулам:
![]()
![]()
где C(HCl) – молярная концентрация раствора HCl, моль/л;
V1 – объем раствора HCl, израсходованный на титрование с фенолфта-
леином, мл;
V2 – общий объем раствора HCl, израсходованный на титрование с
фенолфталеином и метиловым оранжевым, мл;
![]() –
молярная масса эквивалента Na2CO3,
г/моль экв;
–
молярная масса эквивалента Na2CO3,
г/моль экв;
M(NaHCO3) – молярная масса эквивалента NaHCO3, г/моль экв;
Vобщ. – общий объем контрольного раствора смеси Na2CO3 и NaHCO3,
мл;
Vал. – объем аликвоты контрольного раствора смеси Na2CO3 и NaHCO3,
мл.
Рассчитывают процентный состав смеси. Проводят статистическую обработку результатов.
Лабораторная работа №5 Определение содержания NaOh и Na2co3 в растворе при их совместном присутствии
Цель работы – ознакомиться с условиями определения NaOH и Na2CO3 в
растворе при их совместном присутствии методом кислот-
но-основного титрования с двумя индикаторами;
определить содержание NaOH и Na2CO3 в образце щелочи.
Посуда и реактивы
Бюретка емкостью 25 мл;
мерная колба емкостью 100 мл;
пипетка Мора емкостью 10 или 15 мл;
колба для титрования;
раствор HCl, 0,1 М;
NaOH(х. ч.);
индикатор фенолфталеин;
индикатор метиловый оранжевый.
Гидроксид натрия (как и другие щелочи) легко поглощает из воздуха оксид углерода (IV) и частично превращается в карбонат натрия:
2NaOH + CO2=Na2CO3 + H2O
Количественный анализ смеси NaOH и Na2CO3 методом кислотно-основного титрования основан на определении двух точек эквивалентности. Первая точка эквивалентности достигается после протекания реакций:
NaOH + HCl=NaCl + H2O
Na2CO3 + HCl=NaCl + NaHCO3
В первой точке эквивалентности:
![]()
Эту точку фиксируют с помощью индикатора фенолфталеина, интервал перехода которого составляет 8÷10.
Вторая точка эквивалентности достигается после завершения реакции:
![]()
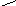
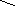
![]()
Во второй точке эквивалентности:
![]()
Эту точку эквивалентности фиксируют с помощью индикатора метилового оранжевого, интервал перехода которого составляет 3,1÷4,4.
Из уравнений реакций видно, что с фенолфталеином оттитровывается весь NaOH и половина Na2CO3. Оставшаяся половина Na2CO3 дотитровывается с метиловым оранжевым.
