
- •Образец оформления работы по качественному функциональному анализу
- •1. Реакции непредельных соединений
- •1.1. Тест на растворимость
- •1.2. Реакции ненасыщенных соединений с бромом
- •1.3. Окисление ненасыщенных соединений перманганатом калия
- •1.4. Образование и свойства этилена
- •1.6. Тест на присутствие в ненасыщенном соединении гидропероксидов
- •2. Реакции спиртов
- •2.1. Взамодействие спиртов с натрием
- •2.2. Реакции окисления спиртов
- •Окисление спиртов хромовой кислотой
- •Окисление этанола перманганатом калия
- •2.3. Реакции спиртов с неорганическими кислотами
- •2.3.1. Взаимодействие спиртов с серной кислотой
- •2.3.2. Взаимодействие одноатомных спиртов с борной кислотой
- •Обнаружение пероксидов в простых эфирах
- •3. Реакции вицинальных гликолей (1,2-диолов)
- •3.1. Реакция комплексообразования виц-диолов
- •3.1.1. Взаимодействие виц-диолов с борной кислотой
- •3.1.2. Взаимодействие виц-диолов с гидроксидом меди(II)
- •4. Реакции фенолов
- •4.1. Тест на растворимость фенолов
- •4.2. Комплексообразование фенолов с хлоридом железа(III)
- •4.3. Реакция фенолов с бромом
- •4.4. Реакции окисления фенолов
- •4.4.1. Окисление перманганатом калия
- •4.4.2. Окисление хромовой кислотой
- •5. Реакции диазотирования ароматических аминов
- •5.1. Диазотирование анилина
- •5.2. Образование азокрасителей реакциями азосочетания
- •5.2.1. Азосочетание с аминами
- •5.2.2. Азосочетание с фенолами
- •5.2.3. Окраска ткани азокрасителями
- •6. Реакции карбонильных соединений
- •6.1. Реакции альдегидов и кетонов по карбонильной группе
- •6.1.1. Реакция с 2,4-динитрофенилгидразином
- •6.1.2. Реакция с бисульфитом натрия
- •6.1.3. Реакция с сульфитом натрия
- •6.1.4. Реакция альдегидов с фуксинсернистой кислотой (реакция Шиффа)
- •6.2. Реакции окисления альдегидов
- •6.2.1. Окисление альдегидов хромовой смесью
- •6.2.2. Окисление альдегидов реактивом Фелинга
- •6.3. Реакции енольных форм
- •6.3.1. Образование дибензальацетона
- •6.3.2. Иодоформная проба
- •6.3.3. Реакция устойчивых енольных форм с хлоридом железа(III)
- •7. Реакции окси- и аминокислот
- •7.1. РеакциИ оксикислот с хлоридом железа(III)
- •7.1.1. Реакции алифатических оксикислот с хлоридом железа(III)
- •7.1.2. Реакции оксибензойных кислот с хлоридом железа(III)
- •7.2. РеакциИ коМплексообразования с участием
- •7.2.1. Реакции α-аминокислот с хлоридом железа(III)
- •7.2.2. Реакции α-аминокислот с солями меди(II)
- •7.3. Реакция аминокислот с нингидрином (реакция Руэманна)
- •7.4. Реакция аминокислот с формальдегидом
- •8. Реакции углеводов
- •8.1. Общая реакция на углеводы с -нафтолом (реакция Молиша)
- •8.2. Реакция Селиванова на кетозы
- •8.3. Взаимодействие сахаров с солями двухвалентной меди в щелочном растворе
- •8.3.1. Доказательство наличия вицинальных гидроксильных групп
- •8.3.2. Окисление восстанавливающих сахаров соединениями двухвалентной меди (реакция Троммера)
- •8.4. Окисление моносахаридов йодом
2.3.2. Взаимодействие одноатомных спиртов с борной кислотой
При взаимодействии спиртов с борной кислотой образуются триалкилбораты:
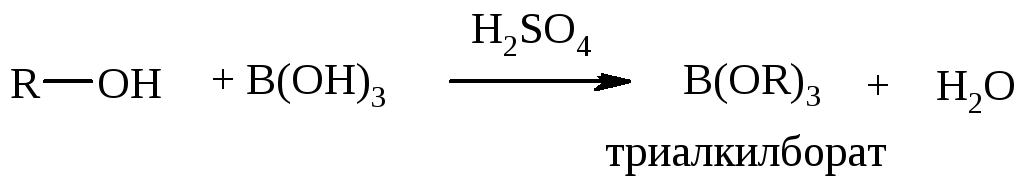
Триметил- и триэтилборат летучи и окрашивают пламя в зеленый цвет.
Выполнение работы
|
Реактивы |
Исследуемые вещества |
|
серная кислота (конц.), борная кислота |
этанол |
В пробирку наливают 1 мл этанола, добавляют 1 мл концентрированной серной кислоты и 0.5-1 г борной кислоты. Содержимое пробирки перемешивают стеклянной палочкой, которую затем помещают в пламя спиртовки. Наблюдают появление зеленой окраски пламени.
-
Обнаружение пероксидов в простых эфирах
При хранении простых эфиров на воздухе в них накапливаются взрывоопасные пероксиды:
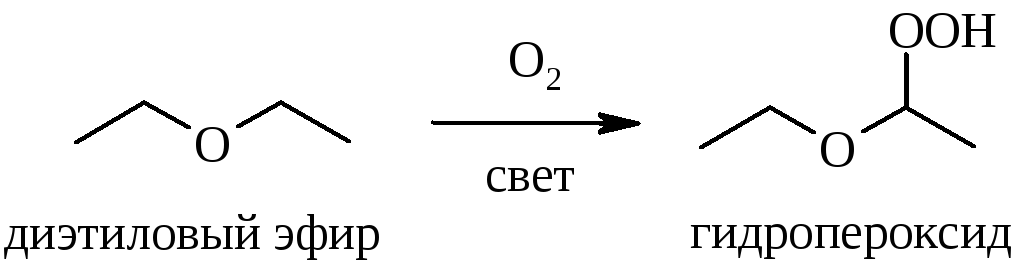
Поскольку в образующихся пероксидах (или гидропероксидах) есть связь O–O, они являются сильными окислителями и способны выделять йод из подкисленного раствора йодида калия:
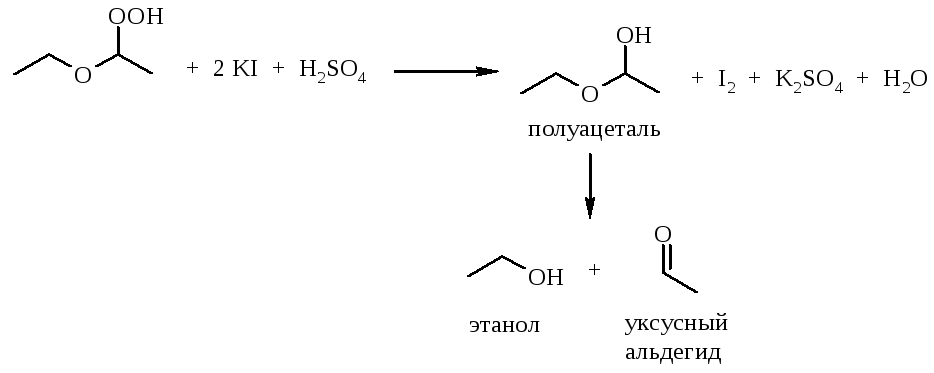
Выполнение работы
|
Реактивы |
Исследуемые вещества (1 в-во): |
|
иодид калия (10% р-р), серная кислота (10%),
|
диэтиловый эфир, диизопропиловый эфир. тетрагидрофуран, 1,4-диоксан |
В две пробирки наливают по 1 мл раствора иодида калия и добавляют по 2-3 капли разбавленной (10%) серной кислоты и по 1 мл свежеприготовленного крахмального клейстера. В одну из пробирок приливают 1 мл исследуемого эфира, смесь сильно встряхивают. Вторая пробирка служит эталоном (холостой опыт).
Через несколько минут сравнивают окраску содержимого двух пробирок. Положительным результатом теста на присутствие пероксида является появление синей окраски комплекса крахмала с йодом (окраска должна быть более интенсивной, чем в холостом опыте).
3. Реакции вицинальных гликолей (1,2-диолов)
3.1. Реакция комплексообразования виц-диолов
3.1.1. Взаимодействие виц-диолов с борной кислотой
Виц-диолы легко реагируют с борной кислотой с образованием хелатного комплекса. Легкость взаимодействия объясняют тем, что соседние гидроксильные группы диола как бы захватывают атом бора клешнями (что называют хелатированием, в хелатном комплексе атом бора четырехкоординирован, четвертая связь с атомом кислорода ОН-группы образована по донорно-акцепторному механизму и показана пунктиром):
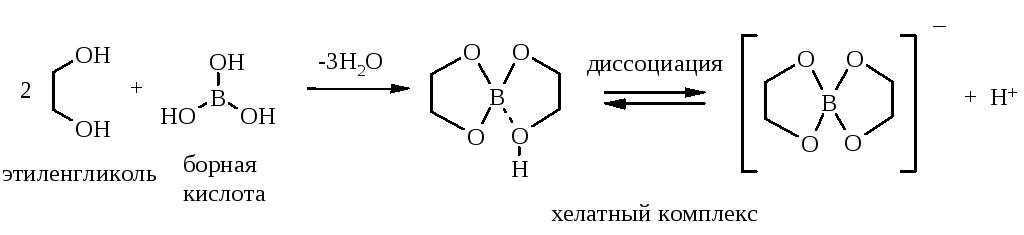
Борная кислота – сравнительно слабая кислота, а полученный хелатный комплекс проявляет значительно более выраженные кислотные свойства. Поэтому о протекании реакции комплексообразования можно судить по понижению pH раствора. Особенно отчетливо это заметно, когда вместо борной кислоты в реакции использовать ее соль – буру Na2B4O7: щелочная среда насыщенного раствора буры становится кислой в результате комплексообразования.
Одноатомные спирты, в отличие от гликолей, не способны образовывать хелатные комплексы с борной кислотой.
Выполнение работы
|
Реактивы |
Исследуемые вещества (1 в-во): |
Вещества для холостого опыта (1 в-во) |
|
бура (тв.), фенолфталеин (р-р) |
этиленгликоль (1,2-этандиол), глицерин (1,2,3-пропантриол), маннит (1,2,3,4,5,6-гексангексаол) |
этанол, пропанол-2. |
В пробирке встряхивают 0.5-1 г кристаллической буры с 10-12 мл воды. Дав осесть нерастворившейся соли, добавляют к полученному почти насыщенному раствору буры 1-2 капли фенолфталеина, при этом появляется малиновая окраска. Содержимое пробирки делят на две части (пробирки). В одну из них добавляют несколько капель или кристалликов виц-диола. В другую пробирку добавляют несколько капель одноатомного спирта (холостой опыт). При положительной реакции малиновая окраска индикатора исчезает.
