
- •Образец оформления работы по качественному функциональному анализу
- •1. Реакции непредельных соединений
- •1.1. Тест на растворимость
- •1.2. Реакции ненасыщенных соединений с бромом
- •1.3. Окисление ненасыщенных соединений перманганатом калия
- •1.4. Образование и свойства этилена
- •1.6. Тест на присутствие в ненасыщенном соединении гидропероксидов
- •2. Реакции спиртов
- •2.1. Взамодействие спиртов с натрием
- •2.2. Реакции окисления спиртов
- •Окисление спиртов хромовой кислотой
- •Окисление этанола перманганатом калия
- •2.3. Реакции спиртов с неорганическими кислотами
- •2.3.1. Взаимодействие спиртов с серной кислотой
- •2.3.2. Взаимодействие одноатомных спиртов с борной кислотой
- •Обнаружение пероксидов в простых эфирах
- •3. Реакции вицинальных гликолей (1,2-диолов)
- •3.1. Реакция комплексообразования виц-диолов
- •3.1.1. Взаимодействие виц-диолов с борной кислотой
- •3.1.2. Взаимодействие виц-диолов с гидроксидом меди(II)
- •4. Реакции фенолов
- •4.1. Тест на растворимость фенолов
- •4.2. Комплексообразование фенолов с хлоридом железа(III)
- •4.3. Реакция фенолов с бромом
- •4.4. Реакции окисления фенолов
- •4.4.1. Окисление перманганатом калия
- •4.4.2. Окисление хромовой кислотой
- •5. Реакции диазотирования ароматических аминов
- •5.1. Диазотирование анилина
- •5.2. Образование азокрасителей реакциями азосочетания
- •5.2.1. Азосочетание с аминами
- •5.2.2. Азосочетание с фенолами
- •5.2.3. Окраска ткани азокрасителями
- •6. Реакции карбонильных соединений
- •6.1. Реакции альдегидов и кетонов по карбонильной группе
- •6.1.1. Реакция с 2,4-динитрофенилгидразином
- •6.1.2. Реакция с бисульфитом натрия
- •6.1.3. Реакция с сульфитом натрия
- •6.1.4. Реакция альдегидов с фуксинсернистой кислотой (реакция Шиффа)
- •6.2. Реакции окисления альдегидов
- •6.2.1. Окисление альдегидов хромовой смесью
- •6.2.2. Окисление альдегидов реактивом Фелинга
- •6.3. Реакции енольных форм
- •6.3.1. Образование дибензальацетона
- •6.3.2. Иодоформная проба
- •6.3.3. Реакция устойчивых енольных форм с хлоридом железа(III)
- •7. Реакции окси- и аминокислот
- •7.1. РеакциИ оксикислот с хлоридом железа(III)
- •7.1.1. Реакции алифатических оксикислот с хлоридом железа(III)
- •7.1.2. Реакции оксибензойных кислот с хлоридом железа(III)
- •7.2. РеакциИ коМплексообразования с участием
- •7.2.1. Реакции α-аминокислот с хлоридом железа(III)
- •7.2.2. Реакции α-аминокислот с солями меди(II)
- •7.3. Реакция аминокислот с нингидрином (реакция Руэманна)
- •7.4. Реакция аминокислот с формальдегидом
- •8. Реакции углеводов
- •8.1. Общая реакция на углеводы с -нафтолом (реакция Молиша)
- •8.2. Реакция Селиванова на кетозы
- •8.3. Взаимодействие сахаров с солями двухвалентной меди в щелочном растворе
- •8.3.1. Доказательство наличия вицинальных гидроксильных групп
- •8.3.2. Окисление восстанавливающих сахаров соединениями двухвалентной меди (реакция Троммера)
- •8.4. Окисление моносахаридов йодом
2.2. Реакции окисления спиртов
Первичные и вторичные спирты окисляются такими реагентами, как хромовая кислота (дихромат калия + серная кислота), перманганат калия. При этом вначале получаются карбонильные соединения:
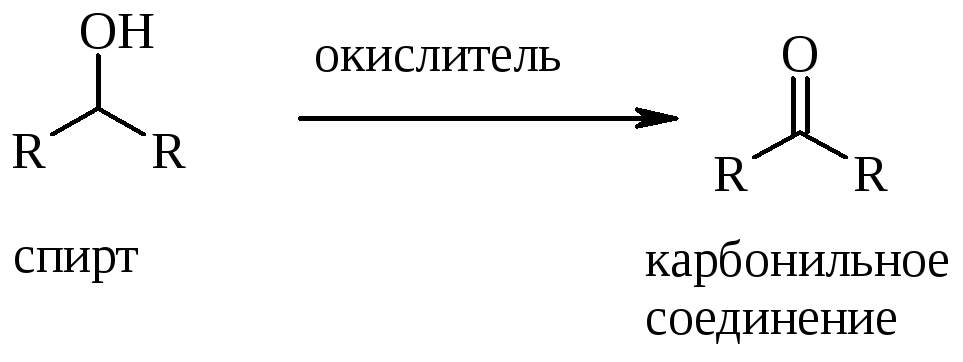
Первичные спирты в присутствии избытка окислителя превращаются далее в карбоновые кислоты. Например:
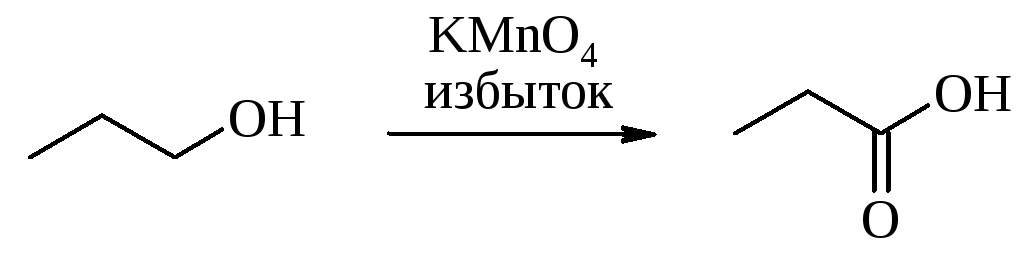
Аналогично ведут себя многоатомные спирты. Виц-диолы окисляются с расщеплением связи углерод-углерод, например:
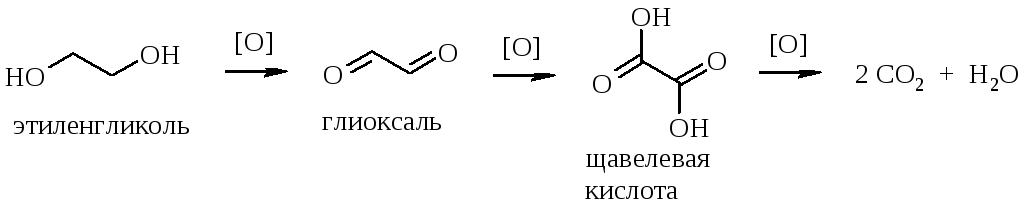
Ненасыщенные углеводороды, фенолы, альдегиды, анилин также окисляются перечисленными выше реагентами.
Насыщенные углеводороды, бензол и его гомологи (при комнатной температуре) устойчивы к действию этих окислителей.
-
Окисление спиртов хромовой кислотой
Выполнение работы
|
Реактивы |
Исследуемые вещества (1 в-во): |
Вещества для холостого опыта (1 в-во) |
|
бихромат калия (5% р-р), серная кислота (конц.) |
этанол, пропанол-2, бутанол-1, бутанол-2. |
октан циклогексан, бензол, толуол |
В двух пробирках готовят хромовую кислоту: к 2-5 каплям 5% раствора бихромата калия осторожно добавляют 2 капли концентрированной серной кислоты. Добавляют в одну пробирку 5 капель исследуемого спирта, а в другую – вещество для холостого опыта, встряхивая после добавления каждой капли. В пробирке со спиртом наблюдается переход оранжевой окраски в голубовато-зеленую (положительная проба). В случае отрицательного теста (в холостом опыте) раствор останется оранжевым.
-
Окисление этанола перманганатом калия
Выполнение работы
|
Реактивы |
Исследуемые вещества (1 в-во): |
|
серная кислота (конц.), перманганат калия (тв.) |
этанол |
В сухую пробирку, закрепленную в штативе, аккуратно пипеткой, не смачивая стенок, вносят 2-3 мл концентрированной серной кислоты. По стенке пробирки другой пипеткой приливают 2-3 мл этанола таким образом, чтобы получилось два слоя. Затем насыпают несколько кристалликов перманганата калия, который будет размещаться на границе раздела двух слоев. Через 1-2 мин начинает протекать реакция, сопровождающаяся появлением ярких вспышек. При этом чувствуется запах уксусного альдегида. Внимание! До полного окончания реакции нельзя выливать смесь из пробирки!
2.3. Реакции спиртов с неорганическими кислотами
2.3.1. Взаимодействие спиртов с серной кислотой
Спирты растворяются в серной кислоте. Растворение обусловлено протеканием реакции образования алкилсульфатов:
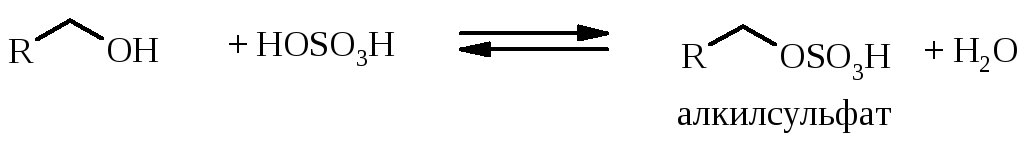
Эта реакция обратима: водой алкилсульфаты постепенно гидролизуются, и гидролиз ускоряется при нагревании. Спирт, взятый в избытке, реагирует с алкилсульфатом (по механизму нуклеофильного замещения) с образованием простого эфира:
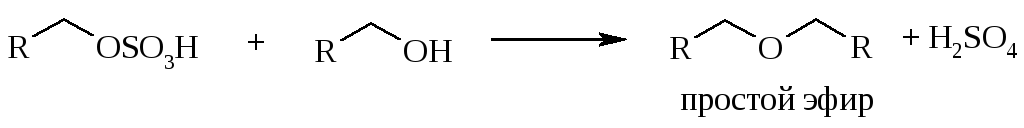
Алкены также реагируют с концентрированной серной кислотой с образованием алкилсульфатов. Насыщенные углеводороды устойчивы к действию этого реагента. Ароматические углеводороды (в особенности полиалкилзамещенные и фенолы) могут сульфироваться.
Выполнение работы
|
Реактивы |
Исследуемые вещества (1 в-во): |
|
серная кислота (конц.), |
3-метилбутанол-1 (изоамиловый спирт) |
В пробирку помещают 4 мл холодной концентрированной серной кислоты и осторожно небольшими порциями добавляют 2 мл изоамилового спирта. Смесь необходимо часто встряхивать и охлаждать ледяной водой. По окончании введения спирта полученную однородную, почти без запаха, жидкость оставляют стоять в течение 3-5 мин, после чего делят ее на две части.
Одну половину раствора осторожно, небольшими порциями выливают в другую пробирку с 5-7 мл холодной воды, взбалтывая и хорошо охлаждая. Образуется прозрачный раствор без запаха, в то время как исходный спирт мало растворим в воде и имеет характерный запах.
Другую половину раствора нагревают почти до кипения 2-3 мин. При этом жидкость сильно буреет, выделяются мелкие пузырьки газа с характерным запахом сернистого ангидрида. Охладив жидкость, осторожно выливают ее в пробирку с водой. В этом случае отделяется нерастворимый в воде слой диизоамилового эфира.
