
- •Образец оформления работы по качественному функциональному анализу
- •1. Реакции непредельных соединений
- •1.1. Тест на растворимость
- •1.2. Реакции ненасыщенных соединений с бромом
- •1.3. Окисление ненасыщенных соединений перманганатом калия
- •1.4. Образование и свойства этилена
- •1.6. Тест на присутствие в ненасыщенном соединении гидропероксидов
- •2. Реакции спиртов
- •2.1. Взамодействие спиртов с натрием
- •2.2. Реакции окисления спиртов
- •Окисление спиртов хромовой кислотой
- •Окисление этанола перманганатом калия
- •2.3. Реакции спиртов с неорганическими кислотами
- •2.3.1. Взаимодействие спиртов с серной кислотой
- •2.3.2. Взаимодействие одноатомных спиртов с борной кислотой
- •Обнаружение пероксидов в простых эфирах
- •3. Реакции вицинальных гликолей (1,2-диолов)
- •3.1. Реакция комплексообразования виц-диолов
- •3.1.1. Взаимодействие виц-диолов с борной кислотой
- •3.1.2. Взаимодействие виц-диолов с гидроксидом меди(II)
- •4. Реакции фенолов
- •4.1. Тест на растворимость фенолов
- •4.2. Комплексообразование фенолов с хлоридом железа(III)
- •4.3. Реакция фенолов с бромом
- •4.4. Реакции окисления фенолов
- •4.4.1. Окисление перманганатом калия
- •4.4.2. Окисление хромовой кислотой
- •5. Реакции диазотирования ароматических аминов
- •5.1. Диазотирование анилина
- •5.2. Образование азокрасителей реакциями азосочетания
- •5.2.1. Азосочетание с аминами
- •5.2.2. Азосочетание с фенолами
- •5.2.3. Окраска ткани азокрасителями
- •6. Реакции карбонильных соединений
- •6.1. Реакции альдегидов и кетонов по карбонильной группе
- •6.1.1. Реакция с 2,4-динитрофенилгидразином
- •6.1.2. Реакция с бисульфитом натрия
- •6.1.3. Реакция с сульфитом натрия
- •6.1.4. Реакция альдегидов с фуксинсернистой кислотой (реакция Шиффа)
- •6.2. Реакции окисления альдегидов
- •6.2.1. Окисление альдегидов хромовой смесью
- •6.2.2. Окисление альдегидов реактивом Фелинга
- •6.3. Реакции енольных форм
- •6.3.1. Образование дибензальацетона
- •6.3.2. Иодоформная проба
- •6.3.3. Реакция устойчивых енольных форм с хлоридом железа(III)
- •7. Реакции окси- и аминокислот
- •7.1. РеакциИ оксикислот с хлоридом железа(III)
- •7.1.1. Реакции алифатических оксикислот с хлоридом железа(III)
- •7.1.2. Реакции оксибензойных кислот с хлоридом железа(III)
- •7.2. РеакциИ коМплексообразования с участием
- •7.2.1. Реакции α-аминокислот с хлоридом железа(III)
- •7.2.2. Реакции α-аминокислот с солями меди(II)
- •7.3. Реакция аминокислот с нингидрином (реакция Руэманна)
- •7.4. Реакция аминокислот с формальдегидом
- •8. Реакции углеводов
- •8.1. Общая реакция на углеводы с -нафтолом (реакция Молиша)
- •8.2. Реакция Селиванова на кетозы
- •8.3. Взаимодействие сахаров с солями двухвалентной меди в щелочном растворе
- •8.3.1. Доказательство наличия вицинальных гидроксильных групп
- •8.3.2. Окисление восстанавливающих сахаров соединениями двухвалентной меди (реакция Троммера)
- •8.4. Окисление моносахаридов йодом
6.3. Реакции енольных форм
6.3.1. Образование дибензальацетона
Наиболее характерной реакцией енольных форм является альдольно-кротоновая конденсация. Так, при смешении ацетона и бензальдегида в мольном соотношении 1 : 2 в присутствии основания протекает следующая реакция:
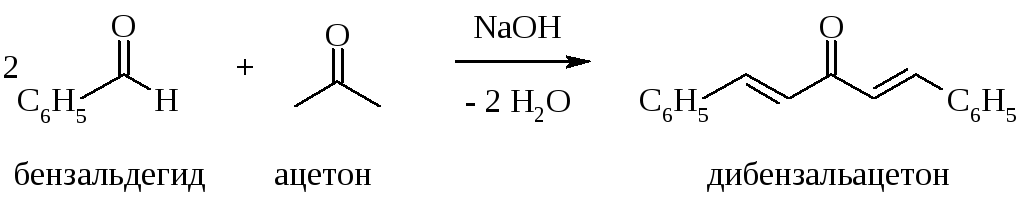
Выполнение работы
|
Реактивы |
Исследуемые вещества |
|
гидроксид натрия (10%- р-р), спирт |
ацетон, бензальдегид |
В широкую пробирку помещают 7.5 мл 10%-го водного раствора гидроксида натрия и 6 мл спирта. При непрерывном встряхивании пробирки прибавляют смесь 0.8 мл бензальдегида и 0.3 мл ацетона. Через некоторое время смесь начинает мутнеть за счет образования желтого хлопьевидного осадка дибензальацетона.
6.3.2. Иодоформная проба
При действии иода в щелочной среде на метилкетоны происходит исчерпывающее иодирование, и трииодметилкетоны расщепляются с выделением иодоформа.
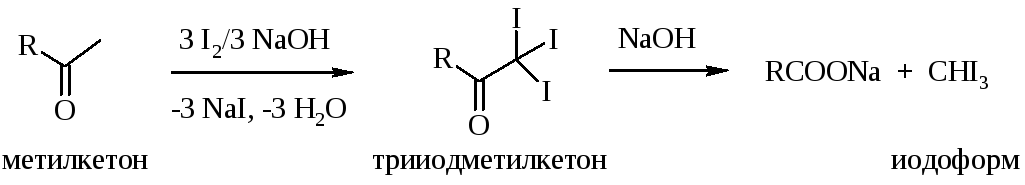
Эту реакцию дают не только метилкетоны, но и спирты, способные при окислении образовывать ацетильную группу СН3СО:
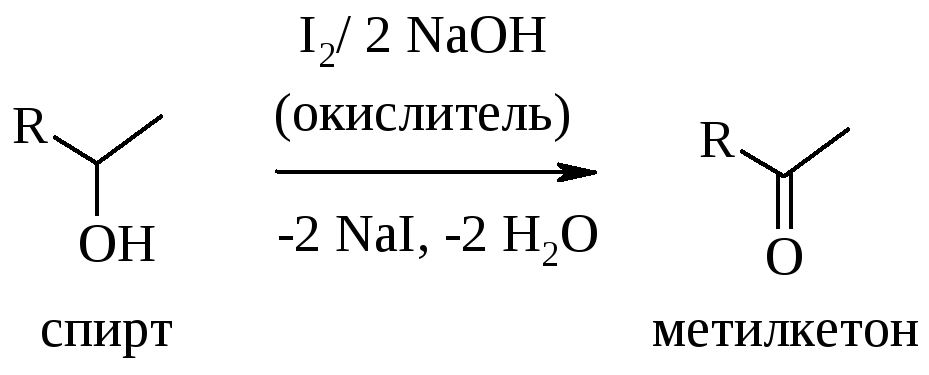
Выполнение работы
|
Реактивы |
Исследуемые вещества (2 в-ва): |
Вещества для холостого опыта (1 в-во) |
|
иод (р-р в иодиде калия), NaOH (10% р-р). |
а) ацетон, ацетофенон; б) бутанол-2, пропанол-2. |
циклогексанон. |
В три пробирки наливают по 1 мл воды и добавляют по капле исследуемых веществ: в первую пробирку ацетон или ацетофенон, во вторую – бутанол-2 или пропанол-2 и в третью – циклогексанон, затем по 2 капли концентрированного раствора иода в иодиде калия и по каплям – 10% раствор NaOН, при постоянном встряхивании. При этом окраска иода исчезает, и в первых двух пробирках одновременно выделяется обильный осадок иодоформа (образование осадка на холоде характерно для ацетона, для других соединений требуется выдержка или нагревание).
В третьей пробирке осадок не образуется (холостой опыт).
6.3.3. Реакция устойчивых енольных форм с хлоридом железа(III)
1,3-Дикарбонильные соединения образуют устойчивые енольные формы, которые можно обнаружить реакцией с хлоридом железа(III), поскольку енолы образуют с ионами железа(III) окрашенные хелатные комплексы:
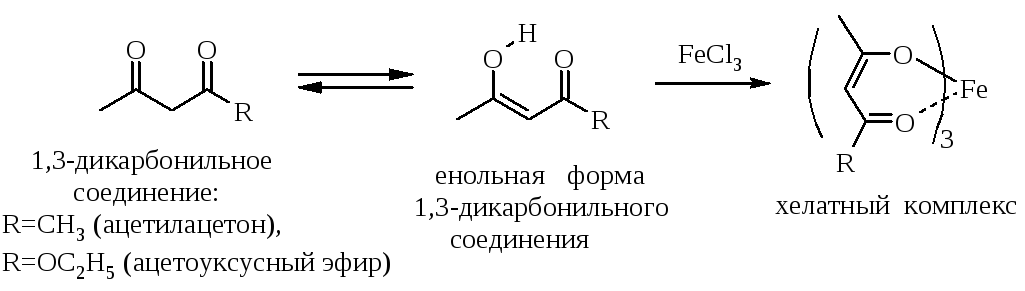
Лучше использовать спиртовые, а не в водные растворы реагентов.
Эту же реакцию дают и фенолы.
Выполнение работы
|
Реактивы |
Исследуемые вещества (1 в-во): |
Вещества для холостого опыта (1 в-во) |
|
хлорид железа(III) (3% р-р в метаноле),
|
ацетилацетон (2,4-пентандион), ацетоуксусный эфир (этил-3-оксобутаноат) |
ацетон, ацетофенон, циклогексанон. |
В двух пробирках растворяют по капле исследуемых веществ (в одной 1,3-дикарбонильное соединение, в другой – кетон), в 1 мл метанола, и добавляют по три капли 3% метанольного раствора хлорида железа(III). Появляющаяся желто-красная (реже сине-зеленая) окраска говорит о наличии устойчивой енольной группировки.
