
- •Неметаллы
- •6. Физические свойства и строение неметаллов
- •7. Получение неметаллов
- •8. Химические свойства неметаллов.
- •9. Соединения неметаллов с водородом
- •10. Соединения неметаллов с кислородом
- •Строение и физические свойства оксидов
- •Получение и химические свойства оксидов
- •11. Кислородные кислоты и их соли
- •Соли кислородных кислот
- •Галогены. Общая характеристика
- •2. Галогены в природе. Получение галогенов.
- •Взаимодействие галогенов с водой.
- •11.1. Оксокислоты hxo и их соли.
- •11.2. Оксокислоты hxo2
- •11.3. Свойства кислот hxo3 и их солей.
- •11.4. Оксокислоты hxo4.
- •Материалы на основе галогенов и их соединений.
- •Фтор и его соединения
- •Физические свойства
- •Хлор и его соединения
- •Соединения хлора Хлористый водород
- •Химические свойства
- •Кислородсодержащие кислоты хлора
- •Бром и его соединения
- •Химические свойства
- •Бромистый водород hBr
- •Иод и его соединения
- •Химические свойства
- •Иодистый водород
- •Кислородные кислоты йода
-
8. Химические свойства неметаллов.
Поскольку у неметаллов высокая электроотрицательность, их простые вещества могут выступать окислителями.
При этом восстановителями могут быть –
а) металлы: O20 + Mg → MgO–2 (оксид магния),
N20 + Li → Li3N–3 (нитрид лития),
S0 + Zn → ZnS–2 (сульфид цинка);
б) менее активные неметаллы: O20 + C→ CO2–2,
O20 + P → P2O5–2,
O20 + S → SO2–2,
в) сложные вещества: O20 + C2H5OH → CO2–2 + H2O–2,
Br20 + Ni(OH) 2 + KOH → KBr–1 + Ni2O3⋅xH2O.
Степень окисления, в которую при этом переходит неметалл-окислитель, легко определить по правилу n–8, где n – номер группы.
Неметаллы бывают восстановителями только в реакциях с более активными неметаллами:
H20 + N2 NH3+1,
S0 + F2 → S+6F6,
а также с сильными окислителями:
P0 + KClO3 (при ударе) → P2+5O5 + KCl,
S0 + KNO3 (при нагревании) → KNO2 + S+4O2.
Углерод при высоких температурах способен восстанавливать даже некоторые оксиды металлов, например, кокс – железную руду:
3С0 + Fe2O3 = 3C+2O + Fe.
Эта реакция возможна за счёт образования газообразного продукта CO.
При взаимодействии с водой ряда наиболее активных неметаллов происходит их диспропорционирование:
Cl20 + H2O HCl–1 + HOCl+1,
I20 + H2O HI–1 + HIO3+5.
Однако эти реакции идут в незначительной степени и равновесия сильно смещены влево.
Поскольку в реакциях образуются кислоты, можно добиться смещения равновесия введением щёлочи:
Cl20 + 2NaOH = NaCl–1 + NaOCl+1 + H2O.
При нагревании раствора устойчивее более высокие степени окисления галогенов:
Cl20 + KOH (раствор, нагревание) → KCl–1 + KClO3+5 (бертолетова соль).
По такой же схеме (с диспропорционированием) при нагревании в щелочах растворяются и некоторые менее активные неметаллы:
3S0 + 3NaOH = 2Na2S–2+ Na2S+4O3,
2P0 + 2NaOH + H2O = P–3H3+ Na2[P+3O3H].
Неметаллы с минимальной электроотрицательностью растворяются в щелочах с выделением водорода:
Si0 + 2NaOH + 2H+12O = Na2[H2Si+4O4] + 2H02↑.
Углерод реагирует с водяным паром только выше 900 °С:
C0 + H+12O = C+2O + H02.
Во фторе вода горит с выделением кислорода:
F20 + H2O–2 = HF–1 + O02.
-
9. Соединения неметаллов с водородом
Из-за высокой прочности молекул водорода при комнатной температуре с ним реагирует только фтор (со взрывом):
H2 + F2 → 2HF (фтороводород).
При нагревании взрывают также смеси H2 с Cl2 и с O2:
2H2 + O2 (гремучая смесь) → 2H2O.
Активно идёт взаимодействие с Br2 и H2. В остальных случаях реакция идёт с трудом или вообще не идёт. Тем не менее, для связывания атмосферного азота в аммиак применяют следующий процесс:
N2 + 3H2 2NH3.
Его обычно проводят при 500 °С и 300 атм, используют катализатор (губчатое железо с активирующими добавками). При этих условиях равновесие смещено влево, но аммиак легко извлечь из смеси, пропустив её через воду.
Часто прямая реакция неметалла с водородом вообще невозможна, а соединение получают косвенным путём:
Mg2Si + HCl = MgCl2 + SiH4↑.
Все соединения неметаллов с водородом состоят из молекул.
Простейшие молекулы содержат один центральный атом и число атомов водорода, определяемое правилом 8–n (n – номер группы Периодической системы):
HCl, H2S, PH3.
У бора такой простой формы нет.
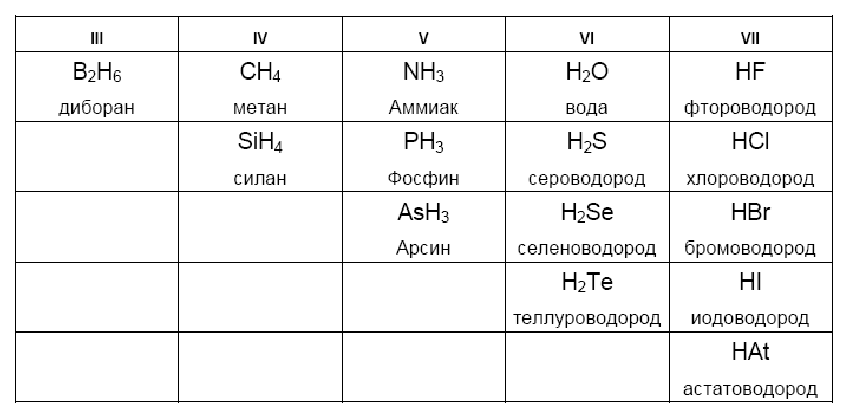
Есть и более сложные формы: B4H10 – тетраборан, N2H4 – гидразин, Si2H6 – дисилан, многочисленные углеводороды, например, октан C8H18, бензол C6H6 и другие.
Связь водорода с центральным атомом: ковалентная полярная, общая электронная пара смещается к более электроотрицательному атому:
H :F.
Обычно водород слабее удерживает свой электрон и приобретает положительный заряд. И лишь в силанах и боранах – наоборот.
Часть водородных соединений при растворении в воде даёт кислоты.
-
Формула
Название
Сила кислоты
Kонстанта диссоциации
Соли
HF
плавиковая
средней силы
6,6⋅10–4
фториды
HCl
соляная
сильная
1⋅10+7
хлориды
H2S
сероводородная
слабая
6⋅10–8
сульфиды
H2Te
теллуроводородная
средней силы
1⋅10–3
теллуриды
В подгруппе сверху вниз сила этих кислот увеличивается, из галогеноводородных слабее всех – плавиковая, сильнее всех – иодоводородная. Причина состоит в увеличении длины и снижении прочности связи H–Э.
При взаимодействии кислотных водородных соединений со щелочами получаются соли:
H2S + 2NaOH → Na2S + 2H2O.
Наоборот, действием сильной или нелетучей кислоты на такую соль можно получить водородное соединение:
ZnS + 2HCl → ZnCl2 + H2S ↑,
KCl (сухой) + H3PO4(конц.) (нагревание) → KH2PO4 + HCI↑,
Из водородных соединений основную природу имеет только аммиак. В его растворе устанавливаются равновесия:
NH3 + H2O NH3⋅H2O NH4+ + OH–.
При взаимодействии аммиака с кислотами получаются соли, содержащие ион NH4+ (ион аммония):
NH3 + HCl (в растворе) → NH4Cl.
Ион NH4+ имеет форму правильного тетраэдра, как и молекула метана CH4, все связи N–H в нём равноценны. Образование четвёртой ковалентной связи можно объяснить донорно-акцепторным механизмом: один из атомов (в данном случае, азот) предоставляет целую электронную пару (является донором), другой (ион водорода H+) имеет выгодную по энергии свободную орбиталь (является акцептором).
Аммиак – слабое основание, поэтому может вытесняться из солей более сильными:
2NH4Cl + Ca(OH)2 (нагревание) → 2NH3↑ + CaCl2 + 2H2O.
Соли аммония разлагаются при нагревании –
А) по обменному механизму:
NH4Cl → NH3 + HCl,
Б) с редокс-реакцией, если анион может быть окислителем:
(N–3H4) 2Cr+62O7 → N02 + Cr+32O3 + 4H2O.
Водородные соединения ряда неметаллов в обычных условиях практически не проявляют ни кислотных, ни основных свойств (фосфин, углеводороды, силаны, бораны).
Все водородные соединения неметаллов, кроме галогеноводородов, сгорают в кислороде:
CH4 + 2O2 → CO2 + 2H2O,
2H2S + 3O2 → 2SO2 + 2H2O,
4NH3 + 5O2 → 4NO + 6H2O.
