
- •Майкл а. Гриппи патофизиология легких
- •Предисловие к изданию на русском языке
- •Часть I
- •Глава 1
- •Майкл а. Гриппи
- •Глава 2 Механика дыхания
- •Закладка
- •I лава с.. Тслагтиа «цылапуш
- •Глава 3. Распределение вентиляции
- •Глава 4. Физиологические основы тестирования функЦий лэтКих
- •Глава 5
- •Глава V
- •Глава 7
- •Глава 8
- •Часть II
- •14 800/Мм3', полиморфноядерные - 71 %, палочкоядерные - 6 %, лимфоциты -
- •Часть III
- •Глава 12
- •Глава 13
- •V/q отношения в нормальном легком
- •Глава 15
- •Часть IV
- •Глава 17
- •Глава 7 9
- •308______Приложение 1. Символы и понятия, общепринятые в физиологии дыхания
- •Глава 10;
- •Часть I Структурно-функциональные связи легких,
- •Глава 1. Структура воздухоносных путей и паренхимы легких
- •Глава 2. Механика дыхания (Майкл а. Гриппы)..............................................................
- •Глава 3. Распределение вентиляции (Майкл а. Гриппы).....,.........................................
- •Глава 4. Физиологические основы тестирования
- •Глава 5. Механизм бронхоконстрикции и бронхиальная астма
- •Глава 6. Хроническая обструктивная болезнь легких
- •Глава 7. Иммунология легких и интерстициальные
- •Глава 8. Клинические примеры: механика дыхания, обструктивные
- •Глава 9. Обмен газов в легких (Майкл а. Гриппи)......................................................139
- •Глава 10. Транспорт газов к периферическим тканям
- •Глава 11. Клинические примеры: обмен газов и их транспорт
- •Часть III. Легочное кровообращение и его отношение
- •Глава 12. Легочное кровообращение (Гарольд и. Належки)....................................179
- •Глава 13.Вентиляционно-перфузионные отношения (Пол н. Ланкен)...............195
- •Глава 14. Кардиогенный и некардиогенный отек легких
- •Глава 15. Клинические примеры: легочное кровообращение
- •Часть IV. Интегрированные дыхательные функции:
- •Глава 16. Гуморальная и нервная регуляция дыхания (Скотт Менакер)...............237
- •Глава 17. Регуляция дыхания во время сна (Ричард Шваб)........................................251
- •Глава 18. Патофизиология дыхательной недостаточности (Пол я. Ланкен)..........265
- •Глава 19. Физиология мышечной деятельности
- •Глава 20. Клинические примеры: нарушения регуляции дыхания и дыхательная недостаточность (Майкл л. Гриппы) .........................................297
- •194021, Ул. Политехническая, д. 26 телефакс (812) 247-9301
- •109202, Перовское шоссе, д. 10 телефакс (095) 170-6674 e-mail: poznkn@orc.Ru
- •703475, Москва, ул. Краснопролетарская, д. 16
Глава 3. Распределение вентиляции


Рис. 3-10. Моде.in неравномерной иептиля-ции легких (А) Чаг-тичiк\я обе гру кцмя ВII в одной легочной единице- (Б) Нарушенная ,)лаети11мосгъ н одной легочной единице. (В) Локализованная дина-м и ч ее к ая ко м 11 po(: cf и я ВП » одной легочной один и не. (Г) Ограниченное растяжение одной единицы во время наполнения легкого. В каждой модели нормальная единица получает большую часть общего вдыхаемого объема. ( П о: F о г s -ter R. E. II, Dubois А. В., Briscoe W. A, Fisher А В. Pulmonary ventilation. In: The Lung: Physiologic Basis of Pulmonary Function Tests. 3rd ed. Chicago: Year Book Medical Pudlishers, 1986; 61.)
В ранней фазе выдоха выводится воздух из верхних дыхательных путей. Поскольку эта область содержит чистый кислород, заполнивший ее после предшествующего вдоха, то содержание там азота равно нулю (фаза I). Далее азотсодержащий газ анатомического мертвого пространства вымывается по мере опорожнения альвеол: концентрация азота резко возрастает (фаза II). Вслед за этим выдыхается альвеолярный газ. У здоровых людей с минимальной неоднородностью вентиляции эта фаза кривой (фаза III) плоская, и она известна как альвеолярное плато.
У пациентов с разнообразными болезнями паренхимы и BII фаза III не плоская. 11аклон фазы III (% концентрации N^/л выдыхаемого объема) фактически является мерой неоднородности вентиляции. Очевидно, что плохо вентилируемые зоны легких получают мало вдыхаемого кислорода. Соответственно эти регионы имеют высокую альвеолярную концентрацию азота по сравнению с нормально вентилируемыми областями, т. е. наблюдается меньшее разведение азота вдыхаемым кислородом. Плохо вентилируемые области опустошаются в последнюю очередь, что и обеспечивает повышение концентрации азота в течение фазы III.
На рис. 3-11 можно видеть еще один заметный подъем концентрации азота после альвеолярного плато (фаза IV). Предполагаемым механизмом, лежащим в основе фазы IV, является закрытие мелких ВП, расположенных у основания легких, при низких легочных объемах.
В период начальной фазы вдоха чистого кислорода мелкие ВП (дыхательные бронхиолы), расположенные в базальных зонах, могут быть сдавлены собственным весом легких вплоть до их закрытия. Как следствие, эти зоны получают малую долю кислорода, попадающего в легкие и начале вдоха. Тем временем вдох до уровня
Рис. 3-9. Измерении региональной легочной вентиляции с помощью ингаляции радиоактивного ксенона. Испытуемый вдыхает определенный объем воздуха, содержащего ксенон-133. Счетная камера сканирует верхние, средние и нижние легочные зоны для количественной оценки региональной вентиляции. Каждое региональное измерение делится па объем легкого ("нормализуется"). Поскольку легкие имеют больший объем у оснований
(где находится больше альвеол), предполагается, что туда поступит больше ксенона. Однако даже с учетом апикалыю-базалыюй разницы в объеме легких вентиляция базальных отделов больше. (Mo: West J. В. Ventilation. In: Respiratory Physiology: The Essentials. 4th eel. Baltimore: Williams & Wilkins, 1990: 19.)
легких это явление, как правило, выражено неравномерно. Рис. 3-10 А представляет две идеальные легочные единицы, одна из которых вентилируется через ВП с нормальным сопротивлением, а другая — с увеличенным.. При каждом вдохе большая часть вдыхаемого объема распределяется в единице без обструкции. Общая эффективность газообмена будет зависеть от степени перераспределения кровотока от единицы с обструкцией к нормально вентилируемой.
На рис. 3-1 ОБ видно, как локализованные изменения эластичности легких (обратная величина растяжимости, как описано в гл. 2) создают неравномерное распределение вентиляции. Такого рода нарушения характерны для эмфиземы (эластичность снижена) и легочного фиброза (эластичность повышена). В ходе повторяющихся дыхательных циклов легочные единицы с увеличенной эластичностью получают большую часть вдыхаемого объема. При некоторых болезнях, например эмфиземе, может преобладать сочетание регионально измененных растяжимости и сопротивления ВП (рис. 3-1 ОБ). Возникая на выдохе, такое увеличение сопротивления ВП является "динамическим" (гл. 2, рис. 2-20). В результате наблюдается заметная неравномерность вентиляции: преобладающая часть вдыхаемого газа идет к областям без обструкции с нормальной растяжимостью.
Наконец, при некоторых заболеваниях сопротивление ВП и эластичность легких могут быть нормальными, а нарушение распределения вентиляции происходит из-за региональных ограничений расправления легких (рис. 3-1ОГ). Клинические примеры включают компрессию легкого плевральным выпотом и ограничение расширения половины грудной клетки при одностороннем параличе диафрагмы.
Тесты на неравномерную вентиляцию легких
Хотя для оценки неравномерности вентиляции используется ряд тестов, здесь описывается только один — тест на вымывание азота при одиночном вдохе кислорода. Другой метод, основанный на определении частотно-зависимой растяжимости, описан в гл. 2. Региональное распределение вентиляции исследуется также при вдыхании радиоактивных газов, например ксенона.
Во время теста на вымывание азота человек делает максимальный вдох чистого кислорода после опорожнения легких до уровня остаточного объема. Таким образом, он делает вдох кислорода, равный по объему жизненной емкости легких. Затем испытуемый делает медленный выдох, объем которого измеряется спирометром, до уровня остаточного объема. Концентрация азота в выдыхаемом воздухе непрерывно регистрируется на протяжении выдоха с помощью азотографа. Рис. 3-11 показывает
ifPTKinP ГмЯ'ЗТ-Л Т Я If НЯ^КГП^Г^\ЛГ»М "wm/mrni пкткллиаима а'э/лта" п/л пхгтглиигл™ тп-тлж* /-«п/••»/-•/-х_
Рис. 3-11. Кривая иымывания а.юта при одиночном вдохе ()2, демонстрирующая четыре фазы. TLC общая емкость легких; CV - объем закрытия; RV - остаточный объем

дение, как указывалось в разделе "Региональное распределение дыхательного объема", подчиняется крутой части кривой давление-объем). Следовательно, эндогенный альвеолярный азот в базальных областях легких подвергнется разведению в большей степени, чем в апикальных зонах. Во время выдоха и те, и другие зоны опорожняются, создавая фазу III кривой. Когда по мере завершения выдоха происходит закрытие мелких ВП базальных отделов, из богатых азотом апикальных легочных зон поступает пропорционально больше газа, создавая фазу IV.
Объем легких, представляющий часть жизненной емкости и остающийся не выдохнутым к началу фазы IV кривой вымывания азота, известен как объем закрытия. Сумма объема закрытия и остаточного объема называется емкостью закрытия. У здоровых молодых людей закрытие ВП происходит на уровне 10 % жизненной емкости, считая от остаточного объема, а после 60 лет — на уровне 40 %. У пациентов даже с малыми степенями обструкции ВП можно обнаружить значительное повышение объема закрытия.
Избранная литература
Forster R. Е. II., Dubois А. В., Briscoe W. A., Fisher А. В. Pulmonary ventilation. In: The Lung: Physiologic Basis of Pulmonary Function Tests. 3rd ed. Chicago: Year Book, Medical Publishers, 1986:25-64.
Hlastala M. Ventilation. In: Crystal R. G., West J. В., eds. The Lung: Scientific Foundations. New York: Raven Press, 1991:1209-1214.
Murray J. F. Ventilation. In: Murray J. F., ed. The Normal Lung. 2nd ed. Philadelphia: W. B. Saunders, 1986:77-113.
West J. B. Ventilation. In: Respiratory Physiology: The Essentials. 4th ed. Baltimore: Williams & Wilkins, 1990:11 -20.
Физиологические основы тестирования функции легких
Марк А. Келли
Общие понятия, представленные в предыдущих главах, составляют основу тестов, используемых для количественной оценки функции легких. Функциональное исследование легких является важной частью клинической медицины и выполняет ряд задач: (1) диагностика заболевания легких и оценка его тяжести; (2) оценка эффективности терапии различных легочных расстройств (например, реакции больных бронхиальной астмой на бронходилататоры); (3) представление о течении бо лезни из результатов последовательных тестов; и (4) обучение больных приемам правильного дыхания и убеждение их в необходимости ведения здорового образа жизни (например, убедить курильщика прекратить курение, показав ему результаты теста, свидетельствующие о нарушении функции легких).
В данной главе рассмотрены физиологические основы и методы тестирования функции легких. Выделены тесты, используемые для оценки различий между наиболее распространенными легочными расстройствами. Другие, менее употребимые тесты рассмотрены для иллюстрации некоторых физиологических принципов. Наконец, представлено несколько клинических случаев, показывающих, как с помощью функциональных тестов могут быть решены диагностические проблемы.
Основы тестирования функции легких
Дыхательная система приспосабливает обмен газов к широкому спектру разнообразных обстоятельств — от состояния покоя до тяжелой физической нагрузки. В условиях последней, когда требуется повышение потребления О2 и выделения (Х)2, необходима большая эффективность газообмена и вентиляции.
Как было изложено в главах 1-3, структура легких обеспечивает максимальную эффективность вентиляции. Функционально дыхательная система может быть разделена на три компонента: (1) воздухоносные пути (ВП), (2) легочная паренхима и (3) грудная клетка, выполняющая функцию мехов.
ВП представлены пол у ригидными трахеей и долевыми бронхами и более податливыми, мелкими бронхиолами, простирающимися до периферии легких. Тип воздушного потока варьирует от турбулентного в центральных ВП до ламинарного в мелких (гл. 2). Мелкие дыхательные пути могут быть сдавлены во время форсированного выдоха. В результате, экспираторный воздушный поток ограничивается как в норме, так и при патологии легких. Это имеет важное значение для функционального исследования легких, поскольку -диализэкспираторной части вентиляции по-
Второй функциональный компонент — эластическая паренхима легких — ведет себя подобно резиновому баллону (гл. 2). Для его наполнения требуется энергия; при прекращении энергетических затрат, поддерживающих баллон в расправленном состоянии, он спадается. Нарушения, делающие легкие жесткими (например, легочный фиброз), препятствуют их полному спадению, в то время как нарушения эластичности легких (например, при эмфиземе) уменьшают силу, с которой они опорожняются.
Третий функциональный компонент — "грудные мехи" — состоит из грудной клетки, межреберных мышц и диафрагмы (гл. 1). Поскольку сами легкие не способны инициировать дыхание, грудная клетка и дыхательная мускулатура должны создавать силы, необходимые для вентиляции. Дыхательные мышцы активны при вдохе; мышцы выдоха обычно работают только при определенных патологических состояниях и при физической нагрузке. Деформация грудной клетки и болезни дыхательных мышц могут влиять на функцию дыхательной "помпы", приводя к дыхательной недостаточности (гл. 18).
Изменения любого из этих трех функциональных компонентов могут стать причиной одышки и измеримых отклонений функции легких. Функциональное исследование легких используется для оценки состояния каждого из этих трех компонентов.
Основные группы клинически важных тестов легочной функции включают спирометрию, тесты на силу дыхательных мышц, измерение легочных объемов и диффузионной способности легких. Диффузионная способность легких обсуждается в главе 9.
Спирометрия
Спирометрия — наиболее важный способ оценки легочной функции. При проведении спирометрии пациент вдыхает и выдыхает с максимальной силой. Измеряются объемная скорость воздушного потока и изменения объема дыхательной системы. Наиболее клинически значимые сведения дает анализ экспираторного маневра (выдоха).
Спирометр с водяным затвором
В течение десятилетий применялись спирометры простой системы, измерявшие объем легких с использованием закрытого контура (рис. 4-1). Пациент в положении сидя дышит в камеру, которая представляет собой подвижный цилиндр, погруженный в емкость с водой. Изменения объема легких регистрируются по изменению объема цилиндра, соединенного с откалиброванным вращающимся барабаном. В примере, представленном на рис. 4-1, вдох регистрируется отклонением записи на барабане кверху, а выдох — книзу.
Основным показателем спирометрии является жизненная емкость легких (ЖЕЛ; VC), представляющая собой максимальный объем воздуха, который можно вдохнуть (инспираторная VC) или выдохнуть (экспираторная VC). Чтобы измерить VC, пациент делает сначала вдох до предельного объема легких, а затем возможно полный выдох.
Некоторое количество воздуха остается в легких даже после максимального экспираторного маневра. Этот объем называют остаточным объемом (ОО; RV). Сумма жизненной емкости и остаточного объема дает общую емкость легких (ОЕЛ; TLC). Остаточный объем нельзя определить с помощью одной спирометрии; это -rtW^roT ттгл1тпгтитлтрт1кныу игшепений объема легких (см. раздел "Измерение легоч-

63
Рис. 4-1. Обычный ноля пой спирометр. 11а-полпенпый ноадухом цилиндр, погруженный в сосуд с водой,соединен с вращающимся барабаном, на котором лаписы-ваютея показания спирометра. Ьарабам вращается с определенной скоростью, бумага па барабане калибрована, что позволяет измерять изменения объема легких и скорость потока вол-духа
Объемная скорость воздушного потока является главным фактором, определяющим вентиляторную способность легких. Объемную скорость потока можно определить по экспираторному маневру жизненной емкости легких, если учесть затраченное на него время. При использовании спирометра, подобного тому, что изображен на рис. 4-1, это время определяется на основании скорости вращения цилиндра. С помощью данных вертикальной оси, представляющих объем (VC), и данных горизонтальной оси, показывающих отсчет времени, рассчитывается объемная скорость воздушного потока (объем/время).
Типичная спирограмма, полученная таким способом, показана на рис. 4-2. Объем легких на вершине спирограммы — TLC. По мере того, как пациент выдыхает, регистрируется кривая, которая постепенно уплощается при приближении к концу выдоха, т. е. к уровню остаточного объема легких. Из спирограммы экспираторного маневра выводят несколько ключевых величин.
Объем форсированного выдоха за 1 секунду (ОФВ,; FEV,) представляет собой количество воздуха, выдохнутого за первую секунду. Принято выражать FEV, в процентах к форсированно!^ жизненной емкости легких (ФЖЕЛ; FVC). Здоровые
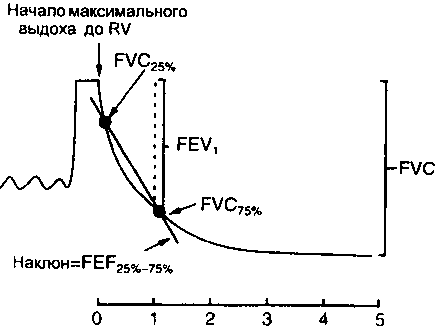
Рис. 4-2. Спирометрические- измерения, полученные в процессе форсированного выдоха от уровня TLC до RV (FVC)
64
