
Лекция 2
Аминокислоты, из которых сложена полипептидная цепь (Рис.2-1), могут находиться в двух стерических формах: L и D.

Рис.2-1. Боковые цепи двадцати стандартных аминокислотных остатков, исходящие из С атомов главной цепи. Белыми кружками показаны С атомы главной цепи, серыми — С атомы боковых групп, светло-серыми — H атомы боковых групп, синими — N атомы боковых групп, красными — O атомы боковых групп, желтыми — S атомы боковых групп.
Эти формы, L и D, зеркально-симметричны: в них массивный боковой радикал (R) и Н-атом, стоящие при -углероде (С) аминокислоты, меняются местами (стрелки указывают углубление атомов в рисунок):
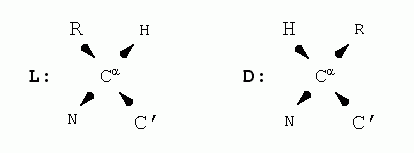
L и D форм нет только у глицина (Gly), "боковая цепь" которого состоит лишь из Н-атома. Белковые цепи сложены только из остатков L-аминокислот. Только они кодируются генами. D-аминокислотные остатки — они встречаются в пептидах — не кодируются при матричном синтезе белка, а синтезируются специальными ферментами. Рацемизация (L D переход) спонтанно в белках практически не происходит. Не происходит она и при биосинтезе, — хотя часто встречается при чисто химическом синтезе пептидов, где на борьбу с рацемизацией уходит много сил. Аминокислоты в белковой цепи связаны между собой пептидными связями C' и N атомов (Рис.2-2).

Рис.2-2. Полипептид: главная цепь и боковая группа (Ser) на ней. Пептидные группы заштрихованы. Показаны углы внутреннего вращения в главной () и боковой () цепях. Стрелки указывают направление вращения, ведущее к росту угла поворота ближней к нам части цепи относительно более отдаленной ее части. Картинка взята из [3] и адаптирована.
Важную роль в структуре белка играет как жесткость этих связей, так и плоская форма всей пептидной группировки

И
то, и другое обеспечивается так называемой
sp2-гибридизацией
электронов N и С' атомов. "Гибридизация"
электронных орбит — это чисто
квантовый эффект. Sp2-гибридизация
преобразует одну сферическую s-
и две вытянутые p-орбиты электронов
атома в три sp2-орбиты.
Эти три орбиты вовлекают атом в три
ковалентные связи, лежащие в одной
плоскости (<). Вовлеченные в
sp2-гибридизацию
электроны ковалентно связанных C' и N
атомов создают "делокализованное"
электронное облако, охватывающее оба
эти атома, и распространяющиеся также
— через связь СО — на атом
О (именно поэтому связи C'![]() N
и C
N
и C![]() O
рисуются как равноправные "полуторные",
O
рисуются как равноправные "полуторные", ![]() ).
Но у C и N атомов есть еще p-электроны
кроме тех, что уже задействованных в
sp2
орбитах! И так как эти p-орбиты имеют
форму "восьмерок", перпендикулярных
всем трем sp2-орбитам
(<), то дополнительная связь этих
p-электронов — связь, требующая
сближения "восьмерочных" орбит и
"обобществления" (т.е. переходов с
атома на атом) находящихся на них
электронов,
).
Но у C и N атомов есть еще p-электроны
кроме тех, что уже задействованных в
sp2
орбитах! И так как эти p-орбиты имеют
форму "восьмерок", перпендикулярных
всем трем sp2-орбитам
(<), то дополнительная связь этих
p-электронов — связь, требующая
сближения "восьмерочных" орбит и
"обобществления" (т.е. переходов с
атома на атом) находящихся на них
электронов,

— это обобществление p-электронов препятствует вращению вокруг С'-N связи.
Хочу напомнить, что делокализация электронов, их переход с атома на атом — основная причина образования химических связей. Это следует из принципа неопределенности Гайзенберга:
|
px
|
(2.1) |
Здесь
p — неопределенность в импульсе
частицы, x — неопределенность в ее
координате, а ![]() h/2, где h — постоянная Планка.
Так как направление движения электрона
в атоме не может быть известно, то p
|p| = mv, где v — скорость, а m —
масса частицы. Следовательно,
h/2, где h — постоянная Планка.
Так как направление движения электрона
в атоме не может быть известно, то p
|p| = mv, где v — скорость, а m —
масса частицы. Следовательно,
v
![]() /(mx)
.
/(mx)
.
В то же время, кинетическая энергия частицы E = mv2/2, т.е.
|
E
|
(2.2) |
Следовательно, при делокализации, когда x возрастает, — энергия частицы падает, и она переходит в более стабильное состояние. Видно, что этот эффект наиболее силен для легких частиц — т.е. электронов. Так делокализация электрона приводит к химической связи.
Длина
химической связи близка к Вандерваальсову
радиусу атома, т.е. составляет 1 —
2![]() (точнее: около 1
(точнее: около 1 ![]() — для связи C-H, N-H или O-H, около 1.2
— 1.3
— для связи C-H, N-H или O-H, около 1.2
— 1.3 ![]() — для С=О, C
— для С=О, C![]() O,
C
O,
C![]() N
и С=С, 1.5
N
и С=С, 1.5 ![]() — для С-С, и около 1.8
— для С-С, и около 1.8 ![]() — для S-S).
— для S-S).
Характерные величины валентных углов составляют около 120о и около 109о. Углы в 120о находятся при sp2-гибридизованных атомах типа C'<, N<, где три валентные связи направлены из центра к вершинам плоского треугольника, углы в 109о — при sp3-гибридизованных атомах типа C<, где четыре связи направлены из центра к вершинам тетраэдра, а также при завязывающих по две связи O< или S< атомах.
Остановимся теперь на характерных величинах флуктуаций, т.е. тепловых колебаний валентных связей и углов. Они могут вносить вклад в гибкость белковой цепи.
Частоты колебаний проявляются в инфракрасных (ИК) спектрах белков. Характерные частоты колебаний таковы: ~ 7x1013 сек-1 — для колебания атома Н, — например, в С-Н связи (при этом длина волны =c/~5мк); и ~ 2x1013 сек-1 — для колебания "тяжелых" групп, — например, в СН3-СН3 связи (при этом =c/~15мк; здесь c — скорость света, 300000 км/сек).
Возбуждены ли эти колебания теплом при комнатной температуре?
Для
ответа на этот вопрос мы должны сравнить
тепловую энергию, приходящуюся на одну
степень свободы ("тепловой квант"
kT) с энергией колебания. Оценим величину
kT при "нормальной" температуре.
Здесь T — абсолютная температура
в градусах Кельвина (Т=300оК
при 27оС,
т.е. при примерно "комнатной"
температуре; К — обозначение
градуса Кельвина), а k (иногда еще пишут
kB)
— постоянная Больцмана [равная 2
(кал/моль)/К, или 0.33x10-23
кал/К в расчете на одну частицу, так как
в одном моле — 6x1023
частиц]. Значит, при комнатной температуре
"тепловой квант" kT = 600 кал/моль, или
(600кал)/(6x1023
частиц), т.е. 10-21
калорий на частицу.
Соответствующую такому тепловому кванту
частоту T
можно найти из соотношения kT = hT
[где постоянная Планка h2![]() =6.6x10-34
Джxсек = 1.6x10-34
калxсек; напомню, что 1 калория (кал) = 4.2
джоуля (Дж)]. Итак, частота T
равна 7x1012
сек-1
при T=300K, т.е. при 27оС.
"Тепловой
квант" не может возбудить более
жесткие, более частые, чем он сам,
колебания.
Значит,
при комнатной температуре валентные
связи "тверды" и не флуктуируют:
для этих связей частота колебаний
~ 2x1013
— 7x1013
сек-1,
т.е. она на порядок больше, чем T
= 7x1012
Джxсек-1.
Однако валентные
связи могут раскачиваться падающим
инфракрасным светом, и на этом основана
ИК-спектроскопия белков. Собственно,
именно ИК спектроскопия и дает сведения
о колебаниях атомов, валентных связей
и валентных углов. Конечно, экспериментально
их исследуют на малых молекулах, а затем
полученную информацию используют при
изучении белков.
В отличие от колебаний длин связей,
тепловые колебания валентных углов, на
порядок более мягкие, — их частоты
лежат в пределах 1012
— 1013
сек-1,
— возбуждены при комнатной температуре.
Однако их характерная амплитуда невелика
— около 5о.
=6.6x10-34
Джxсек = 1.6x10-34
калxсек; напомню, что 1 калория (кал) = 4.2
джоуля (Дж)]. Итак, частота T
равна 7x1012
сек-1
при T=300K, т.е. при 27оС.
"Тепловой
квант" не может возбудить более
жесткие, более частые, чем он сам,
колебания.
Значит,
при комнатной температуре валентные
связи "тверды" и не флуктуируют:
для этих связей частота колебаний
~ 2x1013
— 7x1013
сек-1,
т.е. она на порядок больше, чем T
= 7x1012
Джxсек-1.
Однако валентные
связи могут раскачиваться падающим
инфракрасным светом, и на этом основана
ИК-спектроскопия белков. Собственно,
именно ИК спектроскопия и дает сведения
о колебаниях атомов, валентных связей
и валентных углов. Конечно, экспериментально
их исследуют на малых молекулах, а затем
полученную информацию используют при
изучении белков.
В отличие от колебаний длин связей,
тепловые колебания валентных углов, на
порядок более мягкие, — их частоты
лежат в пределах 1012
— 1013
сек-1,
— возбуждены при комнатной температуре.
Однако их характерная амплитуда невелика
— около 5о.
Итак, колебания валентных связей вовсе не вносят вклада в гибкость белковой цепи, а колебания валентных углов вносят весьма скромный вклад. На самом деле гибкость белковой цепи, а значит — и ее способность складываться и в спирали, и в глобулы обеспечивается вращением (хотя и не вполне свободным вращением, см. ниже) вокруг валентных связей. Поэтому и структура цепи в целом часто описывается просто в терминах углов вращения вокруг валентных связей — тогда она называется "конформацией". Впрочем, очень часто термины "структура" и "конформация" употребляются просто как синонимы.
Основные сведения о вращении атомных группировок вокруг валентных связей тоже поставляет ИК-спектроскопия; как и раньше, я остановлюсь только на результатах. Взаимное расположение атомных группировок, связанных валентной связью, описывается двугранным углом (двугранным — так как это угол между двумя плоскостями — "гранями"). Рисунки 2-2, 2-3 иллюстрируют отсчет этого угла. Отсчет — такой же, как в школьной тригонометрии, если рассматривать ближнюю к нам валентную связь как "вращающуюся стрелку", дальнюю от нас — как "координатную ось", а центральную валентную связь — как "ось вращения". То есть вращение "стрелки" против хода часов увеличивает угол поворота, а по ходу — уменьшает.

Рис.2-3. Отсчет величины двугранного угла (угла поворота): вид поперек (слева) и вдоль (справа) оси вращения. Дальняя от нас валентная связь 0''— c — "ось координатного круга", центральная связь 0'— 0'' — "ось вращения", ближняя к нам связь 0'— a — "стрелка на координатном круге".
Рисунок 2-4 показывает характерное поведение энергии при вращении вокруг связи, соединяющей два sp3-гибридизованных атома (на примере Н3С-СН3 и СН2С-СН2С связей). Такие связи характерны для алифатических боковых групп. Углы вращения боковых групп называются углами , "хи" (см. Рис.2-2). Максимумы такого трехкратного (соответственно симметрии sp3-sp3 связи) потенциала (т.е. потенциала, имеющего три максимума и три минимума при повороте на 360o) соответствуют трем "затененным" конформациям (0о, +120о и -120о), приводящим к сближению (и отталкиванию) электронных облаков. Эти облака отталкиваются, так как образующие их электроны уже задействованы в ковалентных связях. Величина возникающих при этом потенциальных барьеров вращения вокруг Н3С-СН3 связи — около 3 ккал/моль, а характерный размах тепловых флуктуаций вокруг этих минимумов (т.е. те отклонения от них, при которых энергия возрастает на kT) — 15-20о.

Рис.2-4.
Характерный потенциал вращения вокруг
одинарной связи между двумя
sp3-гибридизованными
атомами: вокруг Н3С-СН3
связи (красная кривая) и вокруг
(С-СН2)-(СН2-С)
связи (синяя кривая). Главный энергетический
эффект дает отталкивание электронных
облаков: оно максимально в "затененной"
конформации (при 0, 120, 240о)
и минимально в "скрещенной" (при
60, 180, 300о).
Отталкивание маленьких Н-атомов
несущественно. Однако отталкивание
тяжелых, окруженных большими электронными
облаками С-атомов в окрестности 0о
создает добавочный энергетический
эффект, отличающий поворот вокруг
(С-СН2)-(СН2-С)связи
от поворота вокруг (Н3С)-(СН3)
связи. Для сравнения, стрелкой ![]() отмечена величина kT.
отмечена величина kT.
Когда некоторые из валентностей при sp3 гибридизованных атомах заняты не водородами, а более массивными атомами — их отталкивание повышает соответствующую слишком тесному сближению этих массивных атомов часть барьера. Это показано на Рис.2-4 на примере вращения вокруг центральной связи в (С-СН2)-(СН2-С). Рисунок 2-5 показывает характерное поведение энергии при вращении вокруг пептидной связи, соединяющей два sp2-гибридизованных атома (С' и N). Угол вращения вокруг этой связи называется углом (Рис.2-2). Потенциал двукратен (т.е. имеет два максимума и два минимума при повороте на 360o), соответственно симметрии sp2-sp2 связи. Потенциальные барьеры велики из-за участия в пептидной связи p-электронов (как о том говорилось в начале лекции), минимумы потенциала приходятся на 0o и 180o (где p-орбиты, стягивающие С'- и N-атомы, наиболее сближены), а его максимумы — на 90o и 270o (где эти стягивающие p-орбиты наименее сближены и, следовательно, хуже всего связаны друг с другом). Из-за высоких барьеров характерный размах тепловых флуктуаций угла вращения вокруг таких связей невелик — около 10о.

Рис.2-5. Характерный потенциал вращения вокруг кратной связи, соединяющей два sp2-гибридизованных атома (С' и N) в пептидной связи. Справа показана связь электронных p-орбит при угле, равном 0o (или 180o). Для всех (за исключением пред-пролиновых) пептидных связей энергия (красная кривая) при 0о выше, чем при 180о, из-за отталкивания массивных C-атомов. Эта разность энергий мала для пептидной связи, находящейся перед Pro (синяя кривая), имеющим не один, а два С-атома при N-атоме. См. текст и рисунок, где приведена структурая формула пролина.
Стоит отметить, что отталкивание массивных C атомов делает cis конформацию (=0о) энергетически довольно невыгодной; поэтому почти все пептидные группы в белках находятся в trans конформации (=180о).

Исключение составляет пептидная связь, предшествующая пролину (имино-, а не аминокислоте): в Pro — два почти симметричных массивных радикала при N атоме (-СНС2 и -СН2С, см. Рис.2-1), так что для этой связи trans конформация лишь ненамного лучше, чем cis.

И в глобулярных белках, и в развернутых (т.е. флуктуирующих, не имеющих фиксированной структуры) пептидах наблюдается около 90% trans и 10% cis пролинов. Хочу обратить ваше внимание на эту закономерность — что выгодно само по себе, то чаще встречается и в глобулярных белках. Мы столкнемся с ней еще не раз.
Наконец, рассмотрим потенциал вращения вокруг связи, соединяющей sp3 гибридизованный и sp2 гибридизованный атомы. Углы вращения вокруг такой связи называются углами (вращение вокруг N-C связи) и (вращение вокруг C-С' связи) (Рис.2-2). При вращении по каждому из них возникает шестикратный (6 минимумов и 6 максимумов при повороте на 360o) потенциал с довольно низкими барьерами (Рис.2-6): их высота, 1 ккал/моль — порядка энергии тепловых колебаний (составляющей, как мы помним, 0.6 ккал/моль при комнатной температуре). Именно почти свободное вращение по углам и вокруг такого рода связей (между N и С и между C и C') в главной цепи полипептида и обеспечивает основную гибкость белковой цепи.

Рис.2-6. Характерный потенциал вращения вокруг одинарной связи между sp3- и sp2-гибридизованными атомами (на примере вращения вокруг Н3С-С5Н6 связи).
