
- •Тема 1.1. Основні закони хімії
- •Закон збереження маси речовини
- •Контрольні запитання:
- •Тема 1.2. Оксиди
- •Визначення. Класифікація оксидів.
- •Контрольні запитання:
- •Тема 1.3. Основи
- •Визначення. Класифікація основ.
- •Контрольні запитання:
- •Тема 1.4. Кислоти
- •Визначення. Класифікація кислот.
- •Контрольні запитання:
- •Тема 1.5. Солі
- •Визначення. Класифікація солей.
- •Контрольні запитання:
- •Тема 1.6. Хімічний зв'язок
- •Поняття про хімічний зв'язок. Типи хімічного зв’язку.
- •Контрольні запитання:
- •Тема 1.7. Електролітична дисоціація. Реакції йонного обміну
- •Контрольні запитання:
- •Тема 1.8. Окисно-відновні реакції
- •Контрольні запитання:
- •Тема 2.1. Загальна характеристика металів
- •Контрольні запитання:
- •Тема 2.2. Корозія металів
- •Корозія металів. Види корозії.
- •Контрольні запитання:
- •Тема 2.3. Лужні метали
- •Контрольні запитання:
- •Тема 2.4. Кальцій
- •Кальцій.**
- •Контрольні запитання:
- •Тема 2.5. Сполуки Кальцію
- •Контрольні запитання:
- •Тема 2.6. Алюміній
- •Контрольні запитання:
- •Тема 2.7. Залізо
- •Контрольні запитання:
- •Тема 2.8. Сульфур. Сірка.
- •Контрольні запитання:
- •Тема 2.9. Сполуки Сульфуру
- •Контрольні запитання:
- •Тема 2.10. Сульфатна кислота та її солі
- •Контрольні запитання:
- •Тема 2.11. Нітроген. Азот.
- •Контрольні запитання:
- •Тема 2.12. Аміак. Солі амонію.
- •Контрольні запитання:
- •Тема 2.13. Сполуки Нітрогену
- •Контрольні запитання:
- •Тема 2. 14.Фосфор
- •Фосфор.
- •Контрольні запитання:
- •Тема 2.15. Сполуки Фосфору
- •Контрольні запитання:
- •Тема 2.16. Карбон. Вуглець.
- •Контрольні запитання:
- •Тема 2.16. Сполуки Карбону
- •Контрольні запитання:
- •Тема 2.18. Силіцій.
- •Контрольні запитання:
- •Тема 2.19. Сполуки Силіцію.
- •Контрольні запитання:
- •Тема 3.1. Теорія будови органічних речовин о.М. Бутлерова
- •Контрольні запитання:
- •Тема 3.2. Алкани
- •Контрольні запитання:
- •Тема 3.3. Алкени
- •Контрольні запитання:
- •Тема 3.4. Алкіни
- •Контрольні запитання:
- •Тема 3.5. Алкадієни (дієнові вуглеводні)
- •Контрольні запитання:
- •Тема 3.6. Ароматичні вуглеводні (арени)
- •Контрольні запитання:
- •Тема 3.7. Природні джерела вуглеводнів
- •Контрольні запитання:
- •Тема 4.1. Одноатомні спирти
- •Контрольні запитання:
- •Тема 4.2. Багатоатомні спирти
- •Контрольні запитання:
- •Тема 4.3. Феноли
- •Контрольні запитання:
- •Тема 4.4. Альдегіди
- •Контрольні запитання:
- •Тема 4.5. Карбонові кислоти
- •Контрольні запитання:
- •Тема 4.6. Естери
- •2. Номенклатура:
- •Контрольні запитання:
- •Тема 4.7. Жири. Мило
- •Контрольні запитання:
- •Тема 5.1. Вуглеводи. Глюкоза
- •Контрольні запитання:
- •Тема 5.2. Сахароза
- •Контрольні запитання:
- •Тема 5.3. Крохмаль і целюлоза
- •Контрольні запитання:
- •Тема 5.4. Аміни
- •Контрольні запитання:
- •Тема 5.5. Амінокислоти
- •Контрольні запитання:
- •Тема 5.6. Білки
- •Контрольні запитання:
Контрольні запитання:
-
Які речовини називають амінами?
-
Які хімічні властивості притаманні амінам?
-
Які фізичні властивості має анілін?
-
Якісна реакція на анілін.
-
Яке практичне значення аніліну?
-
До розчину анілін додали надлишок бромної води. Уторилося 6,6 г осаду. Знайдіть масу аніліну, яку витратили на реакцію.
-
Яку масу бензену потрібно ввести в реакцію для синтезу 42 г аніліну, якщо масова частка виходу нітробензену становить 785, а з 32,8 г нітробензену утворюється 20 г аніліну?
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 149.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 18, § 157, с. 164-165.
-
Стахеєв О.Ю. Хімія. Узагальнюючі схеми і таблиці. – Тернопіль.: «Богдан», 1998. – с. 44.
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. ІХ, §§ 1-7, с. 186-192.
Тема 5.5. Амінокислоти
План
-
Визначення та загальна формула.
-
Номенклатура.*
-
Ізомерія.*
-
Фізичні властивості
-
Хімічні властивості.**
-
Добування.*
-
Застосування
1. Амінокислоти – органічні сполуки, що містять одночасно аміногрупу –NH2 і карбоксильну групу –СООН.
Загальна формула амінокислот: NH2–R–СООН.
2. Назви амінокислот утворюють від назв відповідних карбонових кислот з додаванням префіксу аміно-. Однак амінокислоти, які входять до складу білків, мають також історичні назви. Наприклад: амінооцтова кислота називається гліцином, амінопропіолнова кислота – аланіном.
3. Ізомерія: залежно від взаємного розміщення карбоксильної і аміногрупи розрізняють α-, β-, γ-, δ-, ε-амінокислоти.
γ β α γ β α
СН3–СН–СН2–СООН СН3–СН2–СН–СООН
| |
NH2 NH2
β-амінобутанова кислота α-амінобутанова кислота
4. Амінокислоти – кристалічні речовини, мають високі температури плавлення, розчиняються у воді. Цим властивостям відповідає структура біполярного йона:
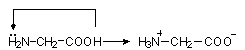
5. Амінокислоти проявляють амфотерні властивості.
1) Як кислоти реагують з металами, оксидами металів, лугами і спиртами:
NH2 –СН2–СООН + NaOH→ NH2 –СН2–СООNa + H2O
NH2 –СН2–СООН + СН3OH→ NH2 –СН2–СООСН3 + H2O
2) Як основи реагують з кислотами, утворюючи солі:
NH2 –СН2–СООН + HCl → [NH3 –СН2 –СООН]Cl
3) реагують між собою за допомогою пептидних зв’язків, утворюючи поліпептиди (реакція поліконденсації):
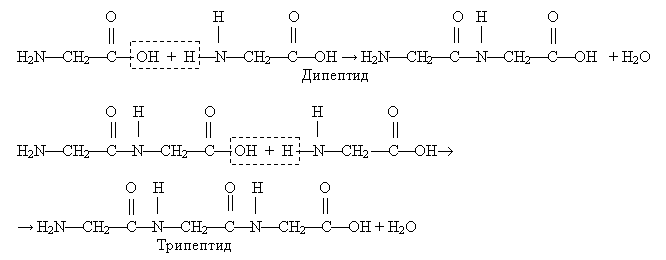 6.
Добування:
6.
Добування:
1) гідроліз білків
2) з карбонових кислот: СН3СООН + Cl2 → ClСН2СООН + HCl
ClСН2СООН + NH3 → NH2CH2COOH + HCl
7.Застосування: 1) у медицині для харчування важкохворих і як ліки;
2) у складі білків харчових продуктів людина отримує всі необхідні
амінокислоти;
3) з амінокапронової і аміноенантової кислот добувають синтетичні
волокна – капрон і енант.
Контрольні запитання:
-
Які органічні речовини називаються амінокислотами? Загальна формула амінокислот.
-
Які хімічні властивості характерні для амінокислот?
-
Що називається реакцією поліконденсації?
-
Яке практичне значення амінокислот?
-
Амінооцтову кислоту одержали з оцтової кислоти масою 12 г та виходом 60%. Який об’єм розчину з масовою часткою лугу (NaOH) 15% (густина 1,16 г/см3) потрібно використати для нейтралізації добутої амінокислоти?
Література:
-
Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 150-151.
-
Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІІ, Гл. 18, § 158, с. 165-167.
-
Стахеєв О.Ю. Хімія. Узагальнюючі схеми і таблиці. – Тернопіль.: «Богдан», 1998. – с. 45.
-
Березан О.В. Органічна хімія. – К.: Абрис, 2000. – Р. ІХ, §§ 11-13, с. 198-203.
